Mikro-CT-Bewertung von Lückenbereichen entlang der Guttapercha-Dichtstoffschnittstelle in ovalen Kanälen
Maschinenübersetzung
Der Originalartikel ist in EN Sprache (Link zum Lesen) geschrieben.
Zusammenfassung
Ziel: Die Bewertung der interfacialen Anpassung (bereich mit Lücken) von zwei Wurzelkanalfüllern (EndoSequence BC Sealer und AH Plus) an einem konventionellen Guttapercha (GP) Kegel (GP-Füller-Schnittstelle) in ovalen Kanälen, die mit der Einzelkegeltechnik gefüllt wurden.
Methodik: Sechzehn Zähne mit ovalen Kanälen wurden ausgewählt, in einem mikro-Computertomographen gescannt und paarweise entsprechend dem Volumen, dem Seitenverhältnis und der Konfiguration der Wurzelkanäle zugeordnet. Die Wurzelkanäle wurden dann nacheinander mit WaveOne Gold Primary und Large Instrumenten vorbereitet, gefolgt von der Füllung mit WaveOne Large GP-Spitzen, die entweder mit dem vorgefertigten kalziumsilicatbasierten EndoSequence BC Sealer oder dem epoxidharzbasierten AH Plus Füller (n = 8 pro Gruppe) unter Verwendung der Einzelkegeltechnik assoziiert waren. Nach 7 Tagen Lagerung in einer phosphate-gepufferten Salzlösung bei 37°C wurden die Proben erneut gescannt und die rekonstruierten Bilder segmentiert, um die Füllmaterialien (Füller und GP-Kegel) vom Dentin zu unterscheiden. Insgesamt wurden 453 Querschnittsschnitte bewertet und entsprechend dem Vorhandensein oder Fehlen von Lücken an der GP-Füller-Schnittstelle kategorisiert. Der Mann-Whitney U-Test überprüfte die Unterschiede zwischen den Gruppen und wurde bei alpha = 5% als signifikant angesehen.
Ergebnisse: Die Lücken waren nicht homogen in zweidimensionalen axialen Querschnittsbildern verteilt, und keines der Proben zeigte vollständig lückenfreie Bereiche entlang der gesamten GP-Dichtungsoberfläche. Wurzelkanäle, die mit EndoSequence BC Sealer und AH Plus gefüllt waren, wiesen 171 (37,75%) bzw. 136 (30,02%) Schnitte mit Lücken in der GP-Dichtungsoberfläche auf, und diese Häufigkeiten waren statistisch signifikant (p = .000).
Schlussfolgerungen: Obwohl keines der Proben einen lückenfreien Bereich entlang der gesamten GP-Dichtungsoberfläche hatte, zeigten ovale Kanäle, die mit AH Plus gefüllt waren, weniger Lücken als die, die mit EndoSequence BC Sealer gefüllt waren.
Einleitung
Hydraulische Zemente, wie bioaktive Calciumphosphatkeramiken, wurden aufgrund ihrer hohen Biokompatibilität, osteoinduktiven und osteokonduktiven Eigenschaften sowohl in der Orthopädie als auch in der Zahnmedizin (Daculsi et al., 1990; Demirkiran, 2012; LeGeros, 1988) umfassend für die Knochenregeneration verwendet. In der Endodontie haben hydrophile bioaktive calcium-silikatbasierte Dichtstoffe (CSS) seit der Einführung von iRoot SP (Innovative BioCeramix Inc.) im Jahr 2007 erhebliche Aufmerksamkeit erlangt. Dieses große Interesse basierte auf der Prämisse, dass CSS als abgeleitete Version des MTA-Zements entwickelt wurden, jedoch mit optimierten Handhabungs-, biologischen und Viskositätseigenschaften (Candeiro et al., 2012; Silva et al., 2017; Silva-Almeida et al., 2017). Dieses Material wird normalerweise als gebrauchsfertige injizierbare Paste präsentiert, die in einer luftdichten Spritze aufbewahrt wird und ihre Anwendung direkt im Wurzelkanalraum ermöglicht. Die inhärenten Eigenschaften und die klinische Nützlichkeit von CSS haben das Verfahren zur Wurzelkanalfüllung für Zahnärzte aller Fähigkeitsstufen vereinfacht. Daher war es sehr beliebt in der endodontischen Gemeinschaft, selbst ohne die vollständige Unterstützung der Wissenschaft bezüglich einiger kritischer Aspekte seiner in vitro-Eigenschaften (Elyassi et al., 2019; Silva et al., 2021; Tanomaru-Filho et al., 2017; Torres et al., 2020; Zordan-Bronzel et al., 2019), sowie dem Mangel an langfristigen Beobachtungsergebnissen aus randomisierten perspektivischen klinischen Studien.
Ursprünglich wurden CSS, als abgeleitete Version der MTA, entwickelt, um den gesamten Kanalraum gemäß dem Konzept des „primären Monoblocks“ auszufüllen, das die Existenz nur einer Schnittstelle umfasst, die zirkumferential zwischen dem Material und den Wänden des Wurzelkanals verläuft, um die langfristige Flüssigkeitsdichtheit zu verbessern (Tay & Pashley, 2007). Dennoch sind CSS nicht geeignet, als einzigartiger Füllstoff verwendet zu werden, da die Möglichkeit besteht, dass sie nach dem endgültigen Aushärten nicht eindringen, was eine Nachbehandlung im Bedarfsfall ausschließt (Eymirli et al., 2019; Hess et al., 2011). Die Lösung bestand darin, ein anderes Material zu verwenden – einen Master-Guttapercha (GP) Kegel – um den Dichtstoff in die Unregelmäßigkeiten des Kanals zu treiben und als weichen Kern zu dienen, der eine Wurzelkanalnachbehandlung ermöglicht. Obwohl diese Technik darauf abzielte, den Wurzelkanalraum durch das Zementieren eines zuvor angepassten GP-Masterkegels mit CSS zu füllen, führt sie auch eine zusätzliche Schnittstelle zur Füllmasse ein. Die Idee eines Wurzelfüllmonoblocks mit zwei zirkumferentialen Schnittstellen (GP-Dichtstoff und Dichtstoff-Dentin), die eine einzige kohäsive Einheit bilden, hat mit dem Aufkommen von methacrylatbasierten Dichtstoffen vor fast zwei Jahrzehnten an Aufmerksamkeit gewonnen. Laut einigen Autoren wäre dieser Dichtstoff das ideale Füllmaterial, um eine ordnungsgemäße koronale Abdichtung zu gewährleisten und die Bruchfestigkeit der Zähne zu verbessern (Shipper et al., 2004, 2005; Teixeira et al., 2004). Leider zeigten langfristige klinische Ergebnisse von endodontischen Behandlungen eine hohe Ausfallwahrscheinlichkeit in Wurzelkanälen, die mit methacrylatbasierten Dichtstoffen gefüllt waren, im Vergleich zu herkömmlichen Materialien (Barborka et al., 2017; Strange et al., 2019), was die Ergebnisse früherer laboratoriumsbasierter Studien unterstützt (De-Deus et al., 2009, 2011; Hiraishi et al., 2007, 2008; Tay, Loushine, et al., 2005a; Tay Pashley, Williams, et al., 2005; Tay, Pashley, Yiu, et al., 2005; Tay et al., 2007).
Die Fähigkeit des Dichtungsmittels, sowohl an dentinale Wände als auch an GP zu haften, ist eine wünschenswerte Eigenschaft, da sie eine wichtige Voraussetzung für die Erreichung einer flüssigkeitsdichten Versiegelung im gesamten Wurzelkanalsystem darstellt. Die Haftung von CSS an Wurzeldentin wurde bereits in mehreren Studien behandelt (Neelakantan et al., 2015; Oliveira et al., 2016; Sagsen et al., 2011; Silva et al., 2019). Es gibt jedoch nur wenige Beweise für die Qualität der interfacialen Anpassung zwischen CSS und konventionellem GP (Gandolfi et al., 2013; Kim et al., 2017, 2018; Moinzadeh et al., 2015; Pedullà et al., 2020; Viapiana et al., 2016; Zare et al., 2021). Idealerweise ist dies ein wichtiger Aspekt, da das Dichtungsmittel gleichzeitig an sowohl Dentin als auch GP haften sollte, um die Gesamtqualität der Füllung zu verbessern. Andernfalls kann eine unterschiedliche Wechselwirkung zwischen ihnen zur Entwicklung von interfacialen Lücken führen, kleinen leeren Bereichen, die in der Regel radiografisch nicht identifiziert werden können. Ein solches interfaciales Versagen kann die Stabilität des GP-Kegels beeinträchtigen und als Weg für Bakterien und deren Abfallprodukte fungieren, was folglich die langfristige Gesamtqualität der Wurzelkanalbehandlung gefährden kann.
Das Ziel der vorliegenden Studie war es, die Qualität der interfacialen Anpassung (Bereiche mit Lücken) zwischen konventionellen GP-Kegeln und dem vorgefertigten Kalzium-Silikat-EndoSequence BC Sealer (Brasseler USA) mithilfe von mikro-Computertomographie (Mikro-CT) als analytisches Werkzeug zu bewerten. Der AH Plus Sealer (Dentsply DeTrey GmbH) wurde als Referenz für den Vergleich verwendet. Die getestete Nullhypothese war, dass die Qualität der Schnittstellenanpassung nicht von der Art des Sealers beeinflusst wird.
Material und Methoden
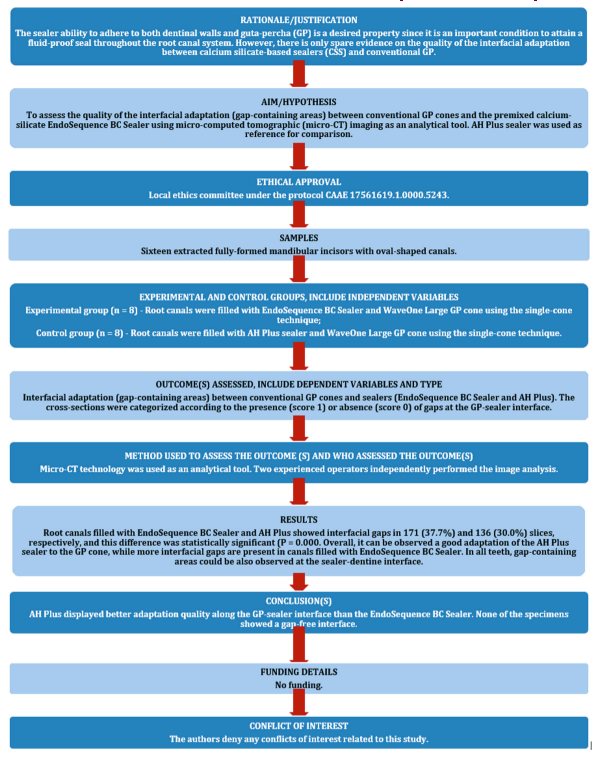
Das Manuskript dieser Laborstudie wurde gemäß den Richtlinien der Preferred Reporting Items for Laboratory studies in Endodontology (PRILE) 2021 (Nagendrababu et al., 2021) verfasst. Die Schritte dieser Studie sind im PRILE-Flussdiagramm dargestellt (Abbildung 1).
Schätzung der Stichprobengröße
Eine punktbasierte Bewertung wurde verwendet, um das Vorhandensein von Lücken im Füllmaterial pro Mikro-CT-Schnitt zu bewerten. Die Anzahl der benötigten Schnitte zur Überprüfung signifikanter Unterschiede zwischen den Gruppen wurde basierend auf der Studie von Eltair et al. (2018) geschätzt, in der eine Effektgröße von 0,43 zusammen mit einem Alpha-Fehler von 0,05 und einer Beta-Power von 0,95 in ein unabhängiges t-Test-Verfahren (G*Power 3.1 für Macintosh; Heinrich Heine, Universität Düsseldorf) eingegeben wurde. Die Ausgabe zeigte ein Minimum von 139 Schnitten pro Gruppe an. Unter Berücksichtigung der Bewertung von 15–20 Querschnitten pro Zahn (erhalten in einem Abstand von 0,5 mm) wurde eine Gesamtzahl von acht Zähnen pro Gruppe für die vorliegende Studie festgelegt.
Auswahl und Vorbereitung der Proben
Das lokale Ethikkomitee genehmigte diese Studie (CAAE 17561619.1.0000.5243). Eine Probe von 237 mandibularen Schneidezähnen, die aus einer Zahnbank entnommen wurden, wurde sowohl in mesiodistaler als auch in buccolingualer Richtung röntgenologisch untersucht, um Zähne mit mehr als einem Wurzelkanal, unvollständiger Wurzelbildung oder Fraktur auszuschließen. Aus dieser ersten Stichprobe wurden 196 Zähne ausgewählt und in einem Mikro-CT-Gerät (SkyScan 1173; Bruker-microCT) bei 70 kV, 114 mA, 19,79 μm (Pixelgröße), 180°-Drehung um die vertikale Achse mit Schritten von 0,7°, Rahmenmittelwert von 5, unter Verwendung eines 1,0 mm dicken Aluminiumfilters gescannt. Die Projektionsbilder wurden (NRecon v.1.7.16; Bruker-microCT) mit ähnlichen Parametern zur Korrektur von Ringartefakten (4), Kontrastgrenzen (0–0,05) und Strahlenhärtungskorrektur (40%) rekonstruiert, was zu 800–900 Graustufenquerschnitten pro Zahn führte, die vom Zement-Schmelz-Übergang bis zur Spitze reichten. Nach dem Ausschluss von Zähnen mit zwei oder mehr Kanälen oder signifikanten zusätzlichen anatomischen Strukturen wurden die Querschnittsbilder von 146 Proben mit einer automatischen Routine segmentiert, die in der ImageJ-Software (Fiji v.1.51n; Fiji) implementiert ist, um dreidimensionale (3D) Modelle der Proben zu erstellen sowie das Volumen (in mm3) und das Seitenverhältnis (AR) der Wurzelkanäle zu berechnen (CTAn v.1.6.6.0; Bruker-microCT; De-Deus et al., 2020). Das AR ist die mathematische Darstellung der Kanalzirkularität und wurde berechnet, indem das Verhältnis zwischen den Haupt- und Nebenachsen einer an die rekonstruierten Kanäle in jedem Querschnitt angepassten Ellipse unter Verwendung des Formbeschreibungs-Plugins der ImageJ-Software ermittelt wurde. Das AR der Wurzelkanäle wurde für jeden Querschnitt berechnet und in einem Diagramm dargestellt. Anschließend wurde die Software CTAn v.1.6.6.0 (Bruker-microCT) verwendet, um 3D-Modelle der Wurzelkanäle der Zähne zu erstellen, während CTVol v.2.3.2.0 (Bruker-microCT) qualitativ zur Analyse der Wurzelkanalkonfiguration eingesetzt wurde (Abbildung 2).
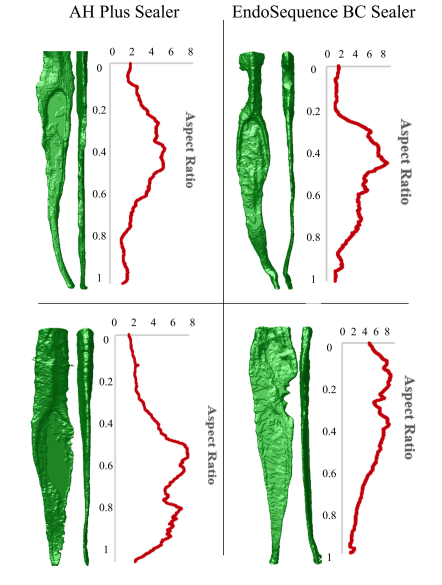
Der Paarabgleichungsprozess wurde zunächst durchgeführt, indem Wurzelkanäle mit ähnlichem Volumen (nicht höher als 2 mm3), ähnlichen AR-Grafikkurven und ähnlicher Kanal-Konfiguration identifiziert wurden. Eine Stichprobenauswahl unter Verwendung dieser drei Parameter ist ein Versuch, die interessierenden Variablen zu isolieren und die Verzerrung zu reduzieren, die durch anatomische Variation entstehen kann, die ein Störfaktor in einer Studie dieser Art sein könnte. Nach diesen strengen Auswahlkriterien wurden 16 Zähne mit ovalen Kanälen (grafische Kurven von AR > 4) und einem maximalen Volumen von 5 mm3 gepaart (Abbildung 3), verteilt auf zwei Versuchsgruppen (n = 8), gescannt und rekonstruiert unter Verwendung der oben genannten Parameter, mit Ausnahme der Pixelgröße (14,37 μm) und der Rotation (360°) in Schritten von 0,5°.
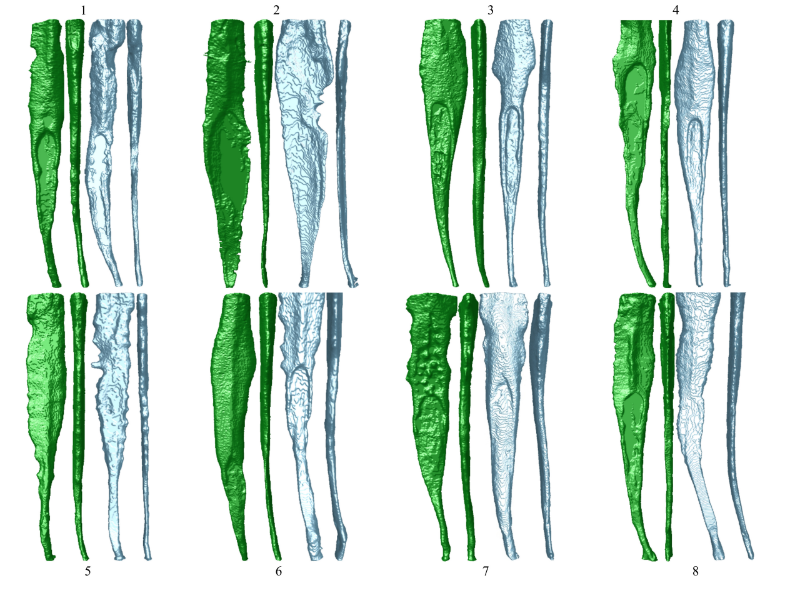
Wurzelkanalvorbereitung
Jede Wurzel wurde in Parafilm-M (Bemis NA) eingewickelt und in Polyvinylsiloxan (Speedex; Coltene) eingebettet, um ein geschlossenes System zu simulieren und die Proben während der experimentellen Verfahren zu stabilisieren. Sowohl die Vorbereitung als auch die Füllverfahren der Wurzelkanäle wurden von einem Spezialisten für Endodontie mit mehr als 8 Jahren Erfahrung durchgeführt.
Nach dem konventionellen Zugang wurde eine K-Datei der Größe 10 (Dentsply Sirona Endodontics) verwendet, um die Durchgängigkeit zu bestätigen und die Arbeitslänge 1,0 mm vor dem apikalen Foramen festzulegen. Anschließend wurden die Wurzelkanäle nacheinander mit WaveOne Gold Primary- und Large-Instrumenten (Dentsply Tulsa Dental Specialties) erweitert, die mit dem VDW Silver-Motor (VDW) im voreingestellten Programm „WAVEONE ALL“ betrieben wurden. Zuerst wurde WaveOne Gold Primary bis zur Arbeitslänge in einer langsamen Hin- und Herbewegung mit 3 mm Amplitude verwendet. Nach drei Bewegungen wurde das Instrument aus dem Kanal entfernt und mit Alkohol gereinigt. Die Arbeitslänge wurde nach drei Wellen der Instrumentierung erreicht. Dann wurde WaveOne Gold Large bis zur Arbeitslänge auf die gleiche Weise wie das Primary-Instrument verwendet. Die apikale Durchgängigkeit wurde während der Instrumentierungsverfahren mit einer K-Datei der Größe 15 (Dentsply Sirona Endodontics) bestätigt. Nach jedem Vorbereitungsschritt mit reziproken Instrumenten wurden die Wurzelkanäle mit 3 ml 2,5% Natriumhypochlorit (NaOCl) unter Verwendung einer 31-G NaviTip-Doppelseitenportnadel (Ultradent Inc.) irrigiert, die bis zu 1 mm vor der Arbeitslänge eingeführt wurde, während nach der Durchgängigkeit 1 ml des Spülmittels abgegeben wurde. Die Entfernung der Schmierschicht erfolgte mit 3 ml 17% EDTA (5 Minuten), gefolgt von einer abschließenden Spülung mit 2 ml bidestilliertem Wasser. Insgesamt wurden also 20 ml Spüllösung in jedem Wurzelkanal verwendet.
Wurzelkanalfüllung
Die Wurzelkanäle wurden mit Papierpunkten (Dentsply Sirona Endodontics) getrocknet und mit der Einzelkonus-Technik unter Verwendung von WaveOne Large GP-Punkten (Dentsply Sirona Endodontics) gefüllt, die entweder mit EndoSequence BC Sealer (experimentelle Gruppe; n = 8) oder AH Plus (Kontrollgruppe, n = 8) kombiniert wurden. Die getesteten Materialien wurden in separaten Glasplatten gemäß den spezifischen Empfehlungen jedes Herstellers vorbereitet. Für das Obturationsverfahren wurden 80 μl Dichtmittel mit einer Mikropipette entnommen und in jeden Wurzelkanal mit einer Größe 25 K-Datei (Dentsply Sirona Endodontics) in einer gegen den Uhrzeigersinn drehenden Bewegung eingebracht. Dann wurde ein WaveOne Large GP-Konus sanft in den Wurzelkanal bis zur Arbeitslänge eingeführt. Der Überschuss des GP-Konus wurde mit einem Wärmeübertrager (B&L Biotech) auf Höhe des Kanalorifices entfernt und das verbleibende Material wurde mit einem kompatiblen Handstopfer (B&L Biotech) vertikal verdichtet. Die Qualität der Wurzelfüllungen wurde durch digitale Röntgenaufnahmen aus buccolingualer und mesiodistaler Richtung bewertet, und kein Präparat wurde verworfen. Die Zugangshohlräume wurden dann mit Cavit G (3M ESPE) gefüllt und die Proben 7 Tage lang bei 37 °C in einer phosphate-gepufferten Kochsalzlösung gelagert, um die vollständige Aushärtung der Dichtmittel zu ermöglichen. Ein erfahrener Bediener führte alle Verfahren durch. Nach diesem Zeitraum wurden alle Proben erneut bei 100 kV, 80 mA, 14,37 μm, 360°-Drehung in Schritten von 0,3° und einem Rahmenmittel von 5 gescannt, gefiltert durch eine 0,5 mm dicke Aluminiumfolie.
Micro-CT-Analyse
Nach der Rekonstruktion der Projektionsbilder unter Verwendung von Kontrastgrenzen, um die Differenzierung von Dichtungsmaterial, GP-Kegel und Dentin zu ermöglichen, wurden pro Zahn etwa 25 Querschnitte ausgewählt, in denen die GP-Kegel-Schnittstelle beobachtet werden konnte, insgesamt 453 Bilder. Zwei erfahrene Operatoren führten unabhängig die Bildanalyse durch, um die Querschnitte entsprechend der Anwesenheit (Punkt 1) oder Abwesenheit (Punkt 0) von Lücken an der GP-Dichtungsmaterial-Schnittstelle zu kategorisieren. Das Endergebnis wurde durch eine Übereinstimmung zwischen ihnen erreicht.
Statistische Analyse
Der Punkt, der verwendet wurde, um das Auftreten von interfacialen Lücken zwischen GP-Kegeln und den getesteten Dichtungsmaterialien pro Mikro-CT-Querschnitt zu kategorisieren, wurde als Einheit für die statistische Analyse betrachtet, und der Mann-Whitney-U-Test wurde angewendet, um Unterschiede zwischen den Gruppen auf einem signifikanten Niveau von 5 % zu überprüfen (SPSS 21.0; SPSS Inc.).
Ergebnisse
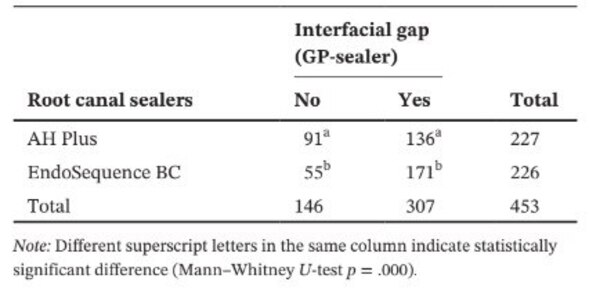
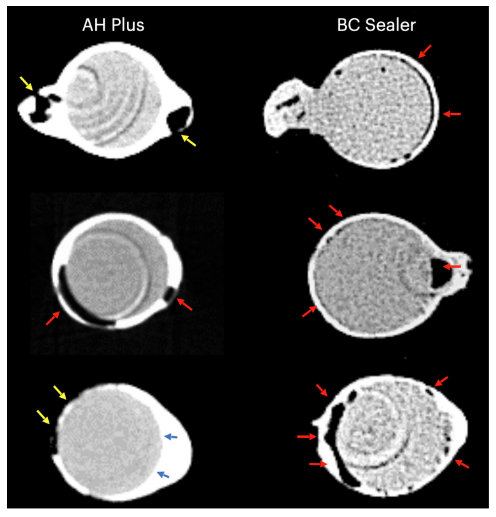
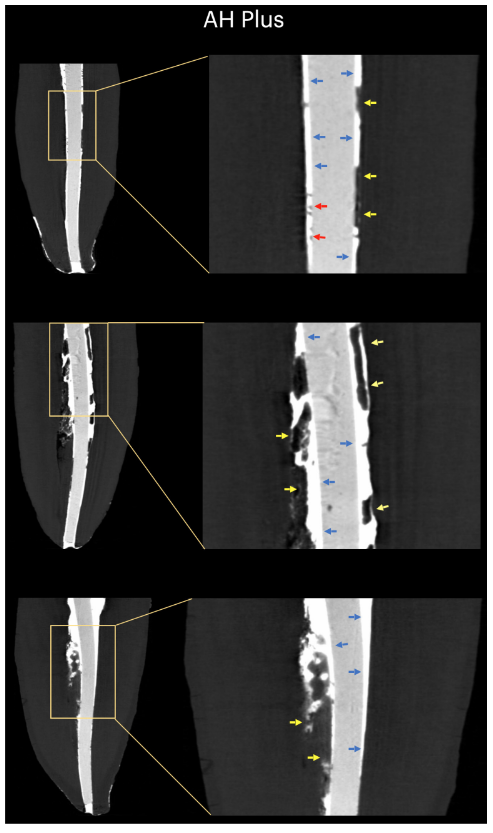
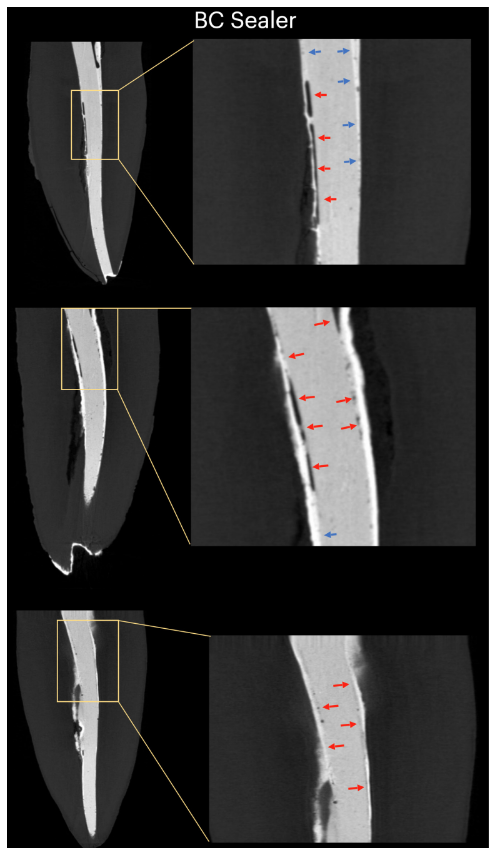
Tabelle 1 zeigt die Anzahl der Mikro-CT-Querschnitte, die entsprechend dem Auftreten von interfacialen Lücken zwischen dem GP-Kegel und den getesteten Dichtungsmaterialien verteilt sind. Lücken waren nicht homogen in den zweidimensionalen (2D) axialen Querschnittsbildern verteilt, und keines der Proben zeigte vollständig lückenfreie Bereiche entlang der gesamten GP-Dichtungsmaterial-Schnittstelle. Wurzelkanäle, die mit EndoSequence BC Sealer und AH Plus gefüllt waren, zeigten interfaciale Lücken in 171 (37,7 %) bzw. 136 (30,0 %) Schnitten, und dieser Unterschied war statistisch signifikant (p = .000). Abbildungen 4–7 zeigen repräsentative transaxiale und sagittale Mikro-CT-Bilder von Wurzelkanälen von mandibulären Schneidezähnen, die mit der Einzelkegeltechnik unter Verwendung von AH Plus und EndoSequence BC Sealer gefüllt sind. Insgesamt kann eine gute Anpassung des AH Plus Dichtungsmaterials an den GP-Kegel beobachtet werden, während mehr interfaciale Lücken in Kanälen vorhanden sind, die mit EndoSequence BC Sealer gefüllt sind. In allen Zähnen konnten auch Bereiche mit Lücken an der Dichtungsmaterial-Dentin-Schnittstelle beobachtet werden.

Diskussion
Die vorliegende Studie verwendete ein nicht destruktives Analysewerkzeug, um die interfaciale Anpassung zwischen konventionellen GP-Kegeln und verschiedenen Wurzelkanaldichtstoffen (AH Plus und EndoSequence BC Sealer) in anatomisch passenden ovalen Kanälen von mandibulären Schneidezähnen zu bewerten, die mit der Single-Cone-Technik gefüllt wurden. Die Ergebnisse zeigten, dass Zähne, die mit EndoSequence BC Sealer gefüllt wurden, eine erheblich höhere Häufigkeit von Querschnittsbildern aufwiesen, die Lücken in der GP-Dichtungsoberfläche zeigten, als die mit AH Plus gefüllten, und die Nullhypothese wurde verworfen.
In der Literatur haben mehrere Studien mit unterschiedlichen Analysemethoden widersprüchliche Ergebnisse über das Vorhandensein von Lücken und Hohlräumen in Wurzelkanälen, die mit CSS gefüllt sind, berichtet (Gandolfi et al., 2013; Kim et al., 2017, 2018; Moinzadeh et al., 2015; Pedullà et al., 2020; Viapiana et al., 2016; Zare et al., 2021). Mit der Mikro-CT-Technologie berichteten Yanpiset et al. (2018) von minimalen Lücken und Hohlräumen in Zähnen, die mit dem CSS TotalFill BC Sealer (FKG Dentaire, La Chaux-de-Fonds, Schweiz) und beschichteten GP-Kegeln gefüllt waren. Ähnlich zeigten Eltair et al. (2018) keinen signifikanten Unterschied in den interfacialen Lücken zwischen TotalFill BC Sealer und AH Plus, kombiniert mit beschichteten oder konventionellen GP-Kegeln, durch eine deskriptive Analyse mit Rasterelektronenmikroskopie. Diese Ergebnisse widersprechen jedoch früheren Erkenntnissen von Zhang et al. (2010), die eine bessere interfaciale Anpassung des iRoot SP Sealers an GP im Vergleich zu AH Plus demonstrierten. Darüber hinaus zeigte Viapiana et al. (2016), dass BioRoot RCS (Septodont) mit einem höheren Prozentsatz an Hohlräumen als AH Plus assoziiert war, während Gandolfi et al. (2013), Kim et al. (2017) und Zare et al. (2021) keine Unterschiede zwischen AH Plus und verschiedenen Marken von CSS berichteten. Diese Inkonsistenzen lassen sich größtenteils durch methodologische Unterschiede erklären, die mit dem Mikro-CT-Gerät (Scan- und Rekonstruktionsparameter), der Auswahl der Proben, der Qualität der Wurzelkanalaufbereitung, der Erfahrung der Betreiber, der Fülltechnik und den physikochemischen Eigenschaften der getesteten Dichtstoffe zusammenhängen. Daher basiert die Begründung zur Interpretation dieser Unterschiede im Vergleich zu den aktuellen Ergebnissen auf der Tatsache, dass die meisten Studien, die Mikro-CT verwendeten, sich auf die Gesamtanalyse des Prozentsatzes an Hohlräumen konzentrierten, die durch die Bewertung des Volumens der Füllmaterialien im Verhältnis zum vorbereiteten Kanalraum berechnet wurden (Gandolfi et al., 2013; Kim et al., 2017, 2018; Moinzadeh et al., 2015; Pedullà et al., 2020; Viapiana et al., 2016). Dieser Ansatz berücksichtigt jedoch nicht die spezifische Interaktion des Dichtstoffs und GP, wie in der vorliegenden Studie demonstriert, die einen spezifischen punktbasierten Parameter verwendet, der hilft, die Inkonsistenzen im Verhältnis zu früheren Ergebnissen zu verstehen.
In dieser Studie hatten ovalförmige Kanäle, die mit konventionellem GP und EndoSequence BC Sealer unter Verwendung der Einzelkonus-Technik gefüllt wurden, eine höhere Anzahl von Schnitten, die Lücken in der GP-Sealer-Schnittstelle aufwiesen, als bei der Verwendung von AH Plus (Tabelle 1). Neben einigen technischen Aspekten der Wurzelkanalfüllung und Unterschieden in den physikochemischen Eigenschaften der Dichtstoffe können die vorliegenden Ergebnisse auch durch Variationen in den chemischen Oberflächenpolaritäten zwischen den getesteten Dichtstoffen und dem Kernmaterial erklärt werden. Insgesamt haben GP-Spitzen nur etwa 20 % der chemischen Zusammensetzung, die GP sein soll, während 60 %–75 % der Zusammensetzung aus Zinkoxidfüllern bestehen. Die verbleibenden Bestandteile sind Wachs oder Harz, um die Spitze flexibler und/oder kompakter zu machen, sowie Metallsalze, um die Radiopazität zu verleihen. Auf organischer versus anorganischer Basis sind GP-Spitzen nur zu 23,1 % organisch (GP und Wachs) und zu 76,4 % anorganische Füllstoffe (Zinkoxid und Bariumsulfat; Friedman et al., 1977). GP hat eine chemische Struktur, die auf der Polymerisation eines Stereoisomers von Isopren basiert, dem Monomer, das Naturkautschuk bildet, was zu einer höheren Kristallinität mit etwa 30 %–40 % Hydrophobizität führt. Mit anderen Worten, die hydrophoben Eigenschaften von GP sind eine Folge seiner aliphatischen chemischen Natur (Le Ferrand & Bacha, 2021). Die anderen beiden Hauptbestandteile von GP-Spitzen sind Zinkoxid, Wachs und Bariumsulfat (anorganische Füllstoffe), die wiederum auch hydrophobe Eigenschaften aufweisen (Friedman et al., 1977; Moorer & Genet, 1982; Wilson et al., 1973; Wolfmeier et al., 2002). Daher ist es möglich, dass die hydrophobe Natur des GP-Konus mehr das CSS abgestoßen hat, ein Material, das für seine Hydrophilie bekannt ist (Hegde & Arora, 2015), als das AH Plus, ein epoxidharzbasiertes Material, das ein hydrophobes Radikal in seinem Molekül hat (Lee et al., 2017), was teilweise die geringere Anzahl von Lücken erklärt, die entlang seiner Schnittstelle beobachtet wurden. Obwohl die Stärke der Polarisationskräfte zwischen hydrophilen und hydrophoben endodontischen Materialien noch bestimmt werden muss, ist es möglich, dass es sich um schwache Kräfte handelt. Folglich ist es unwahrscheinlich, dass sie einen großen Einfluss auf ihre Wechselwirkung haben, insbesondere wenn man bedenkt, dass diese Materialien innerhalb starrer dentinaler Wände eingeschlossen sind. In einer anatomischen Bedingung, in der eine große Menge Dichtstoff benötigt wird, um den Wurzelkanalraum zu füllen, wie bei der Verwendung der Einzelkonus-Technik in ovalförmigen Kanälen, könnte man jedoch hypothetisieren, dass der verfügbare Raum zwischen dem GP-Konus und den dentinalen Wänden genügend Platz für das Wirken dieser Kräfte bieten kann. Wie in den Abbildungen 4 bis 7 gezeigt, wurden die GP-Sealer-Schnittstellenlücken hauptsächlich an den buccalen und lingualen Aspekten der Wurzelkanäle beobachtet, das heißt, in den größten Bereichen zwischen dem Kern und den dentinalen Wänden, in denen sich die größte Menge Dichtstoff befindet. Man könnte argumentieren, dass die vorliegenden Ergebnisse eine Folge des unsachgemäßen Gebrauchs von CSS mit konventionellem GP anstelle von kalziumsilikatbeschichteten Kegeln waren. Bislang hat jedoch kein Hersteller bekannt gegeben, dass CSS nicht mit konventionellen GP-Spitzen verwendet werden könnte. Tatsächlich berichtete eine aktuelle Umfrage, dass nur 22,1 % der CSS-Nutzer vorbeschichtetes GP in ihren Wurzelkanalfüllungen verwendet haben (Guivarc'h et al., 2020), ein Beweis, der das Hauptziel der vorliegenden Studie unterstützt.
Obwohl die Mikro-CT-Technologie nicht-destruktive volumetrische Experimente ermöglicht, hat die hohe Dichte von Füllmaterialien in der Regel einen signifikanten Einfluss auf die Ausgabequalität der rekonstruierten Bilder, insbesondere in den Randbereichen, was die Bewertung von Schnittstellen zu einer echten Herausforderung macht, insbesondere wenn die Dichte zwischen Dichtungsmittel und GP-Kegeln ähnlich ist, was direkt deren Kontraste beeinflusst (Sun et al., 2009; Zeiger et al., 2009). Das bedeutet, dass selbst Bilder, die mit angemessenen Scan- und Rekonstruktionsparametern in geeigneten Mikro-CT-Geräten aufgenommen wurden, oft nicht vernachlässigbare Schwierigkeiten bei der Identifizierung und Unterscheidung der Grenzen zwischen den Wänden des Wurzelkanals und den Füllkomponenten aufweisen. Dies ist ein kritischer methodologischer Aspekt, da die Schwellenwertbestimmung für die Bildsegmentierung ein subjektives Verfahren ist, das von der Erfahrung des Bedieners abhängt und folglich einen direkten Einfluss auf die Genauigkeit und Zuverlässigkeit der Ergebnisse haben kann. Wenn es um nicht-homogene Strukturen wie Dentin, Dichtungsmittel und GP-Kegel geht, ist dies eine ziemlich herausfordernde Aufgabe und immer noch ein nicht einvernehmlicher Aspekt der Mikro-CT-Bewertung. Daher ist es ein Missverständnis zu glauben, dass nur die Pixelgröße die Qualität der aus einem Mikro-CT-Scan erhaltenen Bilder bestimmen würde. Tatsächlich ist es das Zusammenspiel zwischen der Kontrastempfindlichkeit und der räumlichen Auflösung, das definiert, was mit einem CT-Scan erreicht werden kann (Stock 2009). Während die Kontrastauflösung eines bestimmten Bildes ein Maß dafür ist, wie gut ein interessantes Merkmal von dem benachbarten Hintergrund unterschieden werden kann, beschreibt die räumliche Auflösung, wie gut kleine Details abgebildet oder kleine Merkmale in Bezug auf einen Referenzpunkt lokalisiert werden können (Ketcham & Carlson, 2001). In der vorliegenden Studie, obwohl die Proben mit einer Pixelgröße von 14,37 μm gescannt wurden, war die gesamte Kontrastauflösung der erhaltenen Bilder von mittlerer Qualität und daher konnten keine quantitativen volumetrischen Messungen von Lücken durchgeführt werden, was als Einschränkung dieser Studie angesehen werden kann. Die Ausgabequalität war jedoch ausreichend, um die lückenhaltigen Bereiche entlang der GP-Dichtungsmittel-Schnittstelle mithilfe von 2D-transaxialen Bildern zu identifizieren und zu bewerten. Obwohl einige argumentieren mögen, dass die in dieser Studie verwendete Pixelgröße hoch ist, haben Pinto et al. (2021) gezeigt, dass visuelle und automatische Segmentierung auf Mikro-CT-Bilder mit Voxelgrößen von 5 bis 20 µm angewendet werden kann, um die Füllung eines Dichtungsmittels mit Radiopazität zu bewerten, das den ISO 6876:2012-Standard (ISO, 2012) erfüllt, wie das AH Plus (Silva et al., 2013) und das EndoSequence BC Sealer (Candeiro et al., 2012).
Wie in dieser Studie verwendete eine aktuelle Mikro-CT-Untersuchung ebenfalls 2D-Bildschnitte, um die GP-Dichtungsmittel-Schnittstelle in Wurzelkanälen von oberen Frontzähnen zu bewerten, die mit der Einzelkegeltechnik unter Verwendung von konventionellem GP in Verbindung mit AH Plus oder EndoSequence BC-Dichtungsmitteln gefüllt wurden (Zare et al., 2021), jedoch wurde das Scannen in einem Hochauflösungsgerät mit einer kleineren Pixelgröße (6 μm) durchgeführt. Im Gegensatz zu den vorliegenden Ergebnissen hatte die AH Plus-Gruppe ein signifikant niedrigeres Verhältnis der GP-Dichtungsmittel-Schnittstelle (Kontakt) als die EndoSequence BC, und diese Unterschiede können durch einige methodologische Unterschiede erklärt werden, die mit der Morphologie des Wurzelkanals (die runder war), der Methode der Anwendung des Dichtungsmittels (die 'butterte' Kegeltechnik), die Materialien mit niedriger Viskosität wie CSS begünstigt, zusammenhängen. Darüber hinaus führten zwei erfahrene Operatoren die Segmentierungsverfahren und alle Analysen separat durch, um die Gesamtqualität der Analyse in der vorliegenden Studie zu verbessern, und das endgültige Ergebnis wurde durch eine Vereinbarung zwischen ihnen erreicht. Es wurde auch besondere Sorgfalt darauf verwendet, die Vergleichbarkeit zwischen den experimentellen Gruppen sicherzustellen, indem der anatomische Faktor ausgeglichen wurde. Gut ausgewogene experimentelle Gruppen wurden durch die Auswahl anatomisch passender Wurzelkanäle gemäß AR, Volumen und 3D-Kanalgeometrie nach dem Scannen von 237 mandibularen Schneidezähnen erstellt (De-Deus et al., 2020). Dieser Ansatz ermöglicht eine bessere Kontrolle des Störeffekts, den anatomische Variationen in der Morphologie des Wurzelkanals auf die Ergebnisse laborbasierter Studien haben können. Da die Minimierung von Lücken in den GP-Dichtungsmittel- und Dentin-Dichtungsmittel-Schnittstellen klinisch relevant ist, um das Eindringen von Bakterien und/oder deren Abbauprodukten zu verhindern (Yücel & Çiftçi, 2006), sollten die vorliegenden Ergebnisse die Entwicklung weiterer Studien zur Validierung der Füllfähigkeit der Einzelkegeltechnik mit CSS nicht nur in verschiedenen Kanal-Morphologien, sondern auch in Zähnen, die mit minimalinvasiven Ansätzen vorbereitet wurden, fördern.
Schlussfolgerungen
Im Rahmen des experimentellen Rahmens der aktuellen Studie kann festgestellt werden, dass AH Plus eine bessere Anpassungsqualität an der GP-Dichtungsoberfläche im Vergleich zum EndoSequence BC Sealer zeigte. Keines der Proben zeigte eine lückenlose Schnittstelle.
Autoren: Gustavo De-Deus, Gustavo O. Santos, Iara Zamboni Monteiro, Daniele M. Cavalcante, Marco Simões-Carvalho, Felipe G. Belladonna, Emmanuel J. N. L. Silva, Erick M. Souza, Raphael Licha, Carla Zogheib, Marco A. Versiani
Referenzen
- Barborka, B.J., Woodmansey, K.F., Glickman, G.N., Schneiderman, E. & He, J. (2017) Langfristige klinische Ergebnisse von Zähnen, die mit Resilon gefüllt wurden. Journal of Endodontics, 43, 556–560.
- Candeiro, G.T., Correia, F.C., Duarte, M.A., Ribeiro-Siqueira, D.C. & Gavini, G. (2012) Bewertung der Radiopazität, pH, Freisetzung von Calciumionen und Fluss eines biokeramischen Wurzelkanaldichtungsmittels. Journal of Endodontics, 38, 842–845.
- Daculsi, G., Passuti, N., Martin, S., Deudon, C., Legeros, R.Z. & Raher, S. (1990) Makroporöse Calciumphosphatkeramik für die Langknochenchirurgie bei Menschen und Hunden. Klinische und histologische Studie. Journal of Biomedical Materials Research, 24, 379–396.
- De-Deus, G., Di Giorgi, K., Fidel, S., Fidel, R.A. & Paciornik, S. (2009) Push-out-Bondstärke von Resilon/Epiphany und Resilon/Epiphany Selbstätzend zu Wurzel-Dentin. Journal of Endodontics, 35, 1048–1050.
- De-Deus, G., Reis, C., Di Giorgi, K., Brandão, M.C., Audi, C. & Fidel, R.A. (2011) Interfaciale Anpassung des Epiphany selbsthaftenden Dichtungsmittels an Wurzel-Dentin. Oral Surgery Oral Medicine Oral Pathology Oral Radiology and Endodontics, 11, 381–386.
- De-Deus, G., Simões-Carvalho, M., Belladonna, F.G., Versiani, M.A., Silva, E.J.N.L., Cavalcante, D.M. et al. (2020) Erstellung gut ausgewogener experimenteller Gruppen für vergleichende endodontische Laborstudien: ein neuer Vorschlag basierend auf Mikro-CT und in silico Methoden. International Endodontic Journal, 53, 974–985.
- Demirkiran, H. (2012) Biokeramiken für Osteogenese, molekulare und zelluläre Fortschritte. In: Jandial, R. & Chen, M.Y. (Hrsg.) Regenerative Biologie der Wirbelsäule und des Rückenmarks. Fortschritte in der experimentellen Medizin und Biologie. New York, NY: Springer, S. 760.
- Eltair, M., Pitchika, V., Hickel, R., Kühnisch, J. & Diegritz, C. (2018) Bewertung der Schnittstelle zwischen Guttapercha und zwei Arten von Dichtungsmitteln mittels Rasterelektronenmikroskopie (REM). Klinische Munduntersuchungen, 22, 1631–1639.
- Elyassi, Y., Moinzadeh, A.T. & Kleverlaan, C.J. (2019) Charakterisierung von Leachaten aus 6 Wurzelkanaldichtungsmitteln. Journal of Endodontics, 45, 623–627.
- Eymirli, A., Sungur, D.D., Uyanik, O., Purali, N., Nagas, E. & Cehreli, Z.C. (2019) Eindringen in Dentinkanälchen und Rückführbarkeit eines auf Calcium-Silikat basierenden Dichtungsmittels, das in Bulk oder mit unterschiedlichen Hauptkernmaterialien getestet wurde. Journal of Endodontics, 45, 1036–1040.
- Friedman, C.E., Sandrik, J.L., Heuer, M.A. & Rapp, G.W. (1977) Zusammensetzung und physikalische Eigenschaften von Guttapercha-Endodontiefüllmaterialien. Journal of Endodontics, 3, 304–308.
- Gandolfi, M.G., Parrilli, A.P., Fini, M., Prati, C. & Dummer, P.M. (2013) 3D-Mikro-CT-Analyse der Schnittstellenlücken, die mit Thermafil-Wurzelfüllungen verwendet werden, die mit AH Plus oder einem fließfähigen MTA-Dichtungsmittel verwendet werden. International Endodontic Journal, 46, 253–263.
- Guivarc’h, M., Jeanneau, C., Giraud, T., Pommel, L., About, I., Azim, A.A. et al. (2020) Eine internationale Umfrage zur Verwendung von auf Calcium-Silikat basierenden Dichtungsmitteln in der nicht-chirurgischen endodontischen Behandlung. Klinische Munduntersuchungen, 1, 417–424.
- Hegde, V. & Arora, S. (2015) Dichtungsfähigkeit eines neuartigen hydrophilen vs. herkömmlichen hydrophoben Füllsystems: eine bakterielle Leckage-Studie. Journal of Conservative Dentistry, 18, 62–65.
- Hess, D., Solomon, E., Spears, R. & He, J. (2011) Rückführbarkeit eines biokeramischen Wurzelkanaldichtungsmaterials. Journal of Endodontics, 37, 1547–1549.
- Hiraishi, N., Sadek, F.T., King, N.M., Ferrari, M., Pashley, D.H. & Tay, F.R. (2008) Anfälligkeit eines auf Polycaprolacton basierenden Wurzelkanalfüllmaterials gegenüber Abbau unter Verwendung eines Agar-Well-Diffusionstests. American Journal of Dentistry, 21, 119–123.
- Hiraishi, N., Yau, J.Y.Y., Loushine, R.J., Armstrong, S.R., Weller, R.N., King, N.M. et al. (2007) Anfälligkeit eines auf Polycaprolacton basierenden Wurzelkanalfüllmaterials gegenüber Abbau. III. turbidimetrische Bewertung der enzymatischen Hydrolyse. Journal of Endodontics, 33, 952–956.
- ISO. (2012) Internationale Norm ISO 6876:2012: zahnärztliche Wurzelkanaldichtungsmittel. Genf: Schweiz.
- Ketcham, R.A. & Carlson, W.D. (2001) Erwerb, Optimierung und Interpretation von Röntgen-Computertomografie-Bildern: Anwendungen in den Geowissenschaften. Computer und Geowissenschaften, 27, 381–400.
- Kim, J.A., Hwang, Y.C., Rosa, V., Yu, M.K., Lee, K.W. & Min, K.S. (2018) Qualität der Wurzelkanalfüllung eines vorgefertigten Calcium-Silikat-Endodontie-Dichtungsmittels, das unter Verwendung von Guttapercha-Kegel-vermittelter Ultraschallaktivierung aufgetragen wurde. Journal of Endodontics, 44, 133–138.
- Kim, S., Kim, S., Park, J.W., Jung, I.Y. & Shin, S.J. (2017) Vergleich des Anteils an Lücken in der Kanalfüllung eines auf Calcium-Silikat basierenden Dichtungsmittels und Guttapercha-Kegeln unter Verwendung von zwei Fülltechniken. Materialien, 12(10), 1170.
- Le Ferrand, H. & Bacha, A. (2021) Entdeckung und Wiederentdeckung von Guttapercha, einem natürlichen Thermoplasten. MRS Bulletin, 46, 84–85.
- Lee, J.K., Kwak, S.W., Ha, J.H., Lee, W.C. & Kim, H.C. (2017) Physikochemische Eigenschaften von auf Epoxidharz- und biokeramischen basierenden Wurzelkanaldichtungsmitteln. Bioanorganische Chemie und Anwendungen, 2017, 1–8.
- LeGeros, R.Z. (1988) Calciumphosphatmaterialien in der restaurativen Zahnheilkunde: eine Übersicht. Advances in Dental Research, 2, 164–180.
- Moinzadeh, A.T., Zerbst, W., Boutsioukis, C., Shemesh, H. & Zaslansky, P. (2015) Porositätsverteilung in Wurzelkanälen, die mit Guttapercha und Calcium-Silikat-Zement gefüllt sind. Dental Materials, 31, 1100–1108.
- Moorer, W.R. & Genet, J.M. (1982) Antibakterielle Aktivität von Guttapercha-Kegeln, die dem Zinkoxidbestandteil zugeschrieben wird. Oral Surgery, Oral Medicine und Oral Pathology, 53, 508–517.
- Nagendrababu, V., Murray, P.E., Ordinola-Zapata, R., Peters, O.A., Rôças, I.N., Siqueira, J.F. Jr. et al. (2021) PRILE 2021 Richtlinien für die Berichterstattung über Laborstudien in der Endodontologie: Erklärung und Ausarbeitung. International Endodontic Journal, 54, 1491–1515.
- Neelakantan, P., Nandagopal, M., Shemesh, H. & Wesselink, P. (2015) Der Einfluss von Wurzel-Dentin-Bedingungsprotokollen auf die Push-out-Bondstärke von drei Calcium-Silikat-Dichtungsmitteln. International Journal of Adhesion and Adhesives, 60, 104–108.
- Oliveira, D.S., Cardoso, M.L., Queiroz, T.F., Silva, E.J., Souza, E.M. & De-Deus, G. (2016) Suboptimale Push-out-Bondstärken von auf Calcium-Silikat basierenden Dichtungsmitteln. International Endodontic Journal, 49, 796–801.
- Pedullà, E., Abiad, R.S., Conte, G., La Rosa, G.R.M., Rapisarda, E. & Neelakantan, P. (2020) Wurzelfüllungen mit einem abgestimmten Einzelkegel und zwei auf Calcium-Silikat basierenden Dichtungsmitteln: eine Analyse von Lücken mittels Mikro-Computertomographie. Klinische Munduntersuchungen, 24, 4487–4492.
- Pinto, J.C., Torres, F.F.E., Lucas-Oliveira, E., Bonagamba, T.J., Guerreiro-Tanomaru, J.M. & Tanomaru-Filho, M. (2021) Bewertung von gekrümmten Wurzelkanälen, die mit einem neuen biokeramischen Dichtungsmittel gefüllt sind: eine mikrocomputertomographische Studie unter Verwendung von Bildern mit unterschiedlichen Voxelgrößen und Segmentierungsmethoden. Mikroskopieforschung und Technik, 84, 2960–2967.
- Sagsen, B., Ustun, Y., Demirbuga, S. & Pala, K. (2011) Push-out-Bondstärke von zwei neuen auf Calcium-Silikat basierenden endodontischen Dichtungsmitteln zu Wurzelkanaldentin. International Endodontic Journal, 44, 1088–1091.
- Shipper, G., Ørstavik, D., Teixeira, F.B. & Trope, M. (2004) Eine Bewertung der mikrobiellen Leckage in Wurzeln, die mit einem thermoplastischen synthetischen Polymer-basierten Wurzelkanalfüllmaterial (Resilon) gefüllt sind. Journal of Endodontics, 30, 342–347.
- Shipper, G., Teixeira, F.B., Arnold, R.R. & Trope, M. (2005) Periapikale Entzündung nach koronaler mikrobieller Inokulation von Hundewurzeln, die mit Guttapercha oder Resilon gefüllt sind. Journal of Endodontics, 31, 91–96.
- Silva, E.J.N.L., Canabarro, A., Andrade, M.R.T.C., Cavalcante, D.M., Von Stetten, O., Fidalgo, T.K.D.S. et al. (2019) Widerstand gegen Ablösung von biokeramischen und Epoxid-Dichtungsmitteln: eine systematische Überprüfung und Metaanalyse. Journal of Evidence-Based Dental Practice, 19, 221–235.
- Silva, E.J.N.L., Ehrhardt, I.C., Sampaio, G.C., Cardoso, M.L., Oliveira, D.D.S., Uzeda, M.J. et al. (2021) Bestimmung des Setzens von Wurzelkanaldichtungsmitteln unter Verwendung eines in vivo Tierexperimentellen Modells. Klinische Munduntersuchungen, 25, 1899–1906.
- Silva, E.J., Rosa, T.P., Herrera, D.R., Jacinto, R.C., Gomes, B.P. & Zaia, A.A. (2013) Bewertung der Zytotoxizität und physikochemischen Eigenschaften des auf Calcium-Silikat basierenden endodontischen Dichtungsmittels MTA Fillapex. Journal of Endodontics, 39, 274–277.
- Silva, E.J.N.L., Zaia, A.A. & Peters, O.A. (2017) Zytokompatibilität von auf Calcium-Silikat basierenden Dichtungsmitteln in einem dreidimensionalen Zellkulturmodell. Klinische Munduntersuchungen, 21, 1531–1536.
- Silva-Almeida, L.H., Moraes, R.R., Morgental, R.D. & Pappen, F.G. (2017) Sind vorgefertigte auf Calcium-Silikat basierende endodontische Dichtungsmittel mit herkömmlichen Materialien vergleichbar? Eine systematische Überprüfung von In-vitro-Studien. Journal of Endodontics, 43, 527–535.
- Strange, K.A., Tawil, P.Z., Phillips, C., Walia, H.D. & Fouad, A.F. (2019) Langfristige Ergebnisse der endodontischen Behandlung mit Resilon/Epiphany. Journal of Endodontics, 45, 507–512.
- Sun, J., Eidelman, N. & Lin-Gibson, S. (2009) 3D-Kartierung der Polymerisationsschrumpfung mittels Röntgen-Mikro-Computertomographie zur Vorhersage von Mikroleckagen. Dental Materials, 25, 314–320.
- Tanomaru-Filho, M., Torres, F.F.E., Chavez-Andrade, G.M., de Almeida, M., Navarro, L.G., Steier, L. et al. (2017) Physikochemische Eigenschaften und volumetrische Veränderungen von Silikon/bioaktivem Glas und auf Calcium-Silikat basierenden endodontischen Dichtungsmitteln. Journal of Endodontics, 43, 2097–2101.
- Tay, F.R., Loushine, R.J., Lambrechts, P., Weller, R.N. & Pashley, D.H. (2005a) Geometrische Faktoren, die die Dentinbindung in Wurzelkanälen beeinflussen: ein theoretischer Modellierungsansatz. Journal of Endodontics, 31, 584–589.
- Tay, F., Pashley, D., Williams, M., Raina, R., Loushine, R., Weller,
- R. et al. (2005b) Anfälligkeit eines auf Polycaprolacton basierenden Wurzelkanalfüllmaterials gegenüber Abbau. I. Alkalische Hydrolyse. Journal of Endodontics, 31, 593–598.
- Tay, F.R., Pashley, D.H., Yiu, C.K.Y., Yau, J.Y.Y., Yiu-fai, M., Loushine, R.J. et al. (2005c) Anfälligkeit eines auf Polycaprolacton basierenden Wurzelkanalfüllmaterials gegenüber Abbau. II. Gravimetrische Bewertung der enzymatischen Hydrolyse. Journal of Endodontics, 31, 737–741.
- Tay, F.R. & Pashley, D.H. (2007) Monoblöcke in Wurzelkanälen: ein hypothetisches oder ein greifbares Ziel. Journal of Endodontics, 33, 391–398.
- Tay, F.R., Pashley, D.H., Loushine, R.J., Kuttler, S., García-Godoy, F., King, N.M. et al. (2007) Anfälligkeit eines auf Polycaprolacton basierenden Wurzelkanalfüllmaterials gegenüber Abbau. Hinweise auf Biodegradation aus einem simulierten Feldtest. American Journal of Dentistry, 20, 365–369.
- Teixeira, F.B., Teixeira, E.C., Thompson, J.Y. & Trope, M. (2004) Bruchfestigkeit von endodontisch behandelten Wurzeln mit einem neuen Harzfüllmaterial. Journal of the American Dental Association, 135, 646–652.
- Torres, F.F.E., Zordan-Bronzel, C.L., Guerreiro-Tanomaru, J.M., Chavez-Andrade, G.M., Pinto, J.C. & Tanomaru-Filho, M. (2020) Einfluss der Eintauchung in destilliertes Wasser oder phosphate-gepufferte Salzlösung auf die Löslichkeit, volumetrische Veränderung und das Vorhandensein von Lücken in neuen auf Calcium-Silikat basierenden Wurzelkanaldichtungsmitteln. International Endodontic Journal, 53, 385–391.
- Viapiana, R., Moinzadeh, A.T., Camilleri, L., Wesselink, P.R., Tanomaru Filho, M. & Camilleri, J. (2016) Porosität und Dichtungsfähigkeit von Wurzelfüllungen mit Guttapercha und BioRoot RCS oder AH Plus Dichtungsmitteln. Bewertung durch drei ex vivo Methoden. International Endodontic Journal, 49, 774–782.
- Wilson, A.D., Clinton, D.J. & Miller, R.P. (1973) Zinkoxid-Eugenol-Zemente: IV. Mikrostruktur und Hydrolyse. Journal of Dental Research, 52, 253–260.
- Wolfmeier, U., Schmidt, H., Heinrichs, F.L., Michalczyk, G., Payer, W., Dietsche, W. et al. (2002) Wachse. In: Ullmanns Enzyklopädie der industriellen Chemie. Bd. 39. Weinheim: Wiley:112–172.
- Yanpiset, K., Banomyong, D., Chotvorrarak, K. & Srisatjaluk, R.L. (2018) Bakterielle Leckage und mikrocomputertomographische Bewertung in rund geformten Kanälen, die mit biokeramischen Kegeln und Dichtungsmitteln unter Verwendung der abgestimmten Einzelkegeltechnik gefüllt sind. Restaurative Zahnheilkunde & Endodontie, 43, e30.
- Yücel, A.C. & Çiftçi, A. (2006) Auswirkungen verschiedener Wurzelkanalfülltechniken auf das Eindringen von Bakterien. Oral Surgery Oral Medicine Oral Pathology Oral Radiology and Endodontics, 102, e88–e92.
- Zare, S., Shen, I., Zhu, Q., Ahn, C., Primus, C. & Komabayashi, T. (2021) Mikrocomputertomographische Bewertung der Einzelkegelfüllung mit drei Dichtungsmitteln. Restaurative Zahnheilkunde & Endodontie, 46, e25.
- Zeiger, D.N., Sun, J., Schumacher, G.E. & Lin-Gibson, S. (2009) Bewertung der Schrumpfung und Leckage von zahnärztlichen Kompositen in extrahierten Zähnen unter Verwendung von Röntgen-Mikrocomputertomographie. Dental Materials, 25, 1213–1220.
- Zhang, W., Li, Z. & Peng, B. (2010) Auswirkungen von iRoot SP auf die Expression von mineralisierungsbezogenen Genen in MG63-Zellen. Journal of Endodontics, 36, 1978–1982.
- Zordan-Bronzel, C.L., Esteves Torres, F.F., Tanomaru-Filho, M., Chavez-Andrade, G.M., Bosso-Martelo, R. & Guerreiro-Tanomaru, J.M. (2019) Bewertung der physikochemischen Eigenschaften eines neuen auf Calcium-Silikat basierenden Dichtungsmittels, Bio-C Dichtungsmittel. Journal of Endodontics, 45, 1248–1252.
