Bewertung der physikochemischen Eigenschaften von vier Wurzelkanalversiegelungen
Maschinenübersetzung
Der Originalartikel ist in EN Sprache (Link zum Lesen) geschrieben.
Zusammenfassung
Ziel: Die physikochemischen Eigenschaften und die Oberflächenmorphologie von AH Plus, GuttaFlow, RoekoSeal und Activ GP Wurzelkanalfüllmaterialien zu bewerten.
Methodik: Fünf Proben jedes Materials wurden hinsichtlich der Aushärtezeit, dimensionalen Veränderung, Löslichkeit und Radiopazitätstests gemäß ANSI/ADA Spezifikation 57 bewertet. Insgesamt wurden 50 mL deionisiertes destilliertes Wasser aus den Löslichkeitstests verwendet, um die Metalllöslichkeit mittels Atomabsorptionsspektrometrie zu messen. Die Morphologien der äußeren Oberfläche und des Querschnitts der Proben wurden mittels Rasterelektronenmikroskop (REM) analysiert. Die statistische Analyse wurde unter Verwendung von einseitiger ANOVA und post hoc Tukey–Kramer-Tests mit der Nullhypothese auf 5% festgelegt.
Ergebnisse: AH Plus hatte die längste Aushärtezeit (580,6 ± 3,05 min) (P< 0,05). Activ GP hatte keinen Mittelwert bei den Radiopazitäts- und Löslichkeitstests (1,31 ± 0,35 mm und 11,8 ± 0,43%, respektive) gemäß ANSI/ADA und unterschied sich signifikant von den anderen Materialien (P< 0,05), die Mittelwerte für diese Tests gemäß den Anforderungen der ADA aufwiesen. GuttaFlow war das einzige Füllmaterial, das der Spezifikation 57 hinsichtlich des Tests zur dimensionalen Veränderung entsprach (0,44 ± 0,16%) (P< 0,05). Der spektrometrische Test zeigte eine signifikante Freisetzung von Ca2+, K+, Zn2+ Ionen aus dem Activ GP Füllmaterial (32,57 ± 5,0, 1,57 ± 0,22 und 8,20 ± 1,74 μg mL–1, respektive). In der REM-Analyse war der Verlust der Matrix offensichtlich und die Füllpartikel waren in allen Gruppen deutlicher erkennbar.
Fazit: Die Aushärtungszeit aller Dichtstoffe entsprach den Anforderungen der ANSI/ADA. Activ GP erfüllte nicht die Protokolle der ANSI/ADA hinsichtlich Radiopazität, dimensionaler Veränderung und Löslichkeit. Gutta-Flow war der einzige Dichtstoff, der in allen Tests der Spezifikation 57 entsprach. Die SEM-Analyse zeigte, dass die Oberflächen aller Dichtstoffe nach dem Löslichkeitstest mikromorphologische Veränderungen aufwiesen.
Einleitung
Bei der Wurzelkanalbehandlung ist das vollständige Abdichten des Wurzelkanalsystems nach der Reinigung und Formgebung entscheidend, um zu verhindern, dass orale Pathogene kolonisieren und die Wurzel- und periapikalen Gewebe erneut infizieren. Obwohl Guttapercha immer noch das am häufigsten verwendete Wurzelkanalfüllmaterial ist, wurden eine Reihe neuer Techniken und Materialien mit unterschiedlichen physikochemischen Eigenschaften entwickelt (Ørstavik 2005, Versiani et al. 2006, Resende et al. 2009).
Während der Wurzelkanalfüllung erfüllt der endodontische Dichtstoff mehrere Funktionen, einschließlich der Füllung von Unregelmäßigkeiten der Wurzelkanalwände wie apikalen Verzweigungen und Deltas sowie von Räumen, in denen Guttapercha sich nicht anpassen konnte (Kontakiotis et al. 2007). Da die herkömmlichen Füllmaterialien den Wurzelkanalraum nicht effektiv abdichten, wurden neue endodontische Dichtstoffe entwickelt (Bouillaguet et al. 2008).
Obwohl AH Plus eine angemessene langfristige dimensionsstabilität aufweist, bleibt seine Dichtungsfähigkeit umstritten, partly weil AH Plus nicht an Guttapercha bindet (Ørstavik et al. 2001). RoekoSeal Automix (Coltène Whaledent, Langenau, Deutschland) ist ein Dichtungsmittel, das Dimethylpolysiloxan enthält, wobei nur begrenzte Daten zu seinen physikochemischen Eigenschaften vorliegen (Gençoglu et al. 2003). Trotz der vielversprechenden klinischen und laboratorischen Daten, die für das silikonbasierte Dichtungsmittel berichtet wurden, wurde RoekoSeal in verschiedenen Studien mit widersprüchlichen Ergebnissen getestet (De-Deus et al. 2007). GuttaFlow (Coltène Whaledent, Alstätten, Schweiz) ist ein auf Polyvinylsiloxan basierendes Dichtungsmittel und wurde mit der Absicht eingeführt, die Nachteile der warmen Guttapercha-Techniken zu reduzieren (Eldeniz & Ørstavik 2009). Es wurde behauptet, dass GuttaFlow die Dichtung verbessern könnte, weil es eine erhöhte Fließfähigkeit aufweist und das Material sich beim Aushärten leicht ausdehnt (Bouillaguet et al. 2008, Eldeniz & Ørstavik 2009, Roggendorf et al. 2010).
Die zahnmedizinischen Anwendungen von Glas-Ionomer-Dichtstoffen nutzen ihre Bindung an Dentin, die Fluoridfreisetzung, die antimikrobielle Aktivität und die Biokompatibilität (Ørstavik 2005). Einige Labortests haben jedoch eine Neigung zu Undichtigkeiten und Zersetzung angezeigt (Carvalho-Júnior et al. 2003, Schäfer & Zandbiglari 2003). Kürzlich wurde das Activ GP Precision Obturation System (Brasseler USA, Savannah, GA, USA) als ein Monoblock-System für Wurzelfüllungen vermarktet, das konventionelle Guttapercha-Kegel verwendet, die mit Glas-Ionomer-Füllstoffen beschichtet sind (Roggendorf et al. 2010). Der Hersteller behauptet, dass das Produkt in Bezug auf Handhabungseigenschaften, Arbeitszeit, Radiopazität (Fransen et al. 2008) und Dichtheit überlegen ist, aufgrund der erhöhten Fließfähigkeit und der Tatsache, dass das Material beim Aushärten leicht expandiert (Kontakiotis et al. 2007).
Obwohl verschiedene Arten von endodontischen Dichtstoffen als innovative Füllmaterialien vorgeschlagen wurden, wurde der ideale Wurzelkanaldichtstoff noch nicht gefunden (Ørstavik 1983, 2005, Ørstavik et al. 2001, Versiani et al. 2006, Resende et al. 2009). Daher war das Ziel dieser Laborstudie, die Aushärtezeit, Radiopazität, dimensionsänderung und Löslichkeit von silikonbasierten Dichtstoffen (GuttaFlow und RoekoSeal) und einem ionomerbasierten Dichtstoff (Activ GP) mit einem gut etablierten epoxidharzbasierten Dichtstoff (AH Plus) gemäß den ANSI/ADA (2000) Standards zu vergleichen.
Materialien und Methoden
Die Aushärtezeit, Radiopazität, dimensionsale Veränderungen und Löslichkeit nach dem Aushärten für AH Plus (Gruppe I), GuttaFlow (Gruppe II), RoekoSeal (Gruppe III) und Activ GP (Gruppe IV) Wurzelkanalversiegelungen wurden gemäß den ANSI/ADA (2000) Standards für Wurzelkanalversiegelungsmaterialien gemessen. Die getesteten Materialien (Tabelle 1) wurden gemäß den Anweisungen des Herstellers verarbeitet. Die Analysen wurden von einem einzelnen Prüfer durchgeführt, der blind gegenüber den experimentellen Materialien war. Um die Menge des Materials zu standardisieren und zu homogenisieren, wurden 0,3 g Versiegelung auf eine Mischplatte gegeben und für 15 s für jede getestete Probe spatuliert. Für die physikochemischen Tests wurde der arithmetische Mittelwert von fünf Wiederholungen für jede Versiegelung aufgezeichnet und als Ergebnis des Tests betrachtet.
Einstellzeit
Fünf Gipsabdruckringe aus Paris mit einem Innendurchmesser von 10 mm und einer Dicke von 2 mm wurden vorbereitet. Die äußeren Ränder der Formen wurden mit Wachs auf einer Glasplatte (75 x 25 x 1 mm) fixiert. Die Formen wurden dann mit dem Material gefüllt und in eine Kammer mit 95% relativer Luftfeuchtigkeit (RH) und einer Temperatur von 37 °C übertragen. Nach 150 ± 10 s nach Beginn des Mischens des Dichtungsmittels wurde eine Gilmore-Nadel mit einer Masse von 100 ± 0,5 g, die an einem flachen Ende von 2,0 ± 0,1 mm Durchmesser hatte, vorsichtig senkrecht auf die horizontale Oberfläche jeder Probe abgesenkt. Die Nadelspitze wurde gereinigt und das Abtasten wurde wiederholt, bis die Eindrücke nicht mehr sichtbar waren. Wenn die Ergebnisse um mehr als ±5% abwichen, wurde der Test wiederholt.
Radiopazitätstest
Fünf Acrylplatten (2,2 cm x 4,5 cm x 1 mm), die vier Vertiefungen mit einer Tiefe von 1 mm und einem Durchmesser von 5 mm enthielten, wurden vorbereitet und über eine Glasplatte gelegt, die mit einer Zellophanfolie bedeckt war. Jede Vertiefung wurde mit einem der Dichtungsmittel gefüllt, wobei eine Reihenfolge entsprechend der Einstellzeit des Materials eingehalten wurde, von der längsten bis zur kürzesten, sodass die Proben nach der endgültigen Einstellung aller Materialien für die radiografische Bewertung bereit waren. Um die Bildung von Blasen zu vermeiden, wurde das frisch gemischte Dichtungsmittel mit einer Spritze in die Vertiefungen eingeführt. Eine weitere Glasplatte, die mit Zellophan bedeckt war, wurde oben aufgelegt, bis die vollständige Einstellung erreicht war, und überschüssiges Dichtungsmittel wurde entfernt. Jede Platte wurde in einem Inkubator (37 °C, 95% RH) für einen Zeitraum aufbewahrt, der dem Dreifachen der Einstellzeit entsprach.
Jede der Acrylplatten, die die Dichtstoffe enthielten, wurde zum Zeitpunkt der radiografischen Aufnahme neben einer anderen Acrylplatte (1,3 cm x 4,5 cm x 1 mm) positioniert, die einen Aluminium-Stufenkeil enthielt, der aus der Legierung 1100 gefertigt war, mit einer Dicke, die von 1 bis 10 mm variierte, in gleichmäßigen Schritten von jeweils 1 mm (Margraf Dental MFG Inc., Jenkintown, PA, USA). Dieses Set von Acrylplatten wurde vor dieser Phosphorplatte, neben dem Aluminium-Stufenkeil, platziert und eine digitale Radiographie wurde aufgenommen (Digora™-System; Soredex Orion Corporation, Helsinki, Finnland). Radiografische Bilder wurden mit dem Spectro 70X Röntgengerät (Dabi Atlante, Ribeirão Preto, SP, Brasilien) bei 70 kVp und 8 mA aufgenommen. Der Abstand vom Objekt zur Fokussierung betrug 30 cm und die Belichtungszeit betrug 0,2 s. Die belichteten Bildplatten der Testproben wurden unmittelbar nach der Belichtung gescannt (Digora™ Scanner) und mit der Software Digora™ für Windows 5.1 analysiert.
Dimensionale Veränderung
Fünf Teflon® (Polytetrafluorethylen, DuPont, HABIA, Knivsta, Schweden) Formen, die zur Herstellung von 3,58 mm hohen zylindrischen Testkörpern mit einem Durchmesser von 3 mm vorbereitet wurden, wurden auf eine Glasplatte gelegt, die mit einem feinen Zellophanblatt umwickelt war. Die Formen wurden mit einem leichten Überschuss an frisch gemischten Dichtstoffen gefüllt und ein Mikroskopobjektträger, ebenfalls in Zellophan eingewickelt, wurde auf die obere Fläche der Form gedrückt. Die zusammengebaute Gruppe wurde mit einer C-förmigen Klemme fest zusammengehalten und in einen Inkubator (37 °C, 95% RH) transferiert, wo sie für einen Zeitraum stehen gelassen wurde, der dem Dreifachen der Aushärtezeit entsprach. Nach diesem Zeitraum wurden die flachen Enden der Formen, die die Proben enthielten, mit 600er Schleifpapier nass geschliffen. Die Proben wurden aus der Form entfernt, mit einem digitalen Messschieber gemessen, in einem 50-mL-Gefäß mit 2,24 mL deionisiertem destilliertem Wasser aufbewahrt und für 30 Tage in einem Inkubator (37 °C, 95% RH) gelagert. Die Probe wurde dann aus dem Behälter entfernt, auf saugfähigem Papier trocken getupft und erneut auf Länge gemessen. Der Prozentsatz der dimensionalen Veränderungen wurde mit der Formel berechnet:
((L30 — L )/ L) x 100
wobei L30 die Länge der Probe nach 30 Tagen Lagerung und L die ursprüngliche Länge der Probe ist.
Löslichkeit
Eine 1,5 mm dicke zylindrische Teflon®-Form mit einem Innendurchmesser von 7,75 mm wurde mit frisch gemischtem Dichtmittel gefüllt. Die Form wurde von einer größeren Glasplatte gestützt und mit einer Cellophanfolie abgedeckt. Ein undurchlässiger Nylonfaden wurde in das Material eingelegt, und eine weitere Glasplatte, ebenfalls mit Cellophanfolie abgedeckt, wurde auf die Form positioniert und manuell so gedrückt, dass die Platten die gesamte Form gleichmäßig berührten. Die Anordnung wurde in einen Inkubator (37 °C, 95% RH) gestellt und für einen Zeitraum stehen gelassen, der dem Dreifachen der Aushärtezeit entspricht. Sobald die Proben aus der Form entfernt wurden, wurden sie dreimal gewogen (HM-200, A & D Engineering, Inc., Bradford, MA, USA), und der Mittelwert wurde aufgezeichnet. Die Proben wurden an einem Nylonfaden aufgehängt und paarweise in ein Kunststoffgefäß mit einer breiten Öffnung gelegt, das 7,5 mL deionisiertes destilliertes Wasser enthielt, wobei darauf geachtet wurde, jeglichen Kontakt zwischen ihnen und der Innenseite des Behälters zu vermeiden. Die Behälter wurden verschlossen und 7 Tage lang in einem Inkubator (37 °C, 95% RH) gelassen. Nach diesem Zeitraum wurden die Proben aus den Behältern entfernt, mit deionisiertem destilliertem Wasser gespült, mit saugfähigem Papier trocken getupft und für 24 Stunden in einen Luftentfeuchter gelegt. Danach wurden sie erneut gewogen. Der Gewichtsverlust jeder Probe (ursprüngliche Masse minus Endmasse), ausgedrückt als Prozentsatz der ursprünglichen Masse (m% = mi – mf), wurde als Löslichkeit des Dichtmittels betrachtet.
Ein Volumen von 7,5 mL destilliertem Wasser aus jeder Probe wurde in eine gereinigte und getrocknete Porzellanschale gegossen. Jede Schale wurde in einen Muffelofen gelegt und bei 550 °C verbrannt. Die Asche wurde in 10 mL konzentrierter Salpetersäure (Merck KGaA, Darmstadt, Deutschland) mit einem Glasstab gelöst. Anschließend wurden die Proben in 50 mL volumetrische Flaschen gegeben und das Volumen mit ultrapurem deionisiertem Wasser (MilliQ, Millipore, Billerica, MA, USA) aufgefüllt. Die erhaltenen Lösungen wurden in das Atomabsorptionsspektrometer (Perkin Elmer, Überlingen, Deutschland) gesprüht, um das Vorhandensein von Ca2+, K+, Zn2+ und Ag+ Ionen zu überprüfen. Der arithmetische Mittelwert von drei Wiederholungen für jedes Exemplar wurde aufgezeichnet und als Ergebnis betrachtet, ausgedrückt in μg mL–1.
Untersuchung mit Rasterelektronenmikroskopie
Für die Untersuchung mit Rasterelektronenmikroskopie (REM) wurden zylindrische Teflon® Formen (3 x 4 mm) mit frisch gemischten Dichtungsmitteln gefüllt. Die Formen wurden von einer Glasplatte unterstützt, die mit einer Zellophanfolie bedeckt war, und in eine Kammer (37 °C, 95% RH) für einen Zeitraum platziert, der dem Dreifachen der Aushärtezeit entsprach. Danach wurden die Proben mit einer Einweg-Skalpellklinge der Größe 15 geschnitten, auf einem metallischen Stub (10 x 5 mm) fixiert und mit Gold-Palladium (Bal-Tec AG, Balzers, Deutschland) bei 20 mA beschichtet. Die Morphologien der Außenfläche und des Querschnitts der Proben wurden qualitativ unter einem Feldemissions-REM (Jeol JSM 5410; Jeol Technic Co., Tokio, Japan) bei einer Beschleunigungsspannung von 15 kV, einem Arbeitsabstand von 6 bis 10 mm und bei unterschiedlichen Vergrößerungen analysiert.
Statistische Analyse
Fünf Proben aus jeder Gruppe wurden getestet und die Mittelwerte statistisch verglichen. Der Kolmogorov-Smirnov-Test zeigte, dass die Ergebnisse mit einer Normalverteilungskurve übereinstimmten, sodass eine parametrische statistische Analyse möglich war (Einweg-ANOVA und post hoc Tukey-Kramer-Test), und die Nullhypothese wurde auf 5% festgelegt (SPSS 17.0 für Windows; SPSS Inc., Chicago, IL, USA).
Ergebnisse
Einstellzeit
Die ANSI/ADA-Spezifikation (2000) verlangt, dass die Einstellzeit eines Dichtmittels innerhalb von 10% des von den Herstellern angegebenen Wertes liegt. Laut diesen beträgt die Einstellzeit von AH Plus, RSA RoekoSeal und Gutta-Flow 480, 50 und 30 Minuten. Im Gegensatz dazu gibt der Hersteller von Activ GP diese Informationen nicht an und erklärt nur, dass es mit einer verlängerten Arbeitszeit von 15 Minuten formuliert wurde.
Ein statistisch signifikanter Unterschied wurde zwischen den Gruppen AH Plus (580,6 ± 3,05 min), GuttaFlow (24,0 ± 2,0 min), RoekoSeal (40,0 ± 1,58 min) und Activ GP (15,2 ± 1,30 min) beobachtet (P< 0,05). Die Mittelwerte zeigten jedoch Übereinstimmung mit der ANSI/ADA-Standardisierung (Tabelle 2).
Radiopazitätstest
AH Plus (6.0 ± 0.12 mmAl), GuttaFlow (3.0 ± 0.04 mmAl) und RoekoSeal (4.17 ± 0.45 mmAl) hatten eine Radiopazität über den 3-mm Aluminium, wie von der ANSI/ADA-Spezifikation 57 empfohlen, während Activ GP (1.31 ± 0.35 mmAl) diese Anforderung nicht erfüllte. Die statistische Analyse zeigte einen Unterschied zwischen den experimentellen Gruppen (P < 0.05) (Tabelle 2).
Dimensionale Veränderung
Die ANSI/ADA-Standardisierung (2000) besagt, dass die mittlere lineare Schrumpfung des Dichtungsmittels 1% oder 0,1% bei der Expansion nicht überschreiten darf. Außer GuttaFlow (0,44 ± 0,16%) entsprach kein Dichtungsmittel der Spezifikation 57 (ANSI/ADA 2000). Alle Gruppen zeigten nach der Aushärtung eine Expansion, mit Ausnahme von RoekoSeal, das eine Schrumpfung beim Aushärten (-1,33 ± 0,12%) zeigte. Die statistische Analyse ergab einen signifikanten Unterschied zwischen den experimentellen Gruppen (P < 0,05) (Tabelle 2).
Löslichkeit
Die ANSI/ADA-Spezifikation 57 (2000) besagt, dass ein Wurzelkanaldichtungsmittel 3% nach Masse nicht überschreiten sollte, wenn die Löslichkeit des ausgehärteten Materials getestet wird. Außer Activ GP (11,8 ± 0,43%) entsprachen alle Dichtungsmittel der ANSI/ADA-Standardisierung (P < 0,05) (Tabelle 2). Das für den Löslichkeitstest verwendete deionisierte destillierte Wasser, das der atomaren Absorptionsspektrometrie unterzogen wurde, zeigte ein signifikantes Niveau an Ca2+, K+ und Zn2+ Ionenfreisetzung in der Activ GP-Gruppe im Vergleich zu AH Plus, Gutta-Flow und RoekoSeal (P < 0,05). Signifikante Mengen an Ag+ Freisetzung wurden in keiner Gruppe beobachtet (Tabelle 3).

SEM-Untersuchung
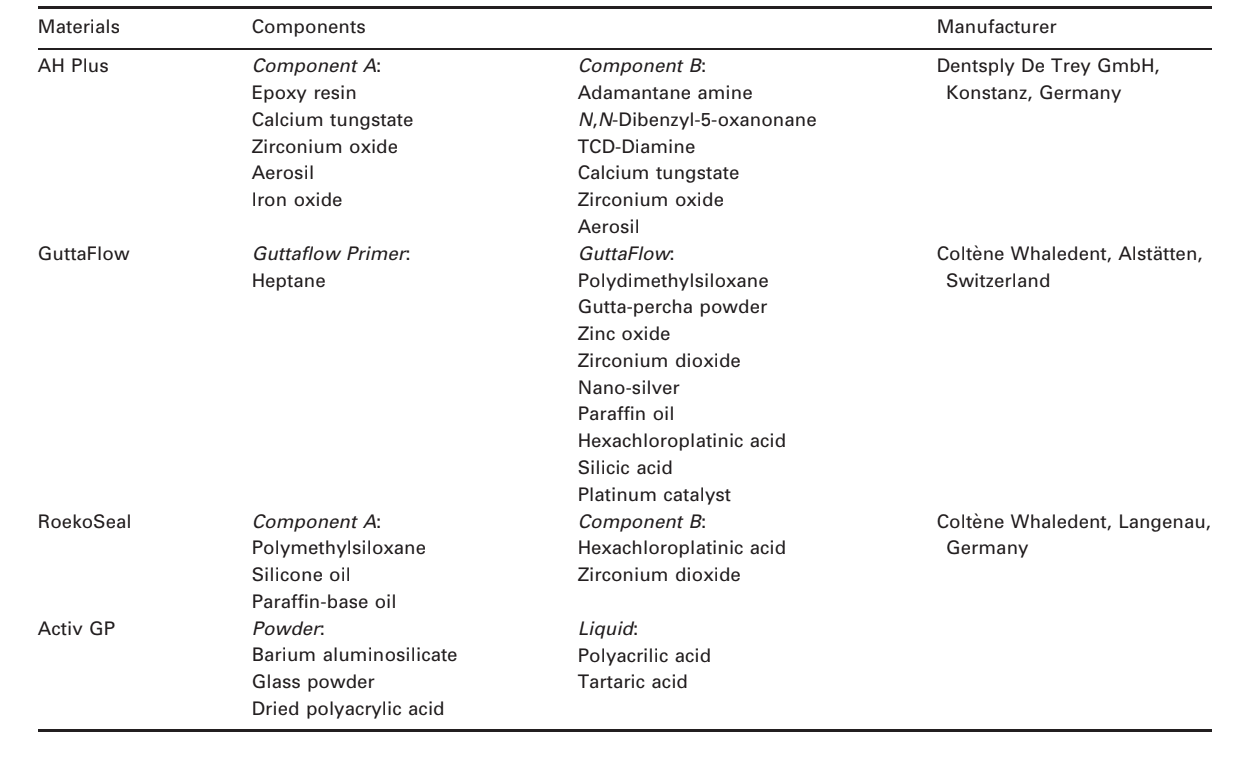
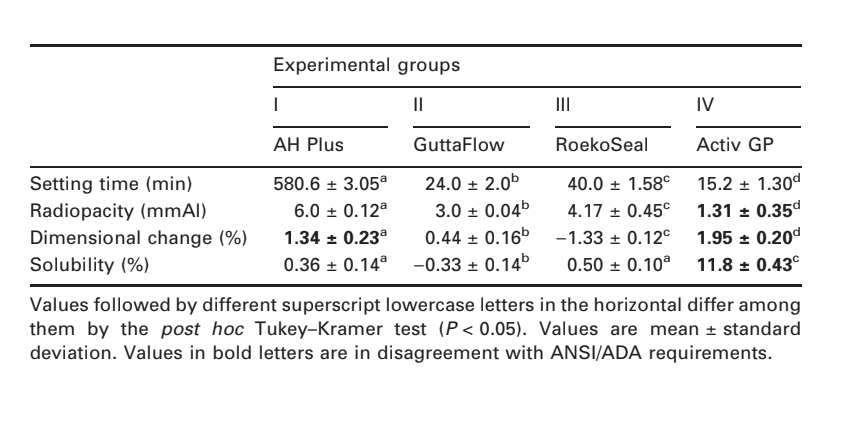
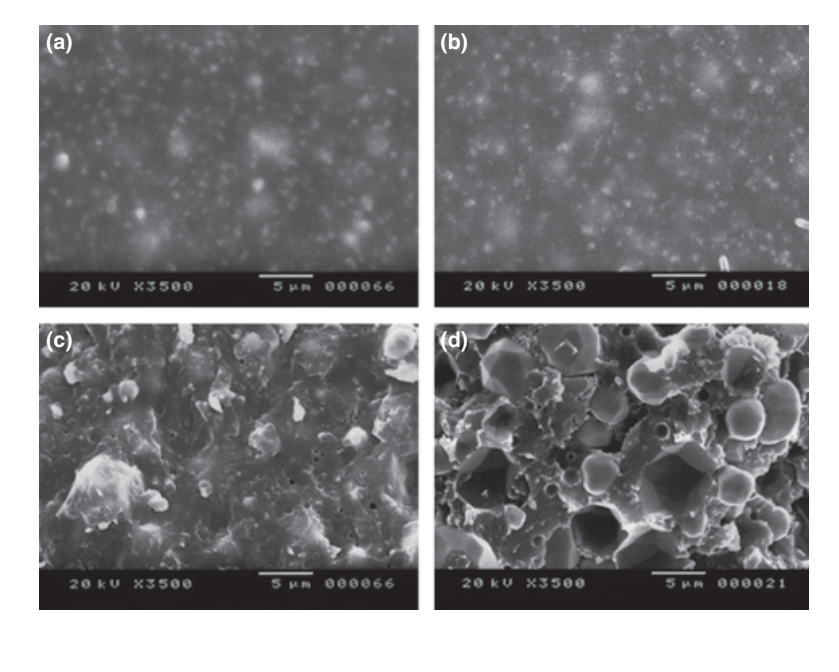
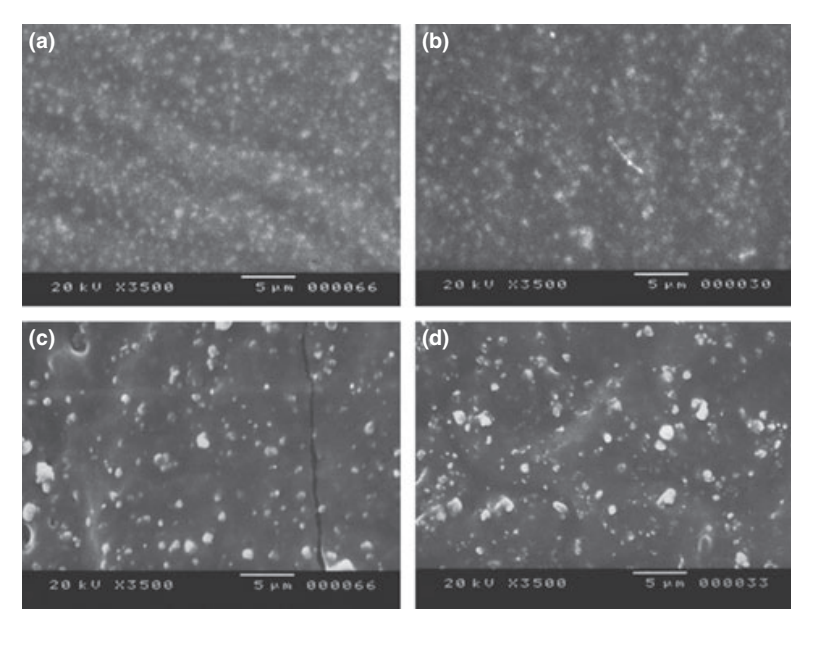
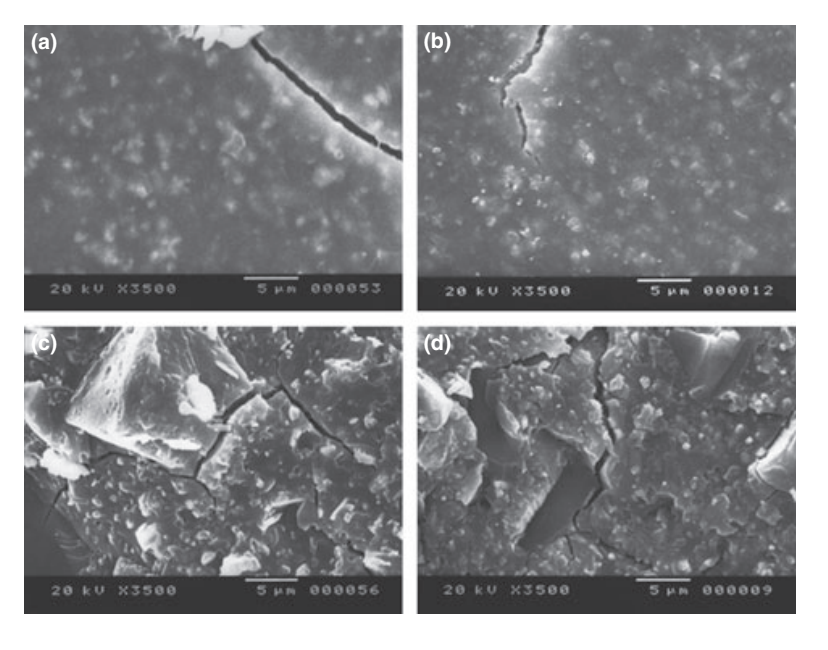
Ausgewählte Photomikrographien der polymerisierten Proben, die vor und nach der Wasserlagerung für 7 Tage erhalten wurden, sind in Abb. 1–4 dargestellt. Insgesamt wurde festgestellt, dass alle Oberflächen nach dem Löslichkeitstest mikromorphologische Veränderungen aufwiesen. Der Verlust der Matrix war offensichtlich und die Füllpartikel waren deutlicher erkennbar. Die Gruppen AH Plus (Abb. 1a,b), GuttaFlow (Abb. 2a,b) und RoekoSeal (Abb. 3a,b) hatten eine äußere Oberfläche, die überwiegend homogen rau erschien und nach dem Löslichkeitstest an Rauheit abnahm, gefolgt von einer anschließenden Rauheit der Oberfläche. Risse wurden in den Proben außer in der Gruppe Activ GP nicht beobachtet. Die Oberfläche der Activ GP-Proben war im Vergleich zu den anderen Gruppen relativ rauer und das Oberflächenmaterial schien nach dem Löslichkeitstest stärker beschädigt zu sein (Abb. 4a,b).
Die Rasterelektronenmikroskopie der Querschnittsoberfläche der Proben zeigte die Anwesenheit von kugelförmigen Polymeren unterschiedlicher Größen, die nicht homogen verteilt waren. Nach dem Löslichkeitstest erschien die innere Oberfläche der AH Plus (Abb. 1c,d), GuttaFlow (Abb. 2c,d) und Activ GP (Abb. 4c,d) Proben viel unregelmäßiger und rauer. Mehrere Mikrorisse wurden an den Füller-polymermatrix Schnittstellen in der Activ GP Gruppe vor und nach dem Löslichkeitstest (Abb. 4c,d) beobachtet. Auf der anderen Seite hatte die RoekoSeal Gruppe eine gleichmäßigere und kompaktere Schicht, die aus kugelförmigen Polymeren mit einer höheren Menge an Harzmatrix bestand (Abb. 3c,d).

Diskussion
Die Aushärtezeit ist in erster Linie ein Kontrolltest für das stabile Verhalten eines Produkts und hängt von den Bestandteilen, ihrer Partikelgröße, der Umgebungstemperatur und der relativen Luftfeuchtigkeit ab (Ørstavik 1983, 2005, Ørstavik et al. 2001). In der vorliegenden Studie waren alle Ergebnisse gemäß der ANSI/ADA-Spezifikation. Die längste Aushärtezeit von AH Plus könnte durch dieses Dichtungsmaterial erklärt werden, das ein zweikomponentiges Pastenmaterial ist, das auf einer langsamen Polymerisationsreaktion von Epoxidharz-Aminen mit hoher Molekulargewicht (Bisphenol A und Bisphenol F) basiert, wobei die Umwandlung von Monomeren in Polymere allmählich erfolgt (Lin-Gibson et al. 2006, Resende et al. 2009). Diese Ergebnisse stimmten mit früheren Forschungen überein (Versiani et al. 2006, Resende et al. 2009), jedoch berichteten Garrido et al. (2010) von einer Aushärtezeit von 13 h für AH Plus, was über der von der ADA zugelassenen 10%-Variation liegt.
Die ANSI/ADA (2000) Standards für die Radiodichte von Wurzelkanaldichtungsmaterialien wurden unter Verwendung konventioneller zahnärztlicher Filme bestimmt, bei denen die radiografischen Bilder durch chemische Verarbeitung erhalten werden (Taşdemir et al. 2008). Digitale Radiographie wird jedoch zunehmend häufiger in der Untersuchung von endodontischen Dichtungsmaterialien verwendet (Baksi Akdeniz et al. 2007, Carvalho-Júnior et al. 2007a, Rasimick et al. 2007, Taşdemir et al. 2008). In der vorliegenden Studie wurden digitale Bilder von Wurzelfüllmaterialien und Schritten eines Aluminiumstufenkeils mit einem Phosphorplattensystem sowie einem digitalen System zur Erfassung und Auswertung aufgenommen.
Eine Analyse der Zusammensetzung der getesteten Materialien ergab, dass alle radiopazifizierende Mittel enthalten (Tabelle 1), mit Ausnahme des Activ GP Dichtungsmittels. Laut Tanomaru-Filho et al. (2008) bietet die Anwesenheit von Barium-Aluminosilikat-Glas-Pulver in seiner Zusammensetzung keine zufriedenstellende Radiopazität. AH Plus enthält Zirkoniumoxid, Eisenoxid und Calciumtugstate als Radiopazifizierer (Tanomaru-Filho et al. 2007) und hatte den höchsten durchschnittlichen Radiopazitätswert (6,0 ± 0,12 mmAl), wie zuvor berichtet (Tagger & Katz 2003, Carvalho-Júnior et al. 2007a, Tanomaru-Filho et al. 2007, Taşdemir et al. 2008). Das RoekoSeal Dichtungsmittel enthält Zirkoniumdioxid als Radiopazifizierer (Baksi Akdeniz et al. 2007) und das vorliegende Ergebnis (4,17 ± 0,45 mmAl) stimmte mit früheren Ergebnissen überein, die eine Radiopazität von 4,0 bis 5,7 zeigten (Tagger & Katz 2003, Gambarini et al. 2006, Tanomaru-Filho et al. 2007, Rasimick et al. 2007). Die niedrigere Radiopazität von GuttaFlow (3,0 ± 0,04 mmAl) im Vergleich zu RoekoSeal wurde auch in früheren Studien beobachtet (Tagger & Katz 2003, Gambarini et al. 2006, Rasimick et al. 2007, Tanomaru-Filho et al. 2007). Da der Hersteller den chemischen Typ und die Konzentration von Nano-Silber in GuttaFlow nicht angibt, ist offensichtlich, dass diese Partikel keine radiopazifizierende Eigenschaft aufwiesen. Eine hohe Löslichkeit von Wurzelkanaldichtungsmitteln ist unerwünscht, da die Auflösung die Freisetzung von Materialien verursachen kann, die periapikale Gewebe reizen könnten, und auch Lücken zwischen Wurzelkanälen und Füllmaterialien ermöglichen kann, was wahrscheinlich die bakterielle Undichtigkeit im Laufe der Zeit erhöht (Donnelly et al. 2007). Trotz der Empfehlungen von ANSI/ADA wurde in der vorliegenden Studie eine zuvor vorgeschlagene Modifikation für beide Tests verwendet, die ähnliche Ergebnisse mit einer Verringerung des für die Herstellung der Testproben erforderlichen Materialvolumens erzielte (Carvalho-Júnior et al. 2007b). In der vorliegenden Studie dehnte sich AH Plus im Test zur dimensionalen Veränderung aus. Der langsame Massenzuwachs über die Zeit war hauptsächlich auf die Wechselwirkungsenergie zwischen Wasser und den Adsorptionsstellen des Systems (d.h. eine Hydroxylgruppe, eine Aminogruppe, das Ende der Polymerketten usw.) zurückzuführen, die die Lücken zwischen den Polymerketten füllten (McDermott 1993). Möglicherweise hat diese Expansion die Schrumpfung ausgeglichen, die das harzbasiertes Dichtungsmittel nach der Polymerisation erlitten hat (Phillips & Skinner 1991, Carvalho-Júnior et al. 2007b, Resende et al. 2009, Garrido et al. 2010).
Die Polymerisation des AH Plus erfolgt durch die Polyamin-Monomere in seiner Zusammensetzung (1-Adamantanamin, N,N’-Dibenzyl-5-oxa-nonandi-amin-1,9, TCD-Diamin). Wenn die Diepoxidverbindungen und die Polyaminpaste miteinander vermischt werden, reagieren die Aminogruppen mit den Epoxidgruppen, um eine kovalente Bindung zu bilden. Die Nutzung von aliphatischen cyclischen Aminogruppen fördert Modifikationen in der Aushärtegeschwindigkeit, der Vernetzungsdichte und der Morphologie von Epoxidharzen. Jede NH-Gruppe kann mit einer Epoxidgruppe reagieren, sodass das resultierende Polymer stark vernetzt ist und somit starr und stark ist (McDermott 1993, Case et al. 2005). Dies könnte die homogene und kompakte raue Oberfläche erklären, die in der SEM-Analyse sichtbar wurde, sowie die niedrigen Löslichkeitsergebnisse von AH Plus in der vorliegenden Studie. Schäfer & Zandbiglari (2003) haben auch die Löslichkeit von Epoxidharzen (AH Plus, AH 26), silikonbasierten (RoekoSeal), Calciumhydroxid (Apexit, Sealapex), Zinkoxid-Eugenol (Aptal-Harz) und glasionomerbasierten (Ketac Endo) Dichtstoffen in Wasser und künstlichem Speichel gemessen. Laut diesen Autoren hatte AH Plus den geringsten Gewichtsverlust aller getesteten Dichtstoffe, unabhängig vom verwendeten Löslichkeitsmedium.
Frühere Ergebnisse haben gezeigt, dass auf Polydimethylsiloxan basierende Dichtstoffe während der Aushärtung leicht expandieren und eine minimale Wasseraufnahme und Löslichkeit aufweisen (Donnelly et al. 2007, Monticelli et al. 2007). In Übereinstimmung mit dieser Aussage hatten in der vorliegenden Studie die Dichtstoffe GuttaFlow und RoekoSeal eine geringe Löslichkeit mit minimaler Freisetzung von Metallionen. Im Hinblick auf den Test zur dimensionalen Veränderung war GuttaFlow der einzige Dichtstoff, der der Spezifikation 57 (ANSI/ADA 2000) entsprach und eine Expansion von etwa 0,44% aufwies. Dasselbe wurde bei seinem Vorgänger, RoekoSeal, nicht beobachtet, der eine Schrumpfung (1,33%) zeigte. Im Gegensatz dazu stimmte dieses Ergebnis nicht mit Ørstavik et al. (2001) überein, die berichteten, dass Roeko-Seal innerhalb von 4 Wochen eine kleine Expansion von etwa 0,2% hatte und danach stabil war.
Die Anwesenheit von Guttapercha und Nano-Silberpartikeln im GuttaFlow-Dichtstoff verleiht der Polymermatrix eine bessere Stabilität aufgrund der Anziehungskraft zwischen Silberatomen und Guttapercha-Molekülen im Polymernetzwerk (Malynych et al. 2001). Diese Wechselwirkungen können die geringe Silberionenfreisetzung von GuttaFlow erklären, die in der atomaren Absorptionsspektroskopie beobachtet wurde. Darüber hinaus führte die Anwesenheit von Guttapercha im Polymernetzwerk von GuttaFlow zu einer höheren Wasseradsorption als bei RoekoSeal (Gong et al. 2008), was die Unterschiede in den Ergebnissen des Tests zur dimensionalen Veränderung und die gleichmäßigere und kompaktere Schicht erklärt, die auf der Oberfläche von RoekoSeal unter SEM beobachtet wurde.
Die höchsten Ergebnisse der Löslichkeit und der dimensionalen Veränderung des Activ GP Dichtungsmittels könnten mit der Methodik von ANSI/ADA zusammenhängen, die empfiehlt, dass eine Probe nach einer Zeitspanne von dreimal der Aushärtezeit des Materials in Wasser eingetaucht wird. Laut Wilson & McLean (1988) ist die Aushärtezeit des Ionomerzements erst 24 Stunden nach dem Mischen abgeschlossen. Während der Reifungszeit von Glas-Ionomer-Zementen kann die Anwesenheit von Feuchtigkeit zur Auflösung von Anionen und Kationen führen, die die Matrix für die Bereiche um den Zement bilden (Monticelli et al. 2007). Diese Ionenauflösung verhindert, dass Wasser, das Teil der Zementzusammensetzung ist, die Matrix hydratisiert (Ca2+ und Al3+ bilden Polysalze mit Gruppen von COO- der Polyacrylsäure), wodurch sie instabil wird (Carvalho-Júnior et al. 2003, Schäfer & Zandbiglari 2003, Donnelly et al. 2007). Dies könnte die rauere Oberfläche erklären, die im SEM beobachtet wurde, und das signifikante Niveau der Freisetzung von Calcium-, Kalium- und Zinkionen von Activ GP in der vorliegenden Studie. Da die Strukturen von Glas-Ionomer-Zementen wahrscheinlich von der Anwesenheit oder Abwesenheit von Wasser beeinflusst werden, sind sie empfindlich gegenüber Dehydration zu Beginn des Aushärteprozesses (Wilson & McLean 1988). Für die SEM-Bewertung ist die Dehydration der Probe ein wesentlicher Prozess, der die in der Oberfläche der Activ GP-Proben beobachteten Mikrorisse erklären könnte. Daher sollten die in der vorliegenden Studie mit Activ GP erzielten Ergebnisse mit Vorsicht interpretiert werden.
Schlussfolgerungen
Die Aushärtezeit aller Dichtstoffe entsprach den Anforderungen der ANSI/ADA. Activ GP erfüllte nicht die Protokolle der ANSI/ADA hinsichtlich Radiopazität, dimensionaler Veränderung und Löslichkeit. GuttaFlow war der einzige Dichtstoff, der in allen Tests der Spezifikation 57 entsprach. Die SEM-Analyse zeigte, dass die Oberflächen aller Dichtstoffe nach dem Löslichkeitstest mikromorphologische Veränderungen aufwiesen.
Autoren: D. S. H. Flores, F. J. A. Rached-Júnior, M. A. Versiani, D. F. C. Guedes, M. D. Sousa-Neto, J. D. Pécora
Referenzen:
- ANSI/ADA (2000) Spezifikation n° 57 Endodontisches Dichtmaterial. Chicago, USA: ADA Publishing.
- Baksi Akdeniz BG, Eyuboglu TF, Sen BH, Erdilek N (2007) Der Einfluss von drei verschiedenen Dichtstoffen auf die Radiopazität von Wurzelfüllungen in simulierten Kanälen. Oral Surgery Oral Medicine Oral Pathology Oral Radiology and Endodontics 103, 138–41.
- Bouillaguet S, Shaw L, Barthelemy J, Krejci I, Wataha JC (2008) Langfristige Dichtfähigkeit von Pulp Canal Sealer, AH-Plus, GuttaFlow und Epiphany. International Endodontic Journal 41, 219–26.
- Carvalho-Júnior JR, Guimarães LF, Correr-Sobrinho L, Pécora JD, Sousa-Neto MD (2003) Bewertung der Löslichkeit, Disintegration und dimensionalen Veränderungen eines Glas-Ionomer-Wurzelkanaldichtstoffs. Brazilian Dental Journal 14, 114–8.
- Carvalho-Júnior JR, Correr-Sobrinho L, Correr AB, Sinhoreti MA, Consani S, Sousa-Neto MD (2007a) Radiopazität von Wurzelfüllmaterialien unter Verwendung digitaler Radiographie. International Endodontic Journal 40, 514–20.
- Carvalho-Júnior JR, Correr-Sobrinho L, Correr AB, Sinhoreti MA, Consani S, Sousa-Neto MD (2007b) Löslichkeit und dimensionale Veränderung nach der Aushärtung von Wurzelkanaldichtstoffen: ein Vorschlag für kleinere Dimensionen der Testproben. Journal of Endodontics 33, 1110–6.
- Case SL, O’Brien EP, Ward TC (2005) Aushärtungsprofile, Vernetzungsdichte, Restspannungen und Haftung in einem Modell-Epoxid. Polymer 46, 10831–40.
- De-Deus G, Brandão MC, Fidel RA, Fidel SR (2007) Die Dichtfähigkeit von GuttaFlow in ovalen Kanälen: eine ex vivo-Studie mit einem polymikrobiellen Leckagemodell. International Endodontic Journal 40, 794–9.
- Donnelly A, Sword J, Nishitani Y et al. (2007) Wasseraufnahme und Löslichkeit von methacrylatbasierten Wurzelkanaldichtstoffen. Journal of Endodontics 33, 990–4.
- Eldeniz AU, Ørstavik D (2009) Eine Laborbewertung der koronalen bakteriellen Leckage in Wurzelkanälen, die mit neuen und konventionellen Dichtstoffen gefüllt sind. International Endodontic Journal 42, 303–12.
- Fransen JN, He J, Glickman GN, Rios A, Shulman JD, Honeyman A (2008) Vergleichende Bewertung von ActiV GP/Glas-Ionomer-Dichtstoff, Resilon/Epiphany und Gutta-Percha/AH Plus Obturierung: eine bakterielle Leckage-Studie. Journal of Endodontics 34, 725–7.
- Gambarini G, Testarelli L, Pongione G, Gerosa R, Gagliani M (2006) Radiografische und rheologische Eigenschaften eines neuen endodontischen Dichtstoffs. Australian Endodontic Journal 32, 31–4.
- Garrido ADB, Lia RCC, França EC, da Silva JF, Astolfi-FIlho S, Sousa-Neto MD (2010) Laborbewertung der physikochemischen Eigenschaften eines neuen Wurzelkanaldichtstoffs auf Basis von Copaifera multijuga Öl-Harz. International Endodontic Journal 43, 283–91.
- Gençoglu N, Türkmen C, Ahiskali R (2003) Ein neuer silikonbasierter Wurzelkanaldichtstoff (Roekoseal-Automix). Journal of Oral Rehabilitation 30, 753–7.
- Gong W, Zeng K, Wang L, Zheng S (2008) Poly(hydroxyether von Bisphenol A)-block-polydimethylsiloxan alternierendes Blockcopolymer und seine nanostrukturierten Mischungen mit Epoxidharz. Polymer 49, 3318–26.
- Kontakiotis EG, Tzanetakis GN, Loizides AL (2007) Eine vergleichende Studie der Kontaktwinkel von vier verschiedenen Wurzelkanaldichtstoffen. Journal of Endodontics 33, 299–302.
- Lin-Gibson S, Landis FA, Drzal PL (2006) Kombinatorische Untersuchung der Struktur-Eigenschaften-Charakterisierung von photopolymerisierten Dimethacrylat-Netzwerken. Biomaterials 27, 1711–7.
- Malynych S, Robuck H, Chumanov G (2001) Herstellung von zweidimensionalen Assemblierungen von Ag-Nanopartikeln und Nano-Hohlräumen in Poly(dimethylsiloxan)-Harz. Nano Letters 1, 647–9.
- McDermott J (1993) Die Struktur der fortschrittlichen Verbundwerkstoffindustrie: Advance Composites Bluebook. Cleveland: Advanstar Communications.
- Monticelli F, Sword J, Martin RL et al. (2007) Dichtfähigkeit von zwei zeitgenössischen Einzelkonus-Obturationssystemen. International Endodontic Journal 40, 374–85.
- Ørstavik D (1983) Physikalische Eigenschaften von Wurzelkanaldichtstoffen: Messung von Fließfähigkeit, Arbeitszeit und Druckfestigkeit. International Endodontic Journal 16, 99–107.
- Ørstavik D (2005) Materialien, die für die Wurzelkanalobturierung verwendet werden: technische, biologische und klinische Tests. Endodontic Topics 12, 25–38.
- Ørstavik D, Nordahl I, Tibballs JE (2001) Dimensionale Veränderung nach der Aushärtung von Wurzelkanaldichtstoffen. Dental Materials 17, 512–9.
- Phillips RW, Skinner EW (1991) Skinner’s Science of Dental Materials, 9. Auflage. Philadelphia: Saunders.
- Rasimick BJ, Shah RP, Musikant BL, Deutsch AS (2007) Radiopazität von endodontischen Materialien auf Film und einem digitalen Sensor. Journal of Endodontics 33, 1098–101.
- Resende LM, Rached-Junior FJ, Versiani MA et al. (2009) Eine vergleichende Studie der physikochemischen Eigenschaften von AH Plus, Epiphany und Epiphany SE Wurzelkanaldichtstoffen. International Endodontic Journal 42, 785–93.
- Roggendorf MJ, Legner M, Ebert J, Fillery E, Frankenberger R, Friedman S (2010) Mikro-CT-Bewertung von Restmaterial in Kanälen, die mit Activ GP oder GuttaFlow nach Entfernung mit NiTi-Instrumenten gefüllt sind. International Endodontic Journal 43, 200–9.
- Schäfer E, Zandbiglari T (2003) Löslichkeit von Wurzelkanaldichtstoffen in Wasser und künstlichem Speichel. International Endodontic Journal 36, 660–9.
- Tagger M, Katz A (2003) Radiopazität von endodontischen Dichtstoffen: Entwicklung einer neuen Methode zur direkten Messung. Journal of Endodontics 29, 751–5.
- Tanomaru-Filho M, Jorge EG, Guerreiro Tanomaru JM, Goncalves M (2007) Bewertung der Radiopazität neuer Wurzelkanalfüllmaterialien durch Digitalisierung von Bildern. Journal of Endodontics 33, 249–51.
- Tanomaru-Filho M, Jorge EG, Tanomaru JM, Goncalves M (2008) Bewertung der Radiopazität von Wurzelkanaldichtstoffen auf Basis von Calciumhydroxid und Glas-Ionomer. International Endodontic Journal 41, 50–3.
- Tas¸demir T, Yesilyurt C, Yildirim T, Er K (2008) Bewertung der Radiopazität neuer Wurzelkanalpasten/Dichtstoffe durch digitale Radiographie. Journal of Endodontics 34, 1388–90.
- Versiani MA, Carvalho-Junior JR, Padilha MI, Lacey S, Pascon EA, Sousa-Neto MD (2006) Eine vergleichende Studie der physikochemischen Eigenschaften von AH Plus und Epiphany Wurzelkanaldichtstoffen. International Endodontic Journal 39, 464–71.
- Wilson AD, McLean JW (1988) Glas-Ionomer-Zement. Chicago: Quintessence Pub. Co.
