Vergleich der intraossären Biokompatibilität von AH Plus, EndoREZ und Epiphany Wurzelkanaldichtstoffen
Maschinenübersetzung
Der Originalartikel ist in EN Sprache (Link zum Lesen) geschrieben.
Zusammenfassung
Um die intraossäre Biokompatibilität von AH Plus, EndoREZ und Epiphany Wurzelkanalversiegelungen zu bewerten, wie im Technischen Bericht #9 der Fédération Dentaire Internationale (FDI) empfohlen. Dreißig Meerschweinchen, 10 für jedes Material, unterteilt in experimentelle Zeiträume von 4 und 12 Wochen, erhielten ein Implantat auf jeder Seite der Symphyse des Unterkiefers. Am Ende der Beobachtungszeiträume wurden die Tiere getötet und die Proben für die routinemäßige histologische Untersuchung vorbereitet. Nach der Analyse beider Zeiträume wurde die entzündliche Gewebereaktion auf EndoREZ als schwerwiegend angesehen. In der AH Plus-Gruppe änderte sich die Reaktion von schwerwiegend zu moderat, während eine biologische Kompatibilität zu Epiphany mit Knochenbildung und keiner bis leichter entzündlicher Reaktion beobachtet wurde. Es wurde festgestellt, dass Epiphany Wurzelkanalversiegelung das einzige Material war, das innerhalb der beiden analysierten Zeiträume intraossäre Biokompatibilität aufwies. (J Endod 2006;32:656 – 662)
Der Erfolg der Wurzelkanalbehandlung hängt von der vollständigen Entfernung des infizierten Kanalinhalts ab, gefolgt von der Füllung mit einem Material von angemessener Kompatibilität, um mögliche Reizungen des periradikulären Gewebes zu vermeiden. Da Gewebeverletzungen, die durch intrakanaläre Verfahren verursacht werden, zu ungünstigen Reaktionen auf die Behandlung führen können, sollte die Wahl des Praktikers für die während der Wurzelkanalbehandlung anzuwendenden Verfahren auf solchen beruhen, von denen bekannt ist, dass sie so wenig Schaden wie möglich verursachen. Es wurde nachgewiesen, dass fremde Materialien, wie Wurzelkanalversiegelungen, die nach der endodontischen Behandlung in periradikulären Geweben eingeschlossen sind, die apikale Parodontitis perpetuieren können.
Es wurde auch gezeigt, dass die Biokompatibilität zu den periradikulären Geweben das wichtigste Kriterium ist, da jedes Material, das biologisch nicht akzeptabel ist, für Misserfolge verantwortlich sein kann. In Bezug auf die biologischen Eigenschaften von endodontischen Materialien gibt es eine breite Palette von Merkmalen, die berücksichtigt werden sollten. Die Methoden zur Bewertung der Parameter umfassen Ersttests, Sekundärtests und Anwendungsstudien. Die erste Bewertung sollte in vitro-Methoden zur Beurteilung des Toxizitätsprofils des Materials umfassen. Die Sekundärtests sollten in vivo an Labortieren durchgeführt werden und können Implantationsexperimente einschließen. Die Anwendungsstudien werden an Primaten oder Menschen durchgeführt.
Die derzeit in der klinischen Praxis verwendeten Materialien umfassen Harz-, Zinkoxid-Eugenol-, Glas-Ionomer-, Calciumhydroxid- und silikonbasierte endodontische Dichtstoffe. Harzfüllmaterialien haben stetig an Beliebtheit gewonnen und werden jetzt als Wurzelkanaldichtstoffe akzeptiert. Verbesserungen in der Klebetechnologie haben Versuche gefördert, apikale und koronale Undichtigkeiten durch Verklebung an den Wurzelkanalwänden zu reduzieren. So wurden die neuartigen methacrylatbasierten Harzdichtstoffe EndoREZ und Epiphany kürzlich entwickelt. Die biologischen Eigenschaften von EndoREZ wurden bereits hinsichtlich seiner Zytotoxizität und Gewebe-Biokompatibilität untersucht. Andernfalls sind die biologischen Eigenschaften von Epiphany, einem dual härtbaren zahnmedizinischen Harzkompositdichtstoff, schlecht untersucht.
Es wurde festgestellt, dass die biologische Grundlage für die Wurzelkanaltherapie hinter den beeindruckenden technologischen Fortschritten in der Endodontie zurückbleibt. Allerdings fehlt es der Mehrheit der Materialien, obwohl sie vor der klinischen Anwendung beworben werden, an sogar grundlegenden Sicherheitstests.
Bis heute wurden keine Studien durchgeführt, um den histologischen Effekt der Implantation von Epiphany im Knochen zu analysieren. Daher war das Ziel dieser Studie, die biologischen Eigenschaften der neu entwickelten methacrylatbasierten Wurzelkanalversiegelungen EndoREZ und Epiphany zu bewerten, im Vergleich zu einem konventionellen, gut etablierten Epoxid-Aminharz-Wurzelkanalversiegler AH Plus, unter Verwendung des von der Fédération Dentaire Internationale (FDI) empfohlenen Protokolls.
Materialien und Methoden
Die bewerteten Materialien waren AH Plus (Dentsply, DeTrey, Konstanz, Deutschland), EndoREZ (Ultradent Products, Inc., South Jordan, UT) und Epiphany (Pentron Clinical Technologies, Wallingford, CT) Wurzelkanalversiegler. Alle Materialien wurden gemäß den Empfehlungen des Herstellers für ihre klinische Anwendung vorbereitet und in Teflon-Träger (Polytetrafluorethylen, DuPont, HABIA, Knivsta, Schweden) geladen, wobei sichergestellt wurde, dass keine Luft eingeschlossen wurde. Das Protokoll für dieses Experiment wurde vom Forschungsethikausschuss der Universität Uberlândia überprüft und genehmigt, und das Experiment wurde in Übereinstimmung mit den 'Prinzipien der Pflege von Labortieren' (NIH, Nr. 86-23, 1985) durchgeführt.
Das intraossäre Implantat im Unterkiefer des Meerschweinchens und die standardisierten Methoden zur Bewertung der biologischen Eigenschaften, die im Technischen Bericht #9 FDI empfohlen werden, wurden verwendet. Dreißig Meerschweinchen (mit einem Gewicht von ~800 g) wurden ausgewählt, und jedes Tier erhielt zwei Implantate aus demselben Material. Zehn Proben wurden für jedes Material und Beobachtungszeitraum verwendet. Darüber hinaus diente die Reaktion des Bindegewebes entlang der lateralen Wand außerhalb der Teflon-Tasse als negativer Kontrollversuch für die Technik.
Die Tiere wurden intraperitoneal mit 0,6 ml Ketamin, das Acepromazin im Verhältnis 1:1 enthielt, anesthesiert. Um lokale Beschwerden zu vermeiden, wurde 0,6 ml 2% Xylocain mit Epinephrin (1:100.000) in die mukobukkale Falte der Region der mandibulären Schneidezähne injiziert. Der submandibuläre Bereich wurde rasiert und die Haut mit 5% Jodtinktur desinfiziert. Der distale ventrale Symphysebereich des Unterkiefers wurde unter antiseptischen Bedingungen chirurgisch durch einen Schnitt in die Haut und das Muskelgewebe freigelegt. Der mandibuläre Knochen auf beiden Seiten der Symphyse wurde freigelegt, und zylindrische Löcher mit einem Durchmesser von 2 mm und einer Tiefe von 2 mm wurden mit Bohrern unter steriler physiologischer Kochsalzlösung hergestellt. Sterilisierte zylindrische Teflon-Tassen, die an einem Ende offen sind und deren Außenseiten gewindet sind, um Halterillen zu bieten, wurden unter sterilen Bedingungen mit den Materialien gefüllt und in die knöchernen Hohlräume eingesetzt, sodass die Füllmaterialien mit dem Knochen in Kontakt kamen und die sterile Bedingung aufrechterhalten wurde. Die Zylinder waren 2,0 mm lang und hatten einen Innendurchmesser von 1,3 mm und einen Außendurchmesser von 2,0 mm. Zufällige Proben der Zylinder wurden in Röhrchen mit Brewer-Thioglykolat-Medium platziert und aerob für 4 Tage inkubiert, um ihre Sterilität zu bestimmen.
Nachdem die Tassen an ihrem Platz waren, wurden die Weichgewebe ersetzt und unabhängig mit einem 3-0 resorbierbaren Material genäht. Die Beobachtungszeiträume betrugen 4 und 12 Wochen, als die Meerschweinchen getötet wurden, wurde der Unterkiefer herausdisseziert und der Knochen, der in situ an den Tassen angrenzte, in 10-mm-Blöcke geschnitten. Die Proben wurden in einer 10% gepufferten Formalinlösung eingelegt und für die routinemäßige histologische Untersuchung vorbereitet. Serielle Schnitte, mit dem Mikrotom auf eine Dicke von 5 µm eingestellt, wurden geschnitten und mit Hämatoxylin und Eosin (H&E) gefärbt, um die Zellen zu erkennen. Ausgewählte Objektträger wurden mit den Masson’s Trichrome- und Brown- und Brenn-Techniken gefärbt, um Kollagen und bakterielle Kontamination zu erkennen.
Die Schnittstelle an der Öffnung der Tasse, zwischen dem Material und dem Knochen, wurde untersucht und auf die Intensität der Entzündung bewertet. Die FDI-Kriterienbewertung ist ausschließlich qualitativ und es wurde kein Bewertungsindex verwendet. Daher wurde das allgemeine Niveau der Gewebereaktion als none bis slight, moderate und severe bewertet, abhängig von der Anwesenheit oder Abwesenheit von neutrophilen Leukozyten, Makrophagen, Lymphozyten, Plasmazellen, riesigen Fremdkörperzellen, dispergiertem Material, Kapsel, neu gebildetem gesundem Knochen, nekrotischem Gewebe und Resorption.
Zwei unabhängige Beobachter bewerteten blind die Reaktionen. Zuvor wurde jedoch jeder Prüfer kalibriert, indem er zweimal eine Standardreihe von 50 Folien hinsichtlich der Intensität und Art der entzündlichen Reaktion bewertete. Die Übereinstimmung zwischen den Prüfern, berechnet als Cohens Kappa, lag zwischen 0,8 und 0,95. Die Reproduzierbarkeit innerhalb der Prüfer wurde durch eine doppelte Bewertung von 25 zufällig ausgewählten Folien im Abstand von 1 Monat bewertet. In diesem Fall lag Cohens Kappa zwischen 0,85 und 0,91. Es wurde als biologisch akzeptabel angesehen, wenn das Material in beiden experimentellen Zeiträumen keine bis leichte Reaktion oder eine moderate Reaktion nach 4 Wochen zeigte, die sich nach 12 Wochen verringerte.
Ergebnisse
Die Anzahl der intraossären Implantate und die Intensität der entzündlichen Reaktion sind in Tabelle 1 dargestellt. Die histologische Bewertung der Materialien nach 4 und 12 Wochen ist in Tabelle 2 zusammengefasst.

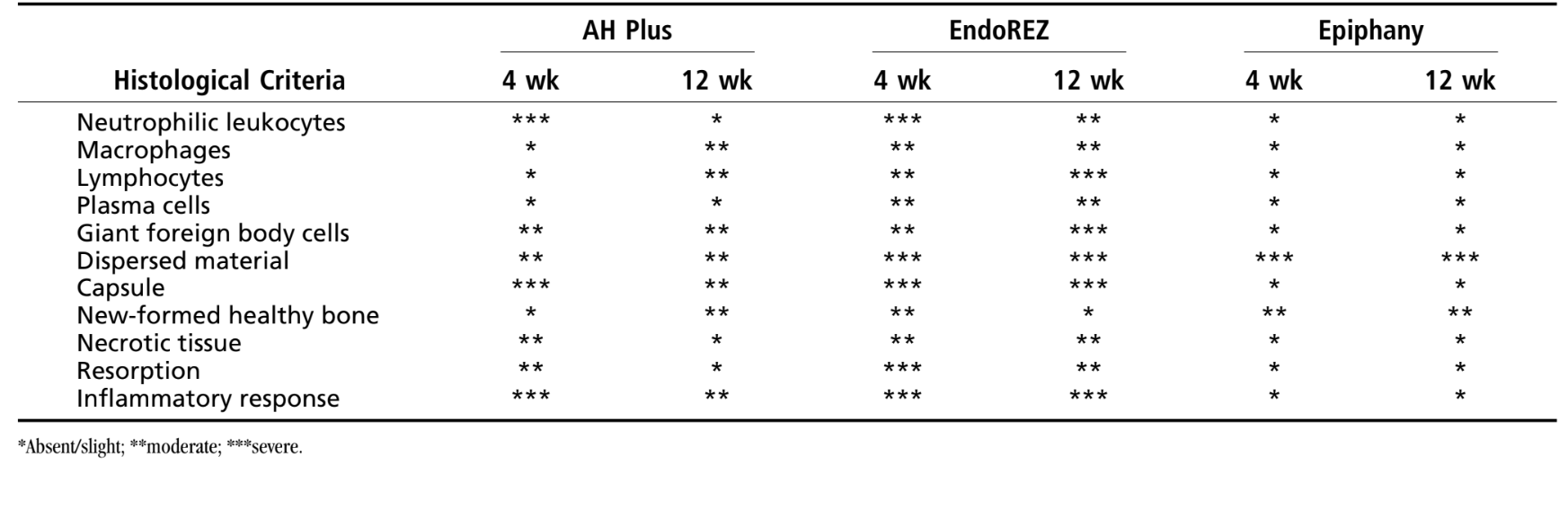
Keine der mit der Brown- und Brenn-Technik gefärbten Folien zeigte das Vorhandensein von bakterieller Kolonisierung in irgendeinem der experimentellen Implantate. Die Zylinder, die mit denen gelagert wurden, die im Kulturmedium Wachstum erzeugten, waren negativ. Die Reaktion des Bindegewebes entlang der seitlichen Wand außerhalb der Teflonbecher aller Proben diente als negativer Kontrollversuch für die Technik. Es war möglich zu beobachten, dass die Rillen auf der Außenseite der Becher mit neuem Knochengewebe gefüllt waren, und eine dünne Schicht Bindegewebe, ohne entzündliche Reaktion, war zwischen dem Becher und dem Knochen in allen Beobachtungszeiträumen bei allen getesteten Proben zu sehen.
Beobachtungen nach vier Wochen
AH Plus
Die Reaktion wurde als schwerwiegend angesehen. Es gab eine dünne Schicht Bindegewebe, die sich zwischen dem Material und dem Knochen befand (Abb. 1b) und die intensive entzündliche Infiltration zeigte das Vorhandensein von Lymphozyten, Makrophagen und riesigen Fremdkörperzellen, nekrotischen Knochenfragmenten (Abb. 1c).

EndoREZ
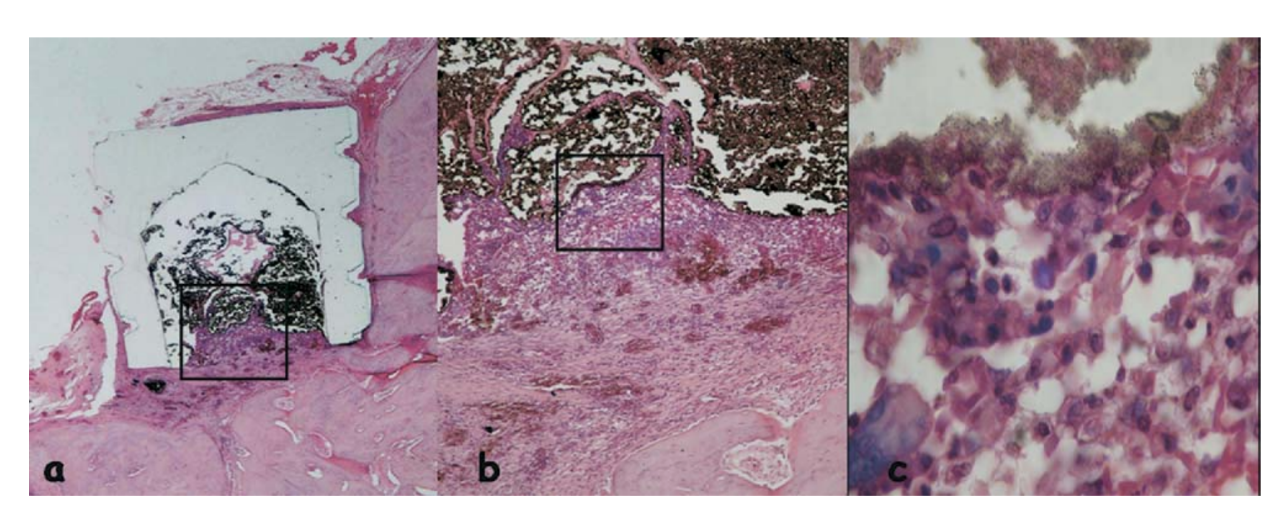
Die Reaktion wurde als schwerwiegend angesehen, mit einem intensiven chronischen entzündlichen Infiltrat, mit der Prävalenz von Lymphozyten, Makrophagen und riesigen Fremdkörperzellen (Abb. 3c). Es gab einige verstreute Materialien und die Bildung einer dicken Schicht von Bindegewebe, die zwischen dem Material und dem Knochen lag (Abb. 3d).
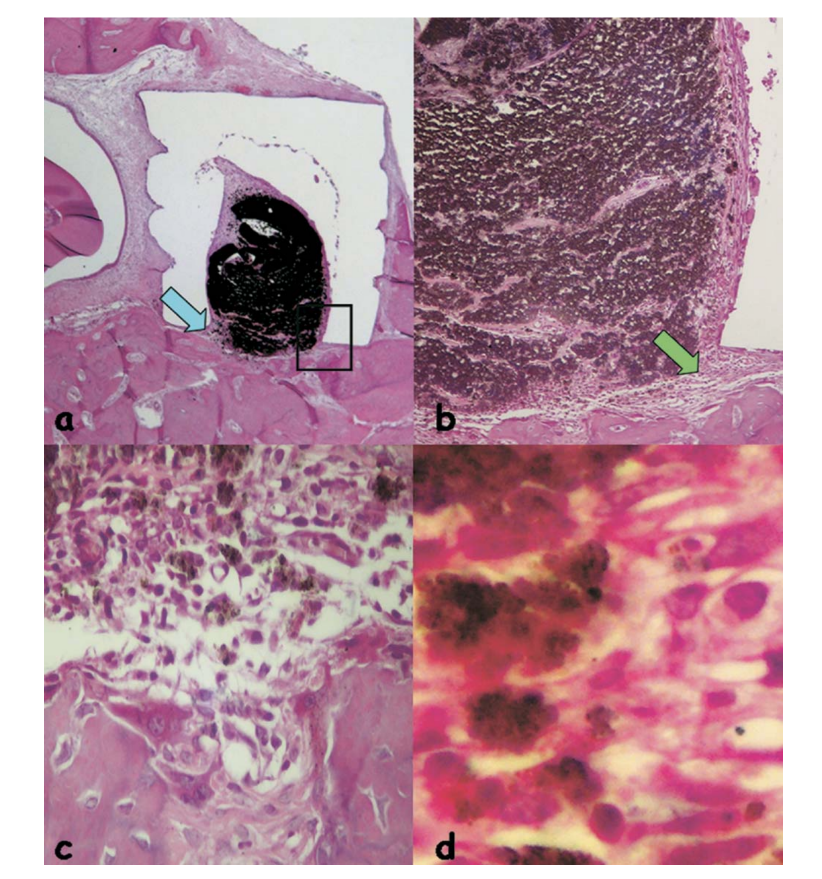
und dem Knochen liegt (umrissene Fläche in a) (H&E, Originalvergrößerung 40x); (c) Bindegewebe mit einigen verstreuten Materialien (grüner Pfeil in b) (H&E, Originalvergrößerung 100x); (d) chronisches entzündliches Infiltrat und Zellen mit Fragmenten des getesteten Materials (blauer Pfeil in a) (H&E, Originalvergrößerung 400x).
Epiphanie
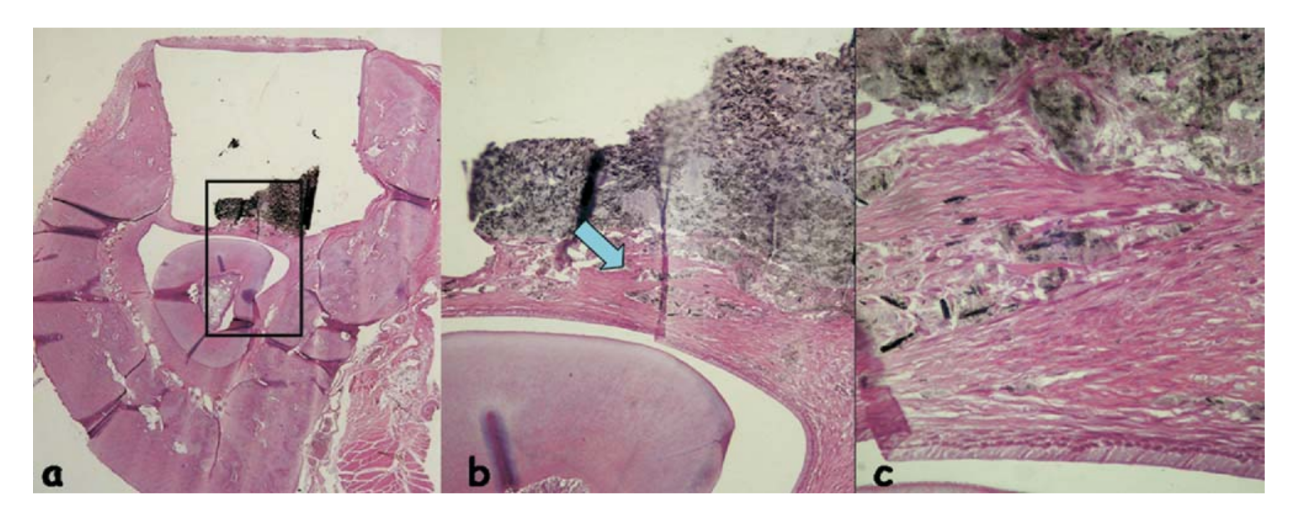
Die entzündliche Reaktion wurde als none bis leicht eingestuft. Es wurde ein organisiertes Bindegewebe in engem Kontakt mit dem getesteten Material beobachtet (Abb. 5b), einige entzündliche Zellen und etwas verstreutes Material (Abb. 5c).
Beobachtungen nach zwölf Wochen
AH Plus
Es wurde eine chronische Entzündungsreaktion festgestellt, die als moderat eingestuft wurde. Es wurde das Vorhandensein einiger riesiger Fremdkörperzellen und einer dünnen Schicht von Bindegewebe beobachtet, die zwischen dem neu gebildeten Knochen und dem implantierten Material lag (Abb. 2c).
EndoREZ
Die entzündliche Reaktion war weiterhin schwerwiegend mit einem intensiven chronischen entzündlichen Infiltrat, mit der Prävalenz von Lymphozyten, Makrophagen und riesigen Fremdkörperzellen (Abb. 4b). Es wurde das Vorhandensein von dispersem Material, hämorrhagischen Bereichen und hyperämischen Gefäßen beobachtet (Abb. 4c).
Epiphanie
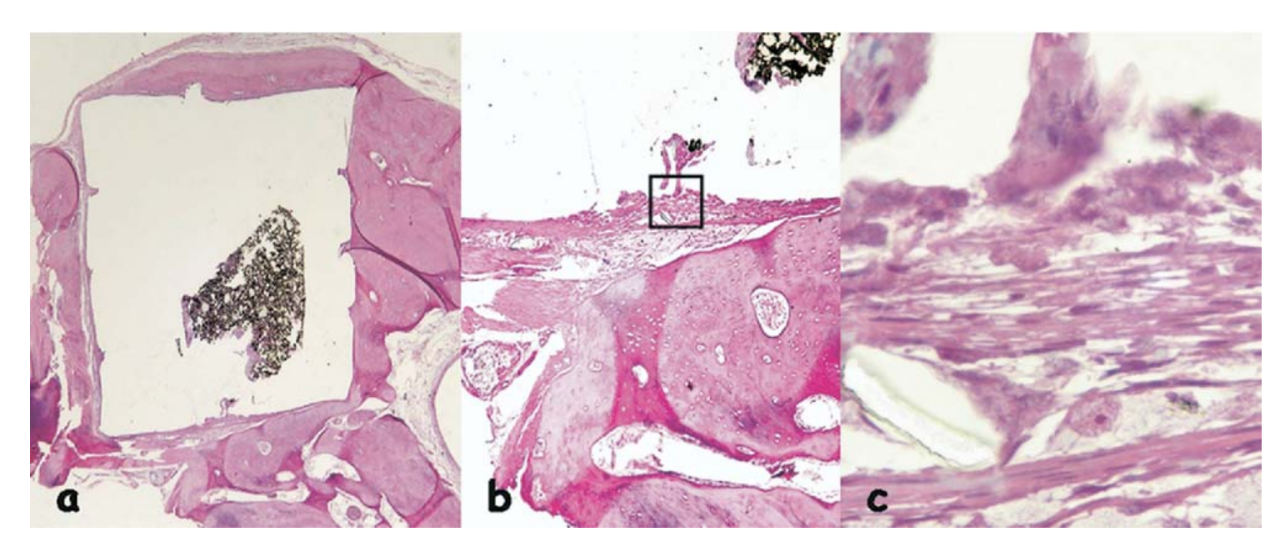
Die entzündliche Reaktion wurde als none bis leicht eingestuft. Es wurde die Anlagerung eines neu gebildeten gesunden Knochens in der Nähe des Materials beobachtet (Abb. 6b) und eine dünne Schicht von Bindegewebe, die dem getesteten Material ohne entzündliche Zellen benachbart ist (Abb. 6c, d).
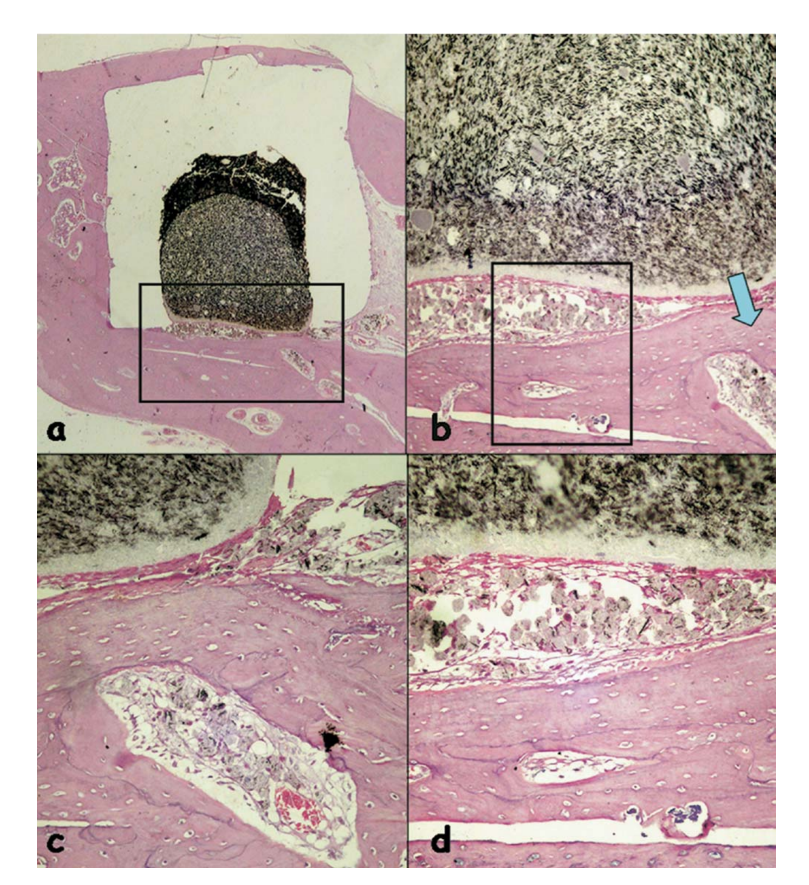
(b) Anlagerung eines neu gebildeten gesunden Knochens in der Nähe des Materials (umrissener Bereich in a) (H&E, Originalvergrößerung 40x); (c) Detail des neu gebildeten gesunden
Knochens (blauer Pfeil in b) (H&E, Originalvergrößerung 100x); (d) dünne Schicht von Bindegewebe, die dem getesteten Material gegenüberliegt (umrissener Bereich in b) (H&E, Originalvergrößerung 200x).
Diskussion
Wenn ein neues Material auf den Markt gebracht wird oder ein bestehendes Material für eine andere Anwendung vorgeschlagen wird, sollten seine Eigenschaften untersucht und die gefundenen Ergebnisse mit den Ergebnissen anderer Forscher verglichen werden. In den Vereinigten Staaten war die Food and Drug Administration (FDA) verantwortlich für die Bewertung und Beurteilung der biologischen Auswirkungen aller Medikamente, Materialien und Geräte, die beim Menschen verwendet werden, einschließlich der meisten zahnmedizinischen Produkte und Geräte. Die FDA erkannte auch Standards an, die von privaten Organisationen, wie der ANSI/ADA, festgelegt wurden. Die Überarbeitung der erstmals veröffentlichten empfohlenen Standardpraktiken für die biologische Bewertung von zahnmedizinischen Materialien wurde verzögert, um die wesentlichen Punkte der Empfehlungen der FDA zu berücksichtigen. Dieses neue Dokument sollte nicht die industrielle Entwicklung neuer und verbesserter zahnmedizinischer Produkte behindern, indem es übermäßige biologische Tests fordert. In dieser Ära der Besorgnis über chemische Gefahren sollte jedoch ein Toxizitätsprofil für alle neuen und verbesserten Materialien entwickelt werden, um relevante Daten zur Sicherheit und Wirksamkeit zu erhalten. Auch wenn keine Menge an experimenteller Forschung absolute Sicherheit für irgendeine Substanz garantieren kann, liefern toxikologische Untersuchungen Daten, aus denen vernünftige Projektionen und Vorhersagen über die Bedingungen, unter denen das Mittel sicher verwendet werden kann, abgeleitet werden können.
Obwohl viele Tests wie Zytotoxizität, Hämolyse, Ames-Test, Styles-Zelltransformation, subkutane und Knochenimplantationen, Sensibilisierung und endodontische Nutzungstests für verschiedene Teststufen aufgeführt sind, sind sie nicht alle für jedes Produkt erforderlich. Es muss eine Entscheidung getroffen werden, welche Tests relevant sind. Die anfänglichen Tests sollen ein Profil der Toxizität in einem biologischen System liefern, sodass der Hersteller auf Vergleichsbasis eine grobe Einschätzung und Vorstellung davon hat, wo sein Produkt steht. Die von der FDA regulierten Geräte fallen in drei Klassen, jedoch würde eine davon, die die Mehrheit der zahnärztlichen Geräte und Hilfsmittel umfasst, nicht der Festlegung von Standards für die Marktzulassung unterliegen. Mit anderen Worten, manchmal sind sogar grundlegende Sicherheitstests nicht erforderlich, bevor Produkte für die klinische Anwendung beworben werden können.
Die Biokompatibilität von zahnärztlichen Materialien ist eine wichtige Anforderung, da die in diesen Materialien enthaltenen toxischen Komponenten Irritationen oder sogar Degeneration des umgebenden Gewebes verursachen könnten, insbesondere wenn sie versehentlich in das periradikuläre Gewebe extrudiert werden.
Schwere Reaktionen wurden nach der Extrusion einiger häufig verwendeter Substanzen in das periradikuläre Gewebe berichtet. Überdehnte Wurzelkanaldichtstoffe stellen ebenfalls eine chemische Reizung dar, da nahezu alle endodontischen Dichtstoffe bei frischer Zubereitung hochgiftig sind. Darüber hinaus könnte ihre reizende Wirkung zunehmen, je größer die Kontaktfläche zwischen Material und Gewebe ist. Je größer das Volumen des überdehnten Materials ist, desto größer ist die Kontaktfläche zwischen Dichtstoff und Gewebe und desto intensiver ist der chemische Schaden.
Der Implantat-Test im Knochengewebe von Meerschweinchen, wie von der FDI empfohlen, ermöglicht die Prüfung des Materials, wie es in der klinischen Einrichtung verwendet wird. Obwohl die Ergebnisse nicht direkt auf Menschen extrapoliert werden können, ist der Test standardisiert und ein direkter Vergleich zwischen Materialien kann hergestellt werden. Die Reaktionen entlang der äußeren Wände der Tasse spiegeln das Trauma wider, das durch die für die Implantation notwendigen chirurgischen Eingriffe verursacht wurde. Teflon selbst hat sich als nur geringfügig reizend für das Gewebe erwiesen und wurde aufgrund seiner Biokompatibilität als Trägermaterial verwendet. Unsere Ergebnisse bestätigten das Fehlen von Entzündungsreaktionen an der Seitenwand der Träger in beiden Beobachtungszeiträumen.
AH Plus, ein zweikomponentiger Paste-Wurzelkanal-Dichtstoff, der auf der Polymerisationsreaktion von Epoxidharz-Aminen basiert, wurde zum Vergleich getestet. Der AH Plus-Dichtstoff zeigte während des 4-wöchigen Beobachtungszeitraums eine starke Reaktion, die sich nach 12 Wochen auf eine moderate Reaktion verringerte (Abb. 1 und 2). Der Mechanismus, der die entzündliche Reaktion in Bezug auf den AH Plus-Dichtstoff erklären könnte, ist die Freisetzung von Formaldehyd, das nachweislich nicht-neoplastische Reaktionen wie epitheliäre Degeneration und eine gemischte Infiltration von Entzündungszellen induziert, neben allergischen Reaktionen und Nekrose des Bindegewebes. Eine andere Studie hat gezeigt, dass einige Dichtstoffe erhebliche biologische Risiken darstellen, insbesondere in frisch gemischtem Zustand. Allerdings kann auch nach der Aushärtezeit weiterhin Toxizität bestehen. Daher könnten die in der Zusammensetzung von AH Plus enthaltenen Amine, die die Polymerisation beschleunigen, ebenfalls der Grund für die starke anfängliche Toxizität sein. Darüber hinaus könnte die entzündliche Aktivität zusammen mit der intakten Blutversorgung im Gewebeheilungsprozess die anfängliche Toxizität des Materials beseitigen.
Vor kurzem wurde ein neuer methacrylatbasierter endodontischer Dichtstoff, EndoREZ, als Wurzelkanaldichtstoff eingeführt. EndoREZ ist ein hydrophiles, zweikomponentiges, chemisch härtendes Material, das Zinkoxid, Barium-Sulfat, Harze und Pigmente in einer Matrix aus Urethan-Dimethacrylat-Harz enthält. In der vorliegenden Studie verursachte EndoREZ in allen experimentellen Zeiträumen eine schwere Entzündungsreaktion (Abb. 3 und 4). An kultivierten Zellen wurde gezeigt, dass EndoREZ mit der Zeit der Exposition zunehmend zytotoxisch wurde und bei frisch gemischtem Material signifikante zytotoxische Risiken aufwies. Die Reaktion des Bindegewebes auf mit EndoRez gefüllte Silikontuben, die in das subkutane Gewebe von Ratten implantiert wurden, zeigte eine schwere Reaktion, die ihr Profil nach 30 Tagen erheblich veränderte, mit einer moderaten Reaktion nach 3 Monaten und ohne Entzündung im vierten Beobachtungszeitraum. Dennoch wurde auch berichtet, dass bei einigen Tieren die Entzündungsreaktion in allen experimentellen Zeiträumen anhielt. Es wurde angenommen, dass nach der subkutanen Implantation von frischem EndoREZ Komponenten wie Zink und Barium in direktem Kontakt mit dem Gewebe standen und diese schwere anfängliche Reaktion verursachten. Im Gegensatz zu den Ergebnissen der vorliegenden Forschung zeigten Zmener et al. eine zufriedenstellende Reaktion des Knochengewebes im 60-tägigen Beobachtungszeitraum von EndoREZ, das in die Tibien von Ratten implantiert wurde. Der langsame Abbau des EndoREZ-Dichtstoffs, veranschaulicht durch das dispergierte Material, und die anschließende Endozytose durch Makrophagen könnten die Ursache für eine solche anhaltende chronische Entzündung gewesen sein. Außerdem scheint die Wurzelkanaltherapie, die mit seitlich kondensierten Guttapercha-Kegeln in Verbindung mit EndoRez durchgeführt wurde, eine gute Gesamterfolgsquote nach 14 bis 24 Monaten Nachuntersuchung aufzuweisen.
In unserer Studie zeigten AH Plus und EndoREZ keine biokompatiblen Eigenschaften, da die Reaktion in allen Zeiträumen schwerwiegend war und das Material gemäß den FDI-Kriterien als inakzeptabel angesehen wird. Epiphany ist ein dual-härtender, zahnmedizinischer, harzbasierten Kompositdichtstoff, dessen Harzmatrix eine Mischung aus Bisphenol-A-Glycidylmethacrylat, ethoxiliertem Bis-GMA, Urethan-Dimetacrylat-Harz und hydrophilen difunktionalen Metacrylaten ist. Die in dieser Arbeit erzielten Ergebnisse zeigten in beiden experimentellen Zeiträumen optimale biologische Reaktionen für dieses Material (Abb. 5 und 6). Kürzlich wurde in einer in vivo-Studie festgestellt, dass Epiphany mit weniger apikaler Parodontitis assoziiert war. Die Autoren korrelierten dieses Ergebnis mit der überlegenen Widerstandsfähigkeit von Epiphany gegen koronale Undichtigkeiten, die in einer früheren Arbeit nachgewiesen wurde. Allerdings zeigten Versiani et al., dass die Löslichkeit von Epiphany höher war als die von der ANSI/ADA-Spezifikation 57 festgelegte. Das für den Löslichkeitstest verwendete deionisierte destillierte Wasser wurde der atomaren Absorptionsspektrometrie unterzogen und zeigte eine umfangreiche Calciumfreisetzung (41,46 mg/L). Diese hohe Calciumfreisetzung durch Epiphany könnte die klinisch beobachtete reduzierte apikale Parodontitis und die Ergebnisse der vorliegenden Arbeit erklären. Die Freisetzung von Calciumionen hat sich als förderlich für einen alkalischeren pH-Wert der Umgebung erwiesen, was zu biochemischen Effekten führt, die im Beschleunigen des Reparaturprozesses kulminieren.
Fazit
Nach den Kriterien der FDI erlaubten die in dieser Studie erzielten Ergebnisse den Schluss, dass das Epiphany Wurzelkanalversiegelungsmaterial das einzige Material war, das intraossäre Biokompatibilität in den beiden analysierten Zeiträumen aufwies.
Autoren: Cássio J. A. Sousa, Cristiana R. M. Montes, Elizeu A. Pascon, Adriano M. Loyola, Marco A. Versiani
Referenzen:
- Sousa CJA, Loyola AM, Versiani MA, Biffi JCG, Oliveira RP, Pascon EA. Eine vergleichende histologische Bewertung der Biokompatibilität von Materialien, die in der apikalen Chirurgie verwendet werden. Int Endod J 2004;37:738 – 48.
- Siqueira JF Jr. Reaktion der periradikulären Gewebe auf die Wurzelkanalbehandlung: Vorteile und Nachteile. Endod Topics 2005;10:123– 47.
- Nair PNR. Pathogenese der apikalen Parodontitis und die Ursachen endodontischer Misserfolge. Crit Rev Oral Biol Med 2004;15:348 – 81.
- Spångberg L. Biologische Effekte von Wurzelkanalfüllmaterialien. Teil 7. Reaktion des Knochengewebes auf implantiertes Wurzelkanalfüllmaterial bei Meerschweinchen. Odontol Tidsk 1969;77:133–59.
- Stanley HR. Toxizitätstests von zahnärztlichen Materialien. Vereinigte Staaten: CRC Press, 1985.
- Zmener O, Banegas G, Pameijer CH. Reaktion des Knochengewebes auf ein methacrylatbasiertes endodontisches Versiegelungsmaterial: eine histologische und histometrische Studie. J Endod 2005;31:457–9.
- Stellungnahme zu posterioren harzbasierten Kompositen. ADA Rat für wissenschaftliche Angelegenheiten: ADA Rat für zahnärztliche Leistungsprogramme 1998;129:1627– 8.
- Tay FR, Loushine RJ, Weller RN, et al. Ultrastrukturelle Bewertung des apikalen Versiegelung in Wurzeln, die mit einem polycaprolactonbasierten Wurzelkanalfüllmaterial gefüllt sind. J Endod 2005;31:514 –9.
- Boiullaguet S, Wataha JC, Lockwood PE, Galgano C, Golay A, Krejci I. Zytotoxizität und Dichtheitseigenschaften von vier Klassen endodontischer Versiegler, bewertet durch die Aktivität der Succinatdehydrogenase und konfokale Laser-Scanning-Mikroskopie. Eur J Oral Sci 2004;112:182–7.
- Louw NP, Pameijer CH, Norval G. Histopathologische Bewertung eines Wurzelkanalversiegelers bei subhumanen Primaten [Abstract]. J Dent Res 2001;80:654
- Zmener O. Gewebereaktion auf einen neuen methacrylatbasierten Wurzelkanalversiegler: vorläufige Beobachtungen im subkutanen Bindegewebe von Ratten. J Endod 2004;30:348 –51.
- Zmener O, Pameijer CH. Klinische und radiographische Bewertung eines harzbasierten Wurzelkanalversiegelers. Am J Dent 2004;17:19 –22.
- Shipper G, Teixeira FB, Arnold RR, Trope M. Periapikale Entzündung nach koronalem mikrobiellen Inokulation von Hundewurzeln, die mit Guttapercha oder Resilon gefüllt sind. J Endod 2005;31:91– 6.
- Bergenholtz G, Spångberg L. Kontroversen in der Endodontie. Crit Rev Oral Biol Med 2004;15:99 –114.
- Fédération Dentaire Internationale. Empfohlene Standardpraktiken für die biologische Bewertung zahnärztlicher Materialien. Int Dent J 1980;30:174 – 6.
- Huang FM, Tsai CH, Yang SF, Chang YC. Induktion der Genexpression von Interleukin-6 und Interleukin-8 durch Wurzelkanalversiegler in menschlichen osteoblastischen Zellen. J Endod 2005;31:679 – 83.
- Lindgren P, Eriksson K-F, Ringberg A. Schwere Gesichtsischämie nach endodontischer Behandlung. J Oral Maxillofac Surg 2002;60:576 –9.
- Spångberg L, Pascon EA. Die Bedeutung der Materialvorbereitung für den Ausdruck der Zytotoxizität während der in vitro Bewertung von Biomaterialien. J Endod 1988;14:247–50.
- Cohen BI, Pagnillo MK, Musikant BL, Dentsch AS. Bewertung der Freisetzung von Formaldehyd für drei endodontische Füllmaterialien. Oral Health 1998;88:37–9.
- Leonardo MR, de Silva LAB, Filho MT, de Silva RS. Freisetzung von Formaldehyd durch 4 endodontische Versiegler. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 1999;88:221–5.
- Morgan KT, Gross EA, Patterson DL. Verteilung, Fortschritt und Erholung der akuten Formaldehyd-induzierten Hemmung der nasalen mukoziliären Funktion bei F-344 Ratten. Toxicol Appl Pharmacol 1983;86:161–76.
- Kaplan AE, Ormaechea MF, Picca M, Canzobre MC, Ubios AM. Rheologische Eigenschaften und Biokompatibilität von endodontischen Versiegelern. Int Endod J 2003;36:527–32.
- Di Felice R, Lombardi T. Gingivale und mandibuläre Knochennekrose verursacht durch eine paraformaldehydhaltige Paste. Endod Dent Traumatol 1998;14:196 – 8.
- Matsumoto K, Inoue K, Matsumoto A. Die Wirkung neu entwickelter Wurzelkanalversiegler auf Rattenzahnmarkzellen in Primärkultur. J Endod 1989;15:60 –7.
- Zmener O, Spielberg C, Lamberghini F, Rucci M. Dichtheitseigenschaften eines neuen epoxidharzbasierten Wurzelkanalversieglers. Int Endod J 1997;30:332– 4.
- Miletić I, Devčić N, Anić I, Borčić J, Karlović Z, Osmak M. Die Zytotoxizität von Roeko-Seal und AH Plus im Vergleich während verschiedener Aushärtezeiten. J Endod 2005;31:307–9.
- Zmener O, Pameijer CH. Klinische und radiographische Bewertung eines harzbasierten Wurzelkanalversiegelers. Am J Dent 2004;17:19 –22.
- Teixeira FB, Teixeira ECN, Thompson JY, Trope M. Bruchfestigkeit von Wurzeln, die mit einem neuen Harzfüllmaterial endodontisch behandelt wurden. J Am Dent Assoc 2004;135:646 –52.
- Shipper G, Trope M. In vitro mikrobielles Leckagen von endodontisch behandelten Zähnen unter Verwendung neuer und standardmäßiger Obturationsmethoden. J Endod 2004;30:154 – 8.
- Versiani MA, Carvalho-Júnior JR, Sasaki E, et al. Eine vergleichende Studie der physikochemischen Eigenschaften von AH Plus™ und Epiphany™ Wurzelkanalversiegelern. Int Endod J (in Druck).
- ANSI/ADA Spezifikation Nr. 57. Endodontisches Dichtungsmaterial. Washington: USA. 2000.
- Seux D, Couble ML, Hartmann DJ, Gauthier JP, Magloire H. Odontoblast-ähnliche Zytodifferenzierung des menschlichen Zahnmarkes ‘in vitro’ in Anwesenheit eines zementhaltigen Calciumhydroxids. Arch Oral Biol 1991;36:117–28.