Periimplantitis behandeln – geht das?
Implantate haben sich längst als Standardverfahren etabliert. Sowohl Patienten als auch Behandler schätzen ihren Wert und die Möglichkeit, vorhersagbar zahnlose Kieferareale zu versorgen. Neue Implantatoberflächen erlauben die Verwendung auch in kompromittierten Situationen mit kürzeren Einheilzeiten. Es scheint, als gäbe es kein Risiko. Überlebensraten deutlich über 95 Prozent werden als selbstverständlich angesehen. Ist es so einfach? Ist das Implantat ein risikoarmes Instrument für die Versorgung im zahnärztlichen Alltag? Survival rates sind nicht gleichzusetzen mit Success. Studien deuten darauf hin, dass bis zu 65 Prozent der Fälle von einer periimplantären Mukositis und 47 Prozent von einer Periimplantitis betroffen sind. Die frühe Therapie der periimplantären Mukositis und Vermeidung der Periimplantitis hat oberste Priorität.
Diagnosik
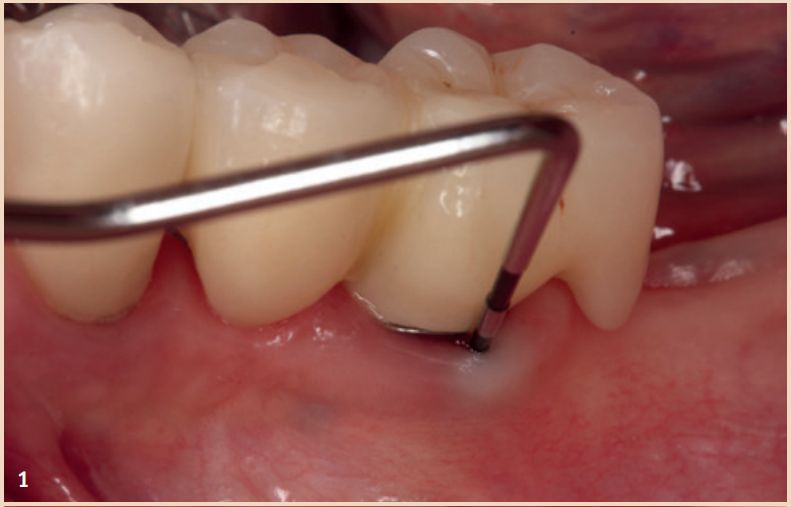
Für die Diagnostik der periimplantären Mukositis und der Periimplantitis sind lediglich eine Parodontalsonde und ein Einzelzahnfilm notwendig.
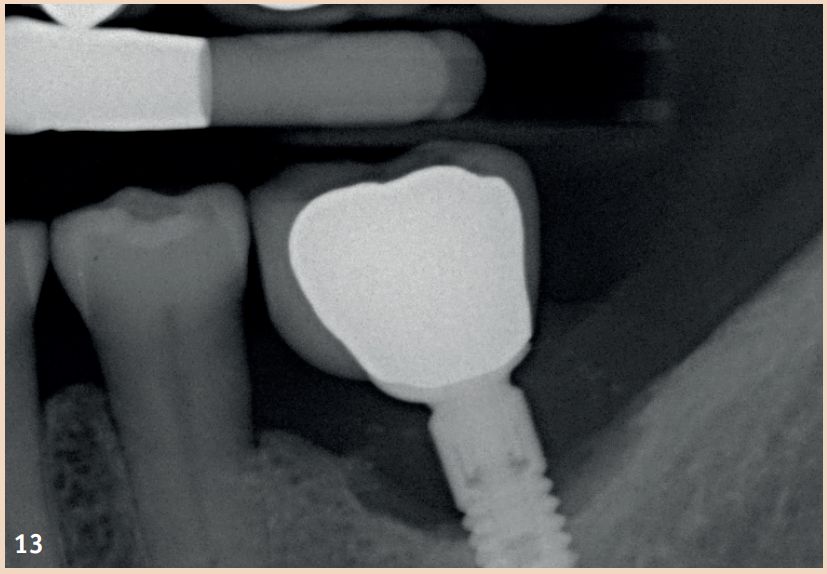
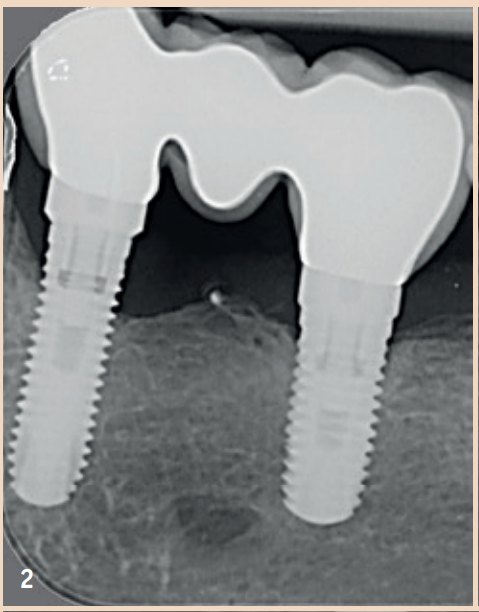
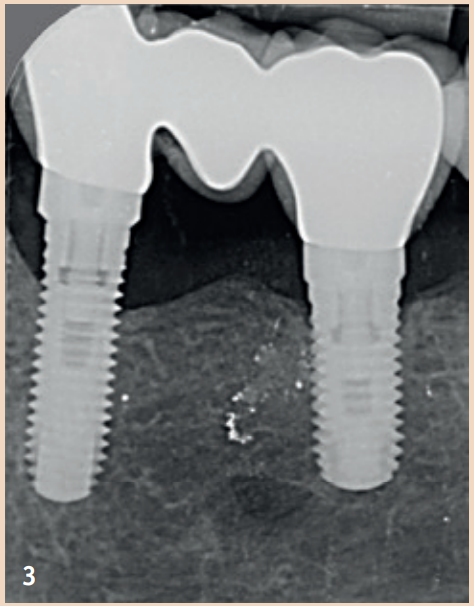
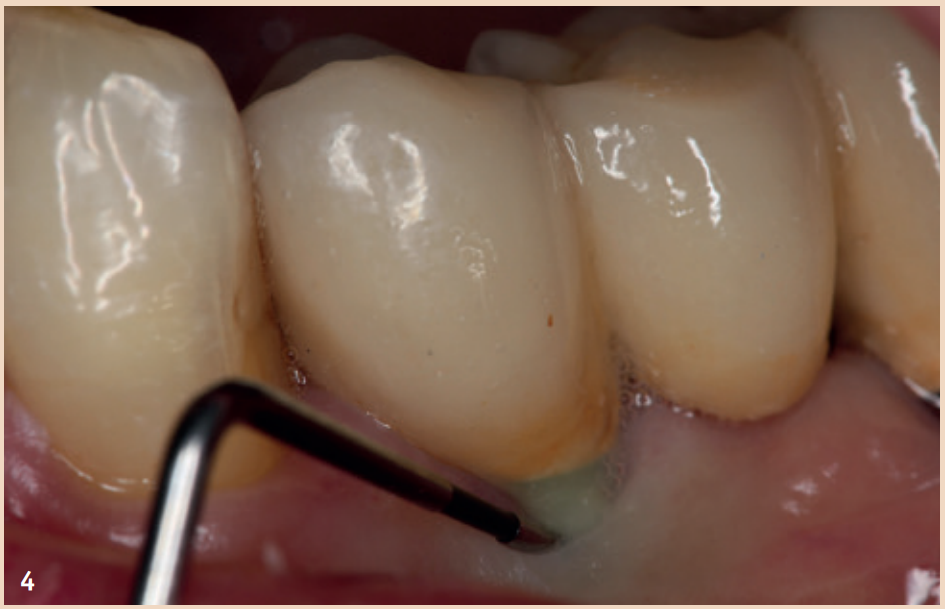
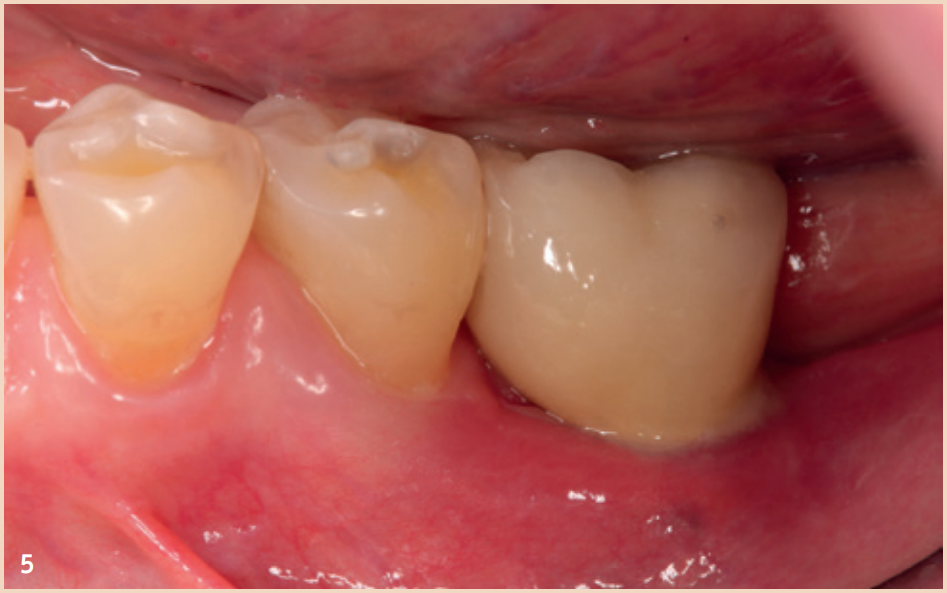
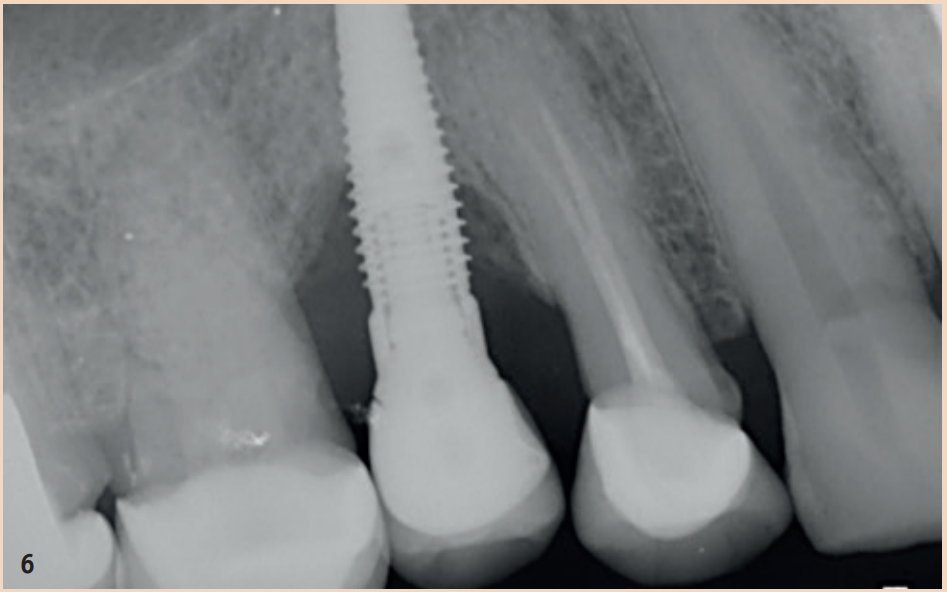
Die regelmässige Sondierung der periimplantären Sondierungstiefen nach der Einheilungsphase wird empfohlen. Hierbei sollte der Druck 0,25 N nicht übersteigen. Die Gefahr, durch den Sondierungsvorgang die Implantatoberfläche zu beschädigen, ist unbegründet, sodass herkömmliche Messsonden nicht durch spezielle Messsonden ersetzt werden müssen. Das frühzeitige Erkennen einer periimplantären Mukositis ist wichtig, da der Übergang zu einer Periimplantitis fliessend ist und das Stadium der Erkrankung aktuell mit keinem zur Verfügung stehenden Hilfsmittel bestimmt werden kann. Neben den Sondierungstiefen steht das Bleeding on Probing (BOP) im Fokus, welches dem Behandler einen ersten Einblick über den entzündlichen Zustand der Mukosa gibt. Während ein positives BOP mindestens für eine periimplantäre Mukositis spricht, ist eine Suppuration ein Zeichen für eine vorliegende Periimplantitis. Für den Knochenverlust sind in der Literatur Grenzwerte zwischen 0,4 mm und 5 mm angegeben, ab welchem von einer Periimplantitis gesprochen werden kann. Auch sind Fälle berichtet, in denen ein Knochenverlust von bis zu drei Schraubenwindungen nicht als Periimplantitis gewertet wurde, sondern noch in den Definitionsbereich der periimplantären Mukositis fiel. Diese knöchernen Umbauprozesse sind jedoch nur im Röntgenbild zu erkennen und je nach angefertigter Aufnahme auswertbar.
Allgemein empfohlen ist hier der Einzelzahnfilm, welcher in Rechtwinkeltechnik aufgenommen wird. Um die Umbauprozesse besser beurteilen zu können, wird empfohlen, neben einem Sondierungsbefund zum Zeitpunkt der Eingliederung des Zahnersatzes (ZE) auch ein Röntgenbild anzufertigen. Die Ausgangssituation kann so besser mit evtl. im Verlauf auftretenden Resorptionsgeschehen verglichen werden. Nicht jeder Verlust von Knochen um Implantate ist mit einer Periimplantitis gleichzusetzen. Vielmehr können auch physiologische Remodellationsvorgänge nach ZE-Versorgung dazu führen, dass Knochen verloren geht. Diese sind, verglichen mit einer Periimplantitis, nicht entzündlich und nicht progredient.
Prävalenz und Risikofaktoren
Ein systematischer Überblick der Epidemiologie periimplantärer Gesundheit und Erkrankungen aus dem Jahre 2015 befasste sich mit den postimplantologischen Komplikationen. Die Prävalenz der periimplantären Mukositis und Periimplantitis reichte, abhängig von verwendeten Falldefinitionen, von 19 bis 65 Prozent und von einem bis 47 Prozent. In folgenden Metaanalysen wurde der Prävalenzmittelwert für die periimplantäre Mukositis auf 43 (CI: 32–54 Prozent) und für die Periimplantitis auf 22 Prozent (CI: 14–30 Prozent) geschätzt.
Allgemeine Risikofaktoren
Da die Periimplantitis auf bakterielle „Plaque“ zurückzuführen ist, kommt insbesondere der Anheftungsmöglichkeit der Plaque an die Implantatoberfläche eine grosse Bedeutung zu. Es konnte nachgewiesen werden, dass sich auf glatten Implantatoberflächen weniger Biofilm anheftet. Darüber hinaus wurde in präklinischen Studien gezeigt, dass der Knochenverlust bei Implantaten mit polierten Oberflächen gegenüber rauen deutlich geringer war.
Als ein wesentlich beeinflussender Risikofaktor für die Entstehung der Periimplantitis wird das Rauchen angesehen.
Ob das Fehlen oder Vorhandensein einer attached/keratinisierten Gingiva als ein weiterer Risikofaktor für die Entstehung periimplantärer Erkrankungen eine Rolle spielt, wird wissenschaftlich kontrovers diskutiert. Es liegt eine Studie vor, in der keine signifikante Assoziation zwischen einer attached Gingiva und einer Periimplantitis nachgewiesen werden konnte. In einer anderen Studie konnte hingegen sowohl für eine Mukositits als auch für eine Periimplantitis ein erhöhtes Risiko bei dem Vorliegen von attached/keratinisierter Gingiva belegt werden. Einen weiteren Einfluss auf periimplantäre Erkrankungen könnte auch die Art der prothetischen Implantatversorgungen, festsitzend oder herausnehmbar, und der sogenannte Prosthetic Misfit bzw. „fehlerhafte Suprakonstruktion“ nehmen. Für beide Faktoren liegen noch keine wissenschaftlichen Er gebnisse vor. Zusätzlich wird die Hygienefähigkeit diskutiert. Serino und Ström (2009) haben festgestellt, dass Implantate mit nicht reinigungsfähigen Suprakonstruktionen häufiger von Periimplantitis betroffen waren.
Darüber hinaus konnte in der systematischen Übersicht von Derks und Tomasi (2015) eine positive Korrelation zwischen „Implantatalter“ und Periimplantitisprävalenz beschrieben.
Parodontitis als Risikofaktor
Eine Vielzahl von Studien nimmt den parodontalen Gesundheitszustand mit in die Befundung auf, sodass mögliche Assoziationen zwischen periimplantären Erkrankungen und einer Parodontitis festgestellt werden können.
Marrone et al. 2013 zeigten, dass Patienten mit einer aktiven Parodontitis anfällig für das Auftreten einer Periimplantitis sind.
Auch bei den Untersuchungen von Koldsland et al. 2011 und Ferreira et al. 2006 wurde eine positive Korrelation zwischen dem Vorliegen einer parodontalen Erkrankung und der Periimplantitis festgestellt.
Patienten mit parodontalen Erkrankungen zeigen ein statistisch signifikant höheres Risiko für periimplantäre Erkrankungen.
In einer Querschnittsstudie von Mir-Mari et al. aus dem Jahre 2012 wurde die Prävalenz periimplantärer Erkrankungen einer Patientengruppe, integriert in ein parodontales Nachsorgeprogramm, untersucht. Alle Probanden entstammten derselben privaten Praxis und das Nachsorgeprogramm enthielt kontinuierliche Neuvorstellungen alle drei bis sechs Monate.
Nach Abschluss der Untersuchungen konnte gezeigt werden, dass die Periimplantitisprävalenz bei Patienten einer privaten Praxis, mit parodontaler Nachbehandlung, zwischen 12 und 22 Prozent liegt. Bei nahezu 40 Prozent lag eine periimplantäre Mukositis vor. Diese Prävalenzwerte sind mit Ergebnissen, ermittelt aus universitären Klinikpatienten, vergleichbar.
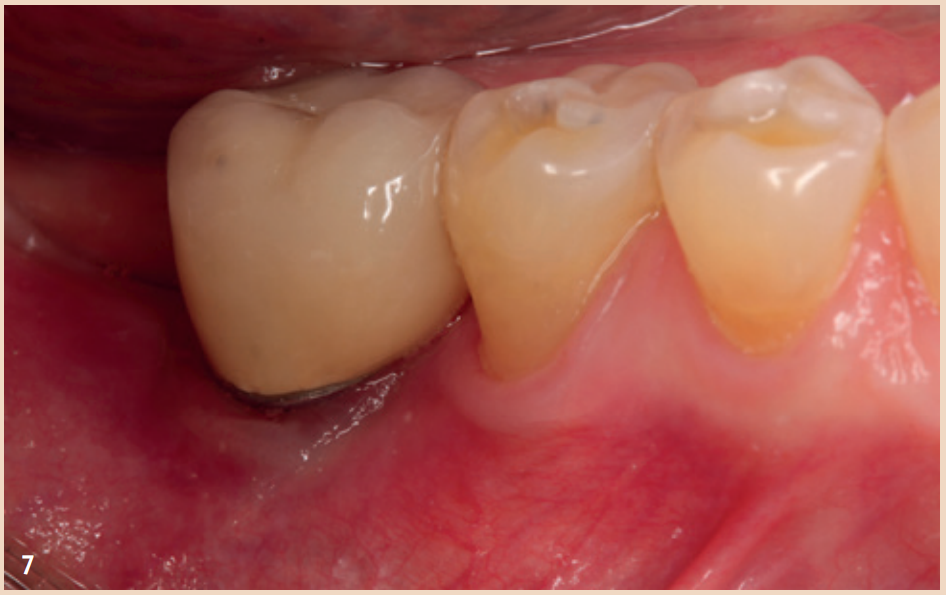
Therapie
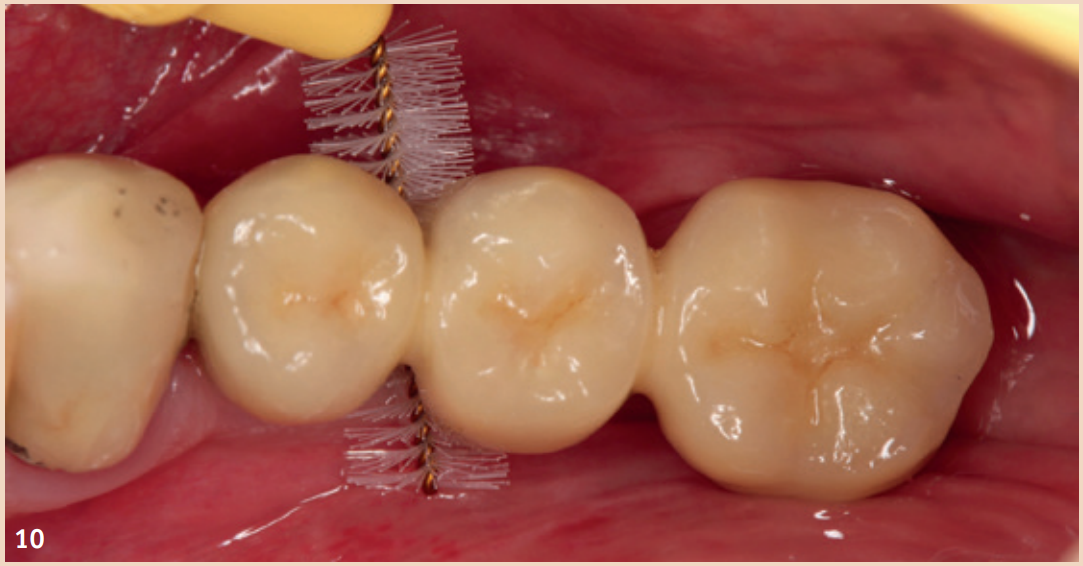
Auch wenn die Therapie der periimplantären Mukositis nicht in allen Fällen zu einer vollständigen Abheilung führt, ist sie besser und für den Patienten kostengünstiger durchführbar, sollte aber in kurzen Intervallen von drei Monaten nachkontrolliert werden. Die empfohlene Therapie beschränkt sich auf die regelmässige, systematische und professionell durchgeführte Plaqueentfernung und das Verbessern der häuslichen Mundhygiene. Ergänzende Hilfsmittel wie Spülungen, Salben mit verschiedenen Inhaltsstoffen, Antibiotika oder Laser haben keinen zusätzlichen Nutzen in der Behandlung einer periimplantären Mukositis. Rauchen sollte, wenn möglich, eingestellt und der ZE auf korrekten Sitz hin überprüft und wenn notwendig korrigiert werden. Die Therapie der Periimplantitis teilt sich in (1) nichtchirurgische Therapie und (2) chirurgische Therapie auf.
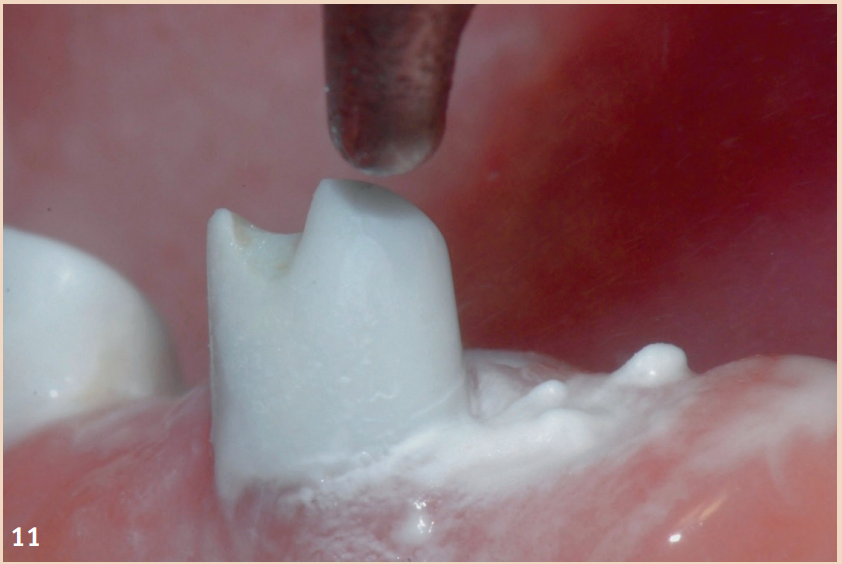
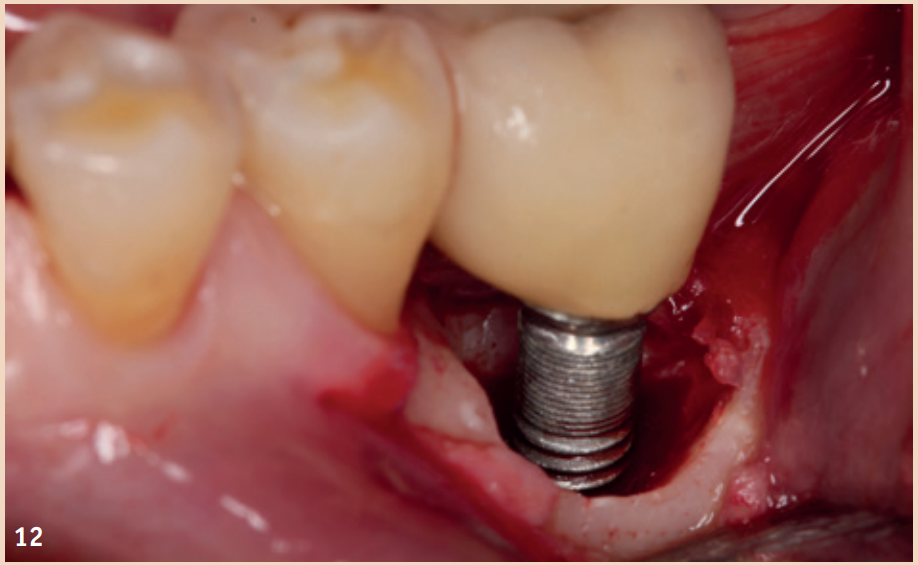
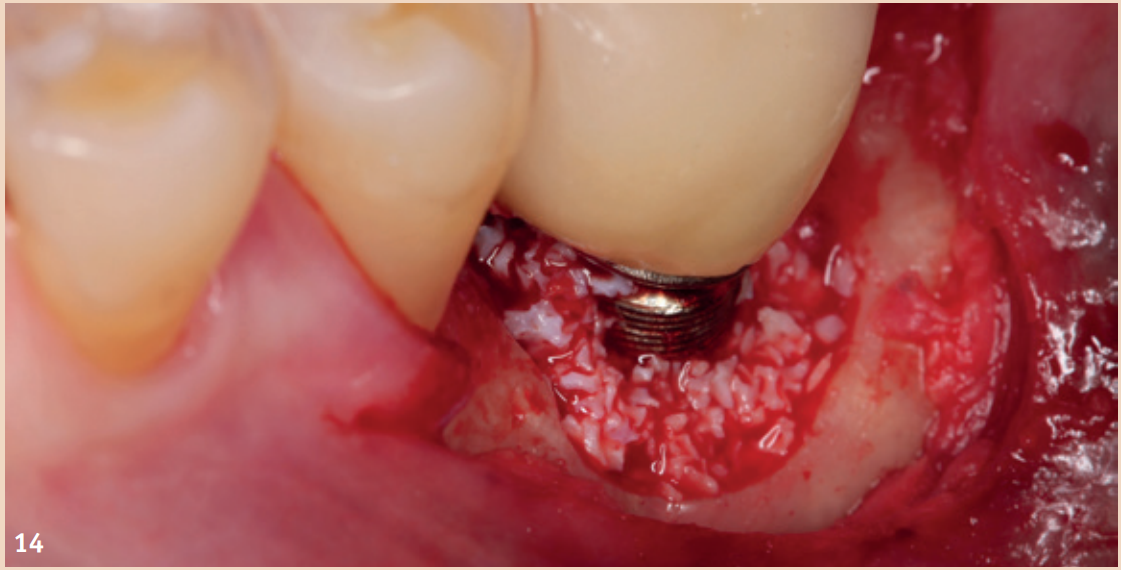
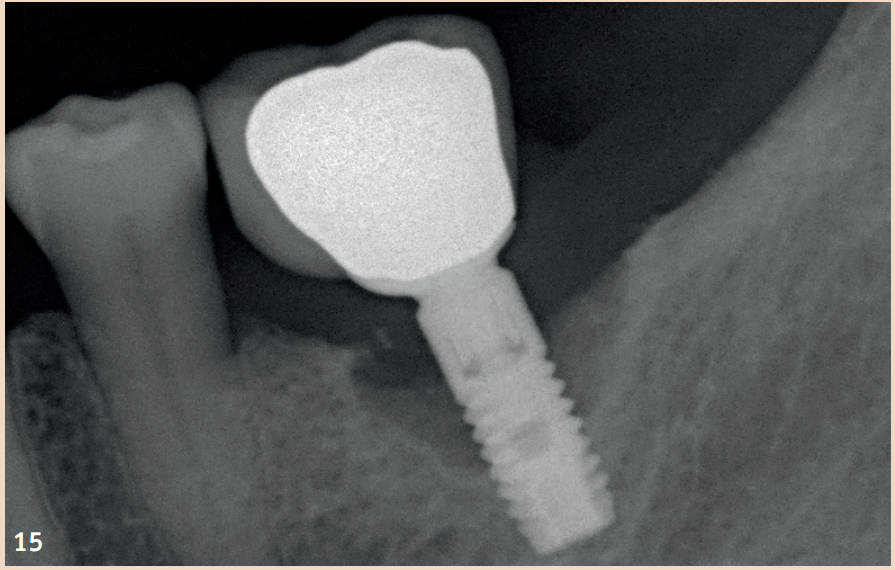
Während bei der periimplantären Mukositis adjuvante Massnahmen keinen zusätzlichen Nutzen brachten, sollten diese für die nichtchirurgische Therapie der Periimplantitis angewendet werden. Neben der Empfehlung von Pulver-Wasser-Strahlgeräten mit Glycin-Pulver zeigt auch der Er:YAG-Laser Vorteile hinsichtlich des Therapieerfolgs. Lokale Antibiotika (Doxycyclin) und CHX-Chips können ebenfalls als Adjuvantien empfohlen werden. Auch bei Vorliegen einer Periimplantitis sollte die Reduktion der Risikofaktoren (nicht passende ZE-Versorgung, Rauchen) nicht ausser Acht gelassen werden. Liegt bereits eine knöcherne Destruktion von mehr als 7 mm vor, ist ein Stopp der Progression (stabiles Ergebnis für mehr als sechs Monate) durch eine rein nichtchirurgische Therapie nicht wahrscheinlich. In diesen Fällen sollte eine frühzeitige chirurgische Therapie bevorzugt werden. Keiner der untersuchten chirurgischen Therapieansätze zeigte im direkten Vergleich einen Vorteil. Einigkeit besteht nur darin, dass das Granulationsgewebe vollständig entfernt werden sollte und die Reinigung der Implantatoberfläche eine zentrale Rolle spielt.
Die nach der Reinigung entstehenden Defekte können mit Knochenersatzmaterial aufgefüllt werden. Rezessionen sind dennoch sehr wahrscheinlich.
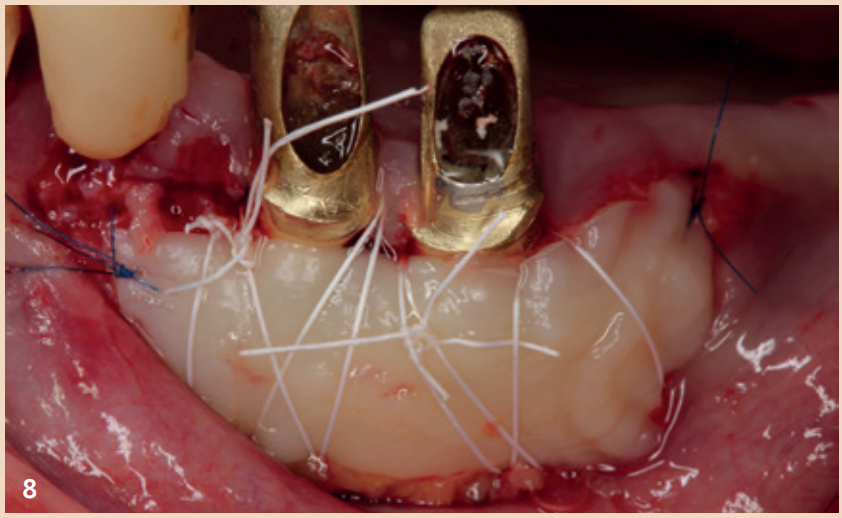
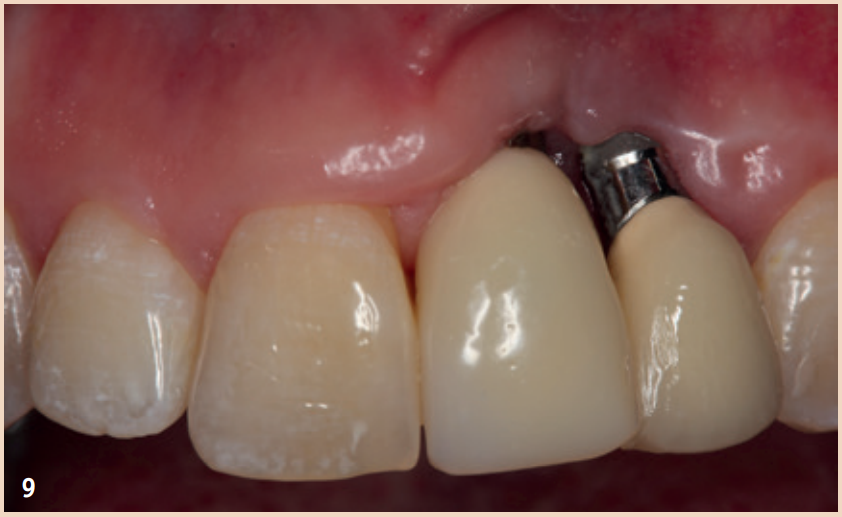
Ausblick
Die Forschung der vergangenen Jahre zeigt deutlich, wie unterschiedlich das Thema periimplantäre Mukositis und Periimplantitis definiert und beobachtet wird. Von einer unkontrollierbaren Welle der Periimplantitis kann aber nicht gesprochen werden und die Bedenken der vergangenen Jahre haben sich glücklicherweise nicht bestätigt. Um für die Behandler mehr Klarheit zu schaffen und ihnen bessere Protokolle für die Therapie der periimplantären Mukositis und Periimplantitis zu geben, besteht noch viel Forschungsbedarf. Ebenso muss das Verständnis bezogen auf Implantate und die sie umgebende Entzündung steigen. Die Implantation wird als einfache und sichere Methode angepriesen, zahnlose Kieferareale schnell mit festen Zähnen zu versorgen. Dem ist auch so, nur müssen die Rahmenbedingungen stimmen, um nachträgliche Eingriffe auf ein Minimum zu reduzieren. Implantate sind verglichen mit anderen Behandlungsmethoden ein noch junges Feld in der Zahnmedizin. Die Veränderung der Werkstoffe, die Oberflächenbeschaffenheit, die Art des Implantats (einteilig, mehrteilig), die Abutmentverbindung, ob der ZE zementiert oder verschraubt wurde, der ZE selbst, der Patient (Raucher, Diabetes, Mundhygiene etc.) und nicht zuletzt der Behandler haben Einfluss auf die Periimplantitiswahrscheinlichkeit. Wir müssen uns überraschen lassen, ob neuere Implantate aus Keramik oder die Behandlung periimplantärer Entzündungen mit Probiotika zu einer Reduktion des Risikos führen. Es bleibt spannend.
Fazit
Die periimplantäre Mukositis ist als Inflammation ohne Knochenverlust/reduziertes Knochenniveau definiert. Die vorliegende Entzündung betrifft die an das Implantat angrenzende Schleimhaut, wohingegen beim Vorliegen einer Periimplantitis die Inflammation mit einem Knochenverlust kombiniert ist. Als ätiologischer Faktor wird die „Plaque“ angegeben. Ähnlich der Gingivitis, welche eine Entzündung der marginalen Mundschleimhaut darstellt, führt Plaque zu einer Mukositis. Es wird angenommen, dass einige, jedoch nicht alle mukositären Veränderungen, in eine Periimplantitis übergehen.
Die Diagnosik erfolgt mithilfe einer Parodontalsonde und einer Röntgenaufnahme. Die regelmässige Kontrolle der periimplantären Sondierungstiefen nach der Einheilungsphase wird empfohlen. Hierbei sollte der Druck 0,25 N nicht übersteigen. Darüber hinaus sollte das Bleeding on Probing (BOP) ermittelt werden.
Die Prävalenz der periimplantären Mukositis und Periimplantitis erreicht in Studien, abhängig von verwendeten Falldefinitionen, Werte von 19 bis 65 Prozent und ein bis 47 Prozent. In folgenden Metaanalysen wurde der Prävalenzmittelwert für die periimplantäre Mukositis auf 43 und für die Periimplantitis auf 22 Prozent geschätzt.
Es konnte nachgewiesen werden, dass sich auf glatten Implantatoberflächen weniger Biofilm anheftet. In einer systematischen Literaturarbeit konnte ein deutlicher Zusammenhang zwischen dem Rauchen und den periimplantären Komplikationen beschrieben werden. Ob das Fehlen einer attached/ keratinisierten Gingiva ein möglicher Risikofaktor für die Entstehung periimplantärer Erkrankungen ist, wird wissenschaftlich kontrovers diskutiert. Es existieren sowohl Studien, die keinen Zusammenhang zwischen Parodontitis und Periimplantitis feststellen konnten, als auch Studien, die eine signifikante Assoziation beider Krankheiten zueinander zeigen. Es wird angeraten, Patienten mit Parodontitis über das mögliche erhöhte Risiko, an einer Periimplantitis zu erkranken, aufzuklären.
Das frühzeitige Erkennen und die anschliessende Therapie der periimplantären Mukositis ist das oberste Ziel in der Prävention der Periimplantitis. Die empfohlene Therapie für eine periimplantäre Mukositis beschränkt sich auf die regelmässige, systematische und professionell durchgeführte Plaqueentfernung und das Verbessern der häuslichen Mundhygiene. Während bei der periimplantären Mukositis adjuvante Massnahmen keinen zusätzlichen Nutzen brachten, sollte diese für die nichtchirurgische Therapie der Periimplantitis angewendet werden. Neben der Empfehlung von Pulver-Wasser-Strahlgeräten mit Glycin-Pulver zeigt auch der Er:YAG-Laser oder lokale Antibiotika (Doxycyclin) und CHX-Chips Vorteile hinsichtlich des Therapieerfolgs. Liegt bereits eine knöcherne Destruktion von mehr als sieben Millimetern vor, ist ein Stopp der Progression (stabiles Ergebnis für mehr als sechs Monate) durch eine rein nichtchirurgische Therapie nicht wahrscheinlich. In diesen Fällen sollte eine frühzeitige chirurgische Therapie bevorzugt werden. Ungeachtet der verschiedenen Operationsmethoden besteht Einigkeit darin, dass das Granulationsgewebe vollständig entfernt werden sollte und die Reinigung der Implantatoberfläche eine zentrale Rolle spielt.
Für die Zukunft besteht weiterhin viel Forschungsbedarf, um die Prävalenzraten der Periimplantitis stetig zu senken, die negative Beeinflussung der periimplantären Gesundheit durch Risikofaktoren zu ermitteln und neue Therapieansätze zur Behandlung der periimplantären Mukositis und Periimplantitis zu erlangen.