Semi-individualisierte dreidimensionale ultrafeine Titan-Maschen in der geführten Knochenregeneration für die Implantattherapie bei schweren alveolären Knochendefekten: ein Fallbericht
Maschinenübersetzung
Der Originalartikel ist in EN Sprache (Link zum Lesen) geschrieben.
Zusammenfassung
Dieser Fallbericht bietet eine detaillierte Beschreibung eines einfachen und schnellen Verfahrens zur Knochenregeneration unter Verwendung eines halbindividualisierten dreidimensionalen ultrafeinen Titannetzes. Ein 50-jähriger Mann mit einem schweren vertikalen und horizontalen Knochendefekt im anterioren Unterkiefer unterzog sich einer Implantatbehandlung in einem gestuften Ansatz. Der autologe Knochen wurde mit einem Xenograft kombiniert, und die Mischung wurde transplantiert, um den Knochendefekt zu augmentieren und mit halbindividualisierten ultrafeinen Titannetzen abgedeckt, die aus verschiedenen Typen entsprechend der Größe und Konfiguration des Knochendefekts ausgewählt, direkt verbunden und mit minimaler Formung an den Tenting-Schrauben fixiert wurden. Bei einer postoperativen Nachuntersuchung nach 6 Monaten wurde das durchgeführte Titannetz entfernt, Implantate wurden eingesetzt und eine Knochenkernbiopsie entnommen, die eine zufriedenstellende Neubildung von Knochen zeigte. Schließlich wurde zwei Monate später die definitive Prothese eingesetzt. Dieses halbindividualisierte ultrafeine Titannetz könnte einem Implantatkliniker helfen, vorhersehbarere Ergebnisse bei der geführten Knochenregeneration (GBR) zu erzielen.
Hintergrund
Die geführte Knochenregeneration (GBR) ist eine Technik, die verwendet wird, um einen Mangel an horizontalem und/oder vertikalem Alveolarknochen zu augmentieren. Es gibt mehrere wichtige Prinzipien für den Erfolg der GBR, einschließlich des Ausschlusses von epithelialem Gewebe, der Aufrechterhaltung des Transplantationsraums, der Stabilisierung eines Fibringerinnsels und der ungestörten Heilung durch spannungsfreien Wundverschluss. Um diese Prinzipien zu erreichen, sollten resorbierbare oder nicht-resorbierbare Barrieremembranen in GBR-Verfahren integriert werden. Eine resorbierbare Kollagenmembran ist einfach zu handhaben und erfordert keine zusätzliche Operation zur Entfernung, aber es ist schwierig, die genaue Abbau- oder Resorptionszeit vorherzusagen und einen größeren Transplantationsraum ohne Kollaps aufrechtzuerhalten. Im Gegensatz dazu erfordert eine nicht-resorbierbare Membran eine zusätzliche Operation zur Entfernung, zeigt jedoch im Allgemeinen ein besseres Ergebnis der Knochenregeneration, es sei denn, die Heilung wird durch Exposition unterbrochen.
Titanmesh ist eine repräsentative Art von nicht-resorbierbarer Membran, die durch ihre inhärente Steifigkeit gekennzeichnet ist und eine zufriedenstellende Knochenregeneration in großen Defekten erzeugt. Allerdings könnte die Knochenregeneration mit Titanmesh durch Exposition kompliziert werden, die häufig aus scharfen Punkten und Winkeln resultiert, die beim Schneiden, Biegen und Trimmen entstehen, um das Titanmesh an den transplantierten Knochen anzupassen. Darüber hinaus sind solche Transplantate anfällig für postoperative Infektionen. Der Begriff „halbkundenspezifisch“ wird in dieser Studie verwendet, da die Titanm meshes nicht vollständig mit CAD/CAM angepasst sind. Stattdessen kann der Kliniker aus einer Reihe von Standardnetzen auswählen, die in verschiedenen Größen und Konfigurationen für die Knochendefekte jedes Patienten verfügbar sind. In diesem Fallbericht beschreiben wir ein einfaches und schnelles GBR-Verfahren, das halbkundenspezifische ultrafeine Titanm meshes zur Anwendung bei einem großen Knochendefekt verwendet.
Fallpräsentation
Patienten und chirurgisches Verfahren
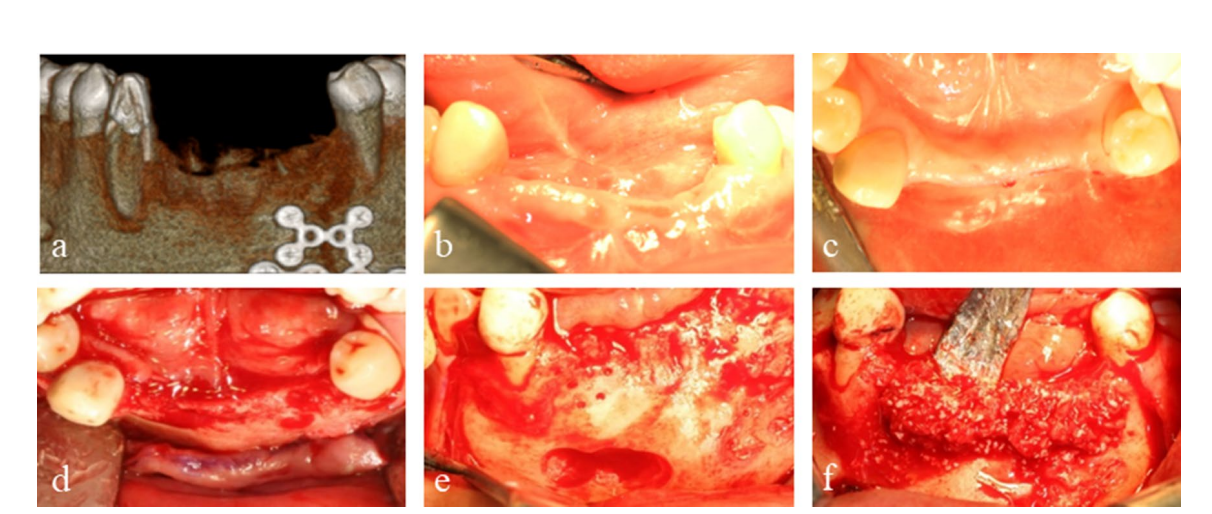
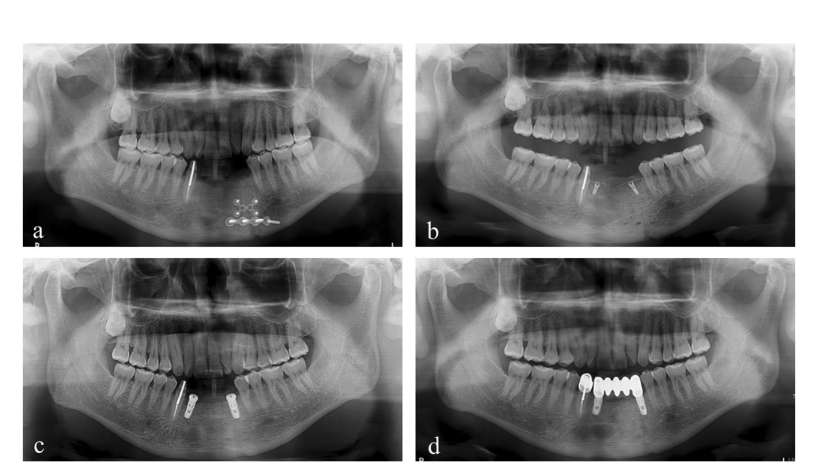
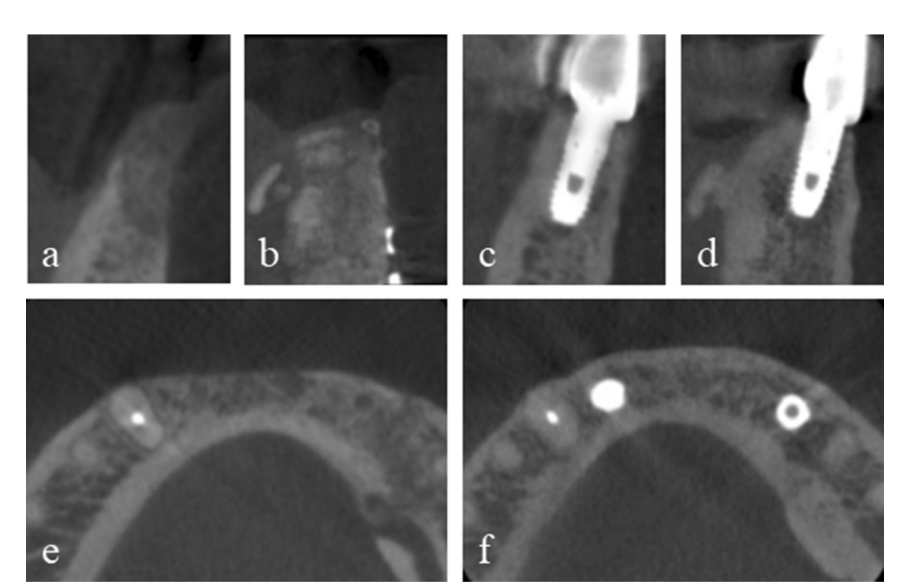
Ein 50-jähriger Mann mit einem kombinierten vertikalen und horizontalen Alveolarknochendefekt im anterioren Unterkiefer aufgrund früherer Gesichtsverletzungen wurde zur Implantatbehandlung überwiesen. Seine medizinische Vorgeschichte umfasste eine offene Reposition und interne Fixierung einer komplizierten Unterkieferfraktur, die durch einen Verkehrsunfall verursacht wurde. Der linke mandibuläre seitliche Schneidezahn und der Eckzahn wurden zusammen mit der Alveolarknochenfraktur avulsiert, und der linke mandibuläre zentrale Schneidezahn sowie der rechte mandibuläre zentrale Schneidezahn und seitliche Schneidezahn wurden während der Frakturoperation extrahiert. Eine Kronenfraktur des rechten mandibulären Eckzahns wurde nach einer Wurzelkanalbehandlung mit Stift und Kern rekonstruiert. Bei der präoperativen Bewertung mit Cone-Beam-Computertomographie (CBCT) wurde der Defekt im anterioren Unterkieferbereich auf etwa 7 mm vertikal und 5 mm horizontal gemessen (Abb. 1a).
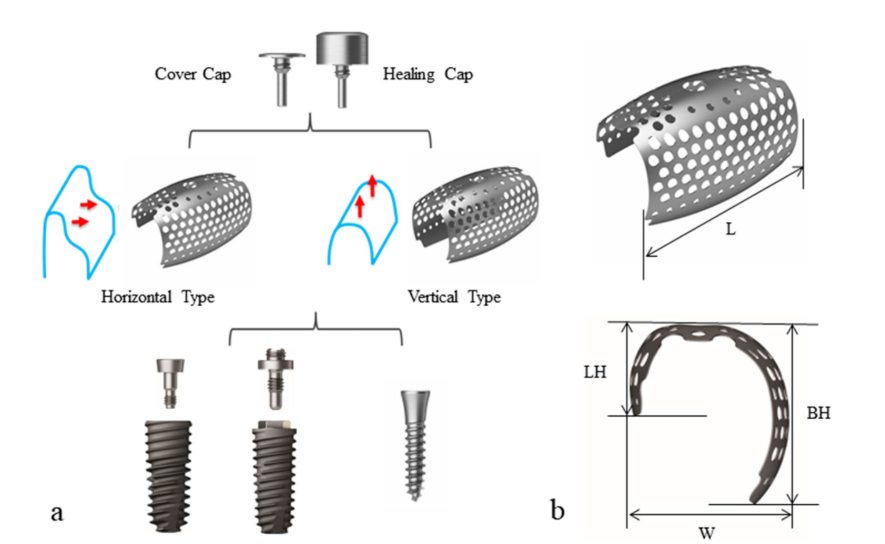
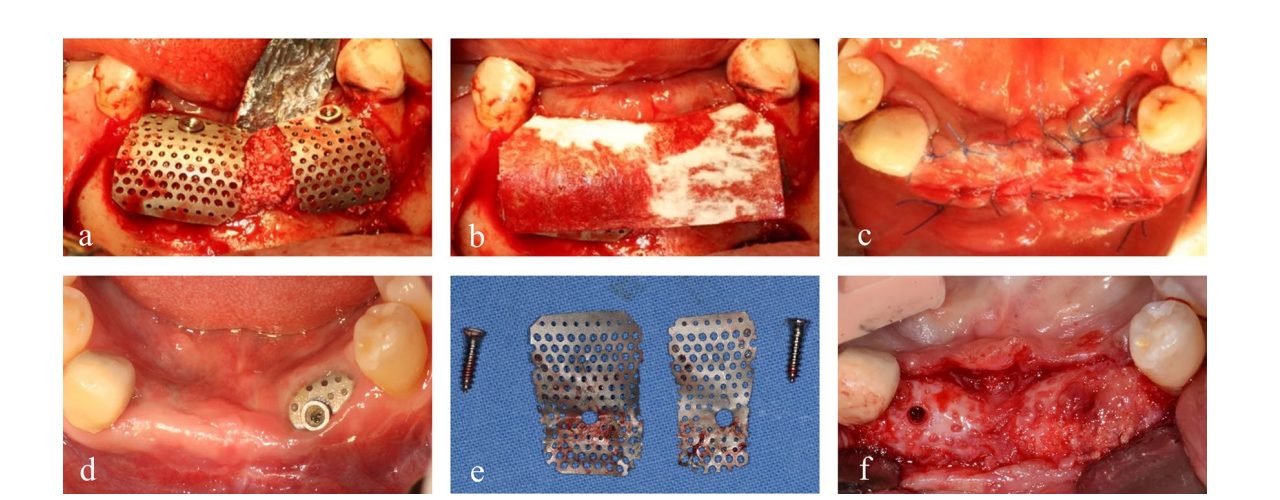
Der Patient gab seine informierte Zustimmung, und eine gestufte Knochenaugmentation wurde zur Implantatplatzierung durchgeführt. Nach der Infiltration von 2% Lidocain mit 1:100.000 Epinephrin wurde ein mittlerer Krestalschnitt mit zwei vertikalen Schnitten von dem linken mandibulären ersten Prämolaren bis zum rechten ersten Prämolaren durchgeführt, und ein vollschichtiges mukoperiostales Lappen wurde reflektiert. Die Platten und Schrauben aus der vorherigen Frakturoperation wurden entfernt. Zwei Tentierungsschrauben wurden an den optimalen Positionen der nachfolgenden Implantate eingesetzt, und die Größe und Konfiguration des Knochenfehlers, die präoperativ durch CBCT beurteilt worden waren, wurden klinisch bestätigt und sorgfältig gemessen. Das autologe Knochenmaterial, das von der Stelle der Platten und Schrauben entnommen und mit einem speziellen Trepanbohrer (Autobone Collector, Osstem, Republik Korea) partikuliert wurde, wurde im Verhältnis 1:1 mit einem Xenograft (A-Oss, Osstem) gemischt und zur Augmentation des vertikalen und horizontalen Knochenfehlers um die Tentierungsschrauben transplantiert (Abb. 1b–f). Zwei halbkundenspezifische ultrafeine Titannetze (OssBuilder, Osstem), als horizontale Typen mit den Abmessungen Länge 10 mm, Breite 9 mm, buccale Höhe 11 mm und linguale Höhe 5,5 mm, wurden speziell aus verschiedenen verfügbaren Untergruppen ausgewählt (Abb. 2). Diese Titannetze wurden angepasst, um den transplantierten Bereich durch minimale Schnitte und Modellierungen abzudecken und mit Abdeckkappen immobilisiert. Eine resorbierbare Kollagenmembran (Oss-Mem hard, Osstem) wurde über die Titannetze gelegt, um eine vorzeitige Verdünnung des darüber liegenden Zahnfleisches zu minimieren. Schließlich wurde eine spannungsfreie primäre Verschlussnaht mit einem Freischnitt am buccalen Periost durchgeführt (Abb. 3a–c).
Der Patient erhielt orale Antibiotika und Analgetika und wurde angewiesen, eine 0,12%ige Chlorhexidin-Gluconat-Lösung für 10 Tage zu verwenden.
Ergebnisse
Außer einer kleinen Exposition des halbkundenspezifischen ultrafeinen Titangewebes an der Position des linken mandibulären Caninus gab es keine Komplikationen. Die Expositionsgröße nahm stetig bis auf etwa
5 mm im Durchmesser zu. Die Gewebe um die Exposition waren rötlich gefärbt, zeigten jedoch keine negativen Anzeichen oder Entzündungen. Sechs Monate später wurde eine Wiedereröffnung unter örtlicher Betäubung durchgeführt und die Titangewebe wurden entfernt. Die makroskopische Untersuchung ergab regeneriertes Knochengewebe, das kortikalisiert war und mit einem dünnen Pseudoperiost ausgekleidet war. In dem Bereich, in dem das Titangewebe exponiert war, war jedoch ein dickeres Pseudoperiost vorhanden, das mit rohen Partikeln des Xenografts vermischt war. Dieses Pseudoperiost löste sich während des Implantatbohrens leicht vom darunterliegenden regenerierten Knochen (Abb. 3d–f).
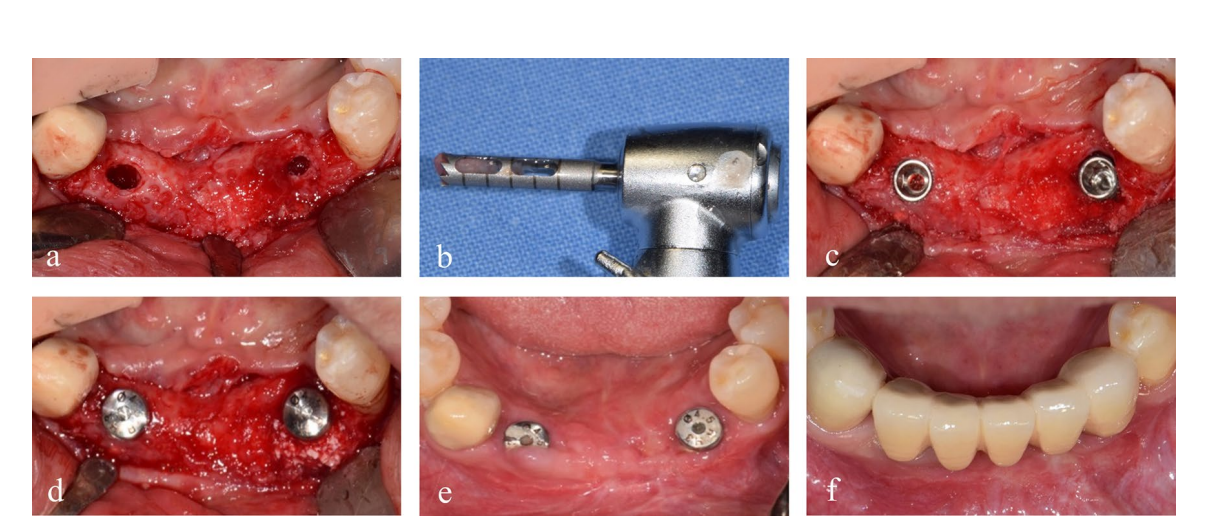
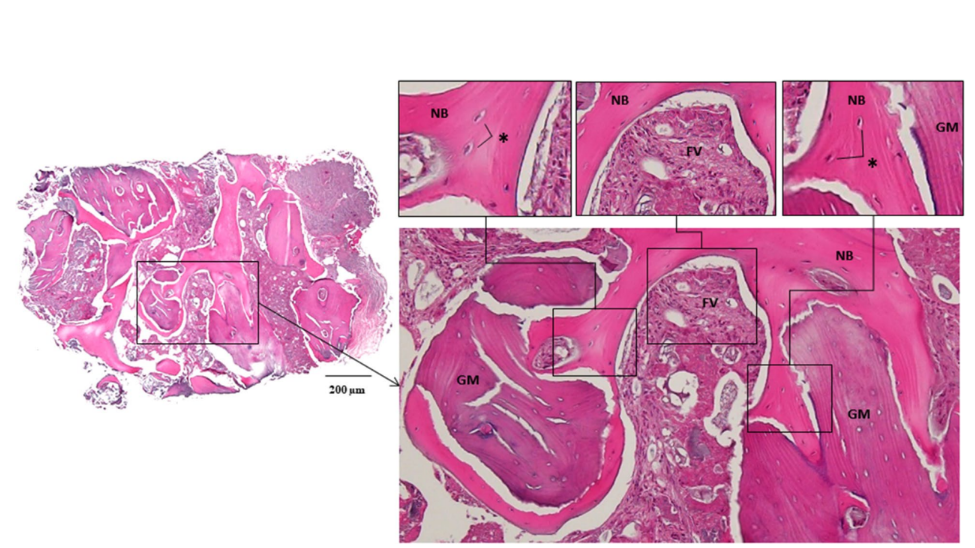
Zwei 4,0 × 10 mm Implantatbefestigungen (TS III SOI, Osstem) wurden im regenerierten Knochen des linken mandibulären Caninus und des rechten seitlichen Schneidezahns mit einem Sitzdrehmoment von über 30 Ncm platziert. Anschließend wurden zwei 5,0 × 3 mm Heilungsabutments verbunden. Vor dem Implantatbohren im Bereich des linken mandibulären Caninus wurde ein Knochenkern für die histologische Analyse mit einem 2,0 mm Durchmesser Trepanbohrer entnommen (Abb. 4). Die Schnitte wurden mit Hämatoxylin und Eosin (H&E) gefärbt und mit einem Lichtmikroskop beobachtet (Abb. 5). Die Bereiche des neuen Knochens, des verbleibenden Transplantatmaterials und des fibrovasculären Gewebes wurden unterteilt, und ihre relativen Prozentsätze wurden gemessen. Zwei Monate später wurden die Abformung und die Lieferung der definitiven Zirkonrestauration durchgeführt. Die postoperative panoramische Röntgenaufnahme zeigte ein stabiles peri-implantäres Knochenniveau und bemerkenswerterweise äußerte der Patient Zufriedenheit mit dem Endergebnis (Abb. 6 & 7).
Diskussion
In Fällen von kombinierten schweren horizontalen und vertikalen Knochendefekten sollte eine Knochenaugmentation vor der Implantation durchgeführt werden. Während dieses schrittweisen Behandlungsansatzes kann die Stabilität des Knochenaugmentationsraums durch routinemäßige Ereignisse in der Mundhöhle, wie Kauen und Sprechen, gestört werden. Daher wird, wenn ein Patient eine erhebliche Menge an Knochenmaterial benötigt, Titanmesh als die am besten geeignete nicht resorbierbare Barrieremembran angesehen, um die Form und das Volumen des Knochenmaterials aufrechtzuerhalten, da es als leichtes Metall steif und kosteneffektiv ist. Im Vergleich zu den Mikroporen anderer Barrieremembranen ist Titanmesh einzigartig, da es Makroporen hat, die Zellen nicht selektiv blockieren oder passieren lassen. Aufgrund seiner Biokompatibilität und der Stabilisierung von Blutgerinnseln wurde Titanmesh auch in der Mund- und Kieferchirurgie weit verbreitet eingesetzt.
Obwohl Titanmesh flexibel und glatt strukturiert ist, hat es einen entscheidenden Nachteil der Exposition, die meist nicht wieder von der Gingiva bedeckt wird. Die Inzidenz der Exposition, die mit Titanmesh verbunden ist, wurde mit 16 bis 34 % angegeben. Seine Steifheit ist vorteilhaft für die Aufrechterhaltung des Augmentationsraums, führt jedoch häufig zu einer Verdünnung der darüber liegenden Mukosa während der Wundkontraktion in der Heilungsphase. Darüber hinaus ist die Verwendung von Titanmesh als Barrieremembran ein sehr technikempfindlicher Eingriff, da es geformt und starr fixiert werden sollte. Während dieses Formungsprozesses könnten die scharfen Punkte und Winkel, die durch Schneiden, Biegen und Trimmen des Titanmesh entstehen, zu seiner Exposition durch die Gingiva beitragen.
Anders als bei einer herkömmlichen Titanmascheplatte kann eine halbkundenspezifische ultrafeine Titanmasche einfach angepasst werden, indem man die am besten geeignete unter den verschiedenen Typen und Untertypen entsprechend der Größe und Konfiguration des Knochendefekts auswählt. Dadurch kann sie einfach und schnell verwendet werden, da die Anpassung minimale Modifikationen ermöglicht und scharfe Punkte und Winkel während der routinemäßigen Formgebung eliminiert. Im Allgemeinen wird die halbkundenspezifische ultrafeine Titanmasche ausgewählt, indem der Typ, die Länge, die Breite und die Höhe des peri-implantären Knochendefekts mit einer Parodontalsonde oder einem Implantat-Tiefenmessgerät genau beurteilt und direkt mit dem Implantat verbunden wird, sodass eine spezifische und effiziente Knochenaugmentation für das optimale Ergebnis durchgeführt werden kann. Darüber hinaus wird eine starre Fixierung und stabile Immobilisierung ebenfalls einfach und schnell erreicht. Angesichts der Tatsache, dass der 3D-Druck einer patientenspezifischen Titanmasche basierend auf einem präoperativen CBCT-Datensatz teuer ist und einen komplizierten digitalen Workflow erfordert, ist diese halbkundenspezifische ultrafeine Titanmasche kosteneffektiv und sofort einsatzbereit, wie eine fertiggestellte Titanmasche. Falls erforderlich, kann diese halbkundenspezifische ultrafeine Titanmasche durch minimale Zuschnitte und Biegungen für eine bessere Anpassung an einen Knochendefekt modifiziert werden. Darüber hinaus waren die in diesem Fall verwendete Titanmasche und ihre Komponenten vielseitig und erweiterten ihre Anwendbarkeit auf Implantate mit internen und externen Verbindungen von anderen Herstellern.
Das halbkundenspezifische dreidimensionale ultrafeine Titannetz besteht aus Titan der Klasse 2, das kommerziell rein ist, mit einer Dicke von 0,1 mm. Es hat drei Poren mit unterschiedlichen Größen; 1,0 mm um das Implantat, 0,6 mm an der Erweiterung und 0,5 mm an den Seiten des Titannetzes. Mit den 1,0 mm Poren kann eine angemessene Blutversorgung und Diffusion von Wachstumsfaktoren zur Förderung der Heilung bereitgestellt werden. Die 0,6 mm Poren ermöglichen ebenfalls eine ausreichende Blutversorgung und können verhindern, dass das Knochenersatzmaterial migriert. Darüber hinaus hat das halbkundenspezifische ultrafeine Titannetz 0,5 mm Poren an seinen Seiten, die dazu entworfen wurden, die mechanische Steifigkeit während der Formgebung zu erhalten.
Autologes Knochenmaterial, der Goldstandard für Knochenersatzmaterial aufgrund seiner osteogenen Wirkung, wurde entnommen, partikuliert und im vorliegenden Fall verwendet. Kortiko-spongiöses Knochenmaterial wurde für den volumenhaltenden Effekt des harten kortikalen Knochens und den pluripotentialen Effekt des lockeren spongiösen Knochens verwendet. Häufige intraorale Stellen zur Entnahme von autologem Knochen sind die mandibuläre Symphyse, die maxilläre Tuberositas, der Ramus, Tori oder Exostosen. In unserem Fall war der Operationsort der vordere Mandibularbereich, daher wurde autologes Knochenmaterial aus der Mandibularsymphyse mit einer kleinen Erweiterung der Klappenreflexion entnommen, was keinen zusätzlichen chirurgischen Ort erforderte. Die Reduzierung der Anzahl der chirurgischen Stellen hat die Vorteile einer schnellen Genesung und weniger Komplikationen. Darüber hinaus wurde ein bovines Xenograft, das während der Osteokonduktion wenig oder keine Resorption zeigte, mit dem autologen Knochenmaterial gemischt. In der histomorphometrischen Analyse zeigte die Entfernung der halbkundenspezifischen ultrafeinen Titannetze eine erfolgreiche Knochenregeneration, die mit einem dünnen Pseudoperiost ausgekleidet war. Histologisch wurde gemessen, dass es aus 36,6 % neuem Knochen, 36,0 % restlichem Transplantatmaterial und 27,4 % fibrovasculärem Gewebe bei der Wiederöffnung bestand (Abb. 5).
Allerdings war im Bereich der Exposition des Titannetzes das Pseudoperiost viel dicker, und die Qualität des darunter liegenden regenerierten Knochens war so schlecht, dass der regenerierte Knochen dem Implantatbohren nicht standhalten konnte und abbrach, sodass ein zusätzliches Xenograft erforderlich war, um die zwei exponierten Gewinde des Implantatkopfes zu bedecken. Eine frühere Studie zeigte ebenfalls, dass es möglich war, das Titannetz nach der Exposition an Ort und Stelle zu lassen, obwohl im exponierten Bereich weniger regenerativer Knochen gefunden wurde. Die Anwendung einer resorbierbaren Kollagenmembran über dem Titannetz, wie in diesem Fall, ist derzeit umstritten. Unser Ziel war es, die Zellverschlussfähigkeit zu fördern und eine vorzeitige Verdünnung des darüber liegenden Zahnfleisches zu verhindern, indem eine klare Trennung zwischen den Kompartimenten für sowohl knöcherne als auch epitheliale Regeneration geschaffen wurde.
Fazit
Zusammenfassend zeigt der vorliegende Fall, dass GBR einfach und schnell mit einem halbindividualisierten ultrafeinen Titannetz durchgeführt werden kann. Das halbindividualisierte ultrafeine Titannetz sollte entsprechend der Größe und Konfiguration des Knochendefekts richtig ausgewählt und dann mit dem Implantatbefestigungselement oder dem Zelt-Schraube verbunden und immobilisiert werden. Dieses halbindividualisierte ultrafeine Titannetz könnte einem Implantatkliniker helfen, vorhersehbarere Ergebnisse bei der GBR für schwere horizontale und vertikale alveoläre Knochendefekte zu erzielen.
Dae‑Ho Park, Jong‑Hun Jun, Seo‑Hyoung Yun, Baek‑Sun Choi, Joseph P. Fiorellini, Marco Tallarico, Kyung‑Gyun Hwang und Chang‑Joo Park
Referenzen
- Liu J, Kerns DG. Suppl 1: Mechanismen der geführten Knochenregeneration: eine Übersicht. Open Dent J. 2014;8:56.
- Wang H‑L, Boyapati L. „PASS“-Prinzipien für vorhersehbare Knochenregeneration. Implant Dent. 2006;15(1):8–17.
- Dahlin C, Linde A, Gottlow J, Nyman S. Heilung von Knochendefekten durch geführte Geweberegeneration. Plast Reconstr Surg. 1988;81(5):672–6.
- Dahlin C, Sennerby L, Lekholm U, Linde A, Nyman S. Bildung neuen Knochens um Titanimplantate mit einer Membrantechnik: eine experimentelle Studie an Kaninchen. Int J Oral Maxillofac Implants. 1989;4(1):19–25.
- Becker W. Geführte Geweberegeneration für Implantate, die in Extraktionssocket platziert werden, und für Implantatdehiszenzen: chirurgische Techniken und Fallberichte. Int J Periodont Rest Dent. 1990;10:377–91.
- Becker W. Knochenbildung an dehiszierten Zahnimplantatstandorten, die mit Implantat-Augmentationsmaterial behandelt wurden: eine Pilotstudie an Hunden. Int J Periodont Rest Dent. 1990;10:93–101.
- Rakhmatia YD, Ayukawa Y, Furuhashi A, Koyano K. Aktuelle Barrieremembranen: Titanmesh und andere Membranen für die geführte Knochenregeneration in zahnmedizinischen Anwendungen. J Prosthodont Res. 2013;57(1):3–14.
- Tallarico M, Ceruso FM, Muzzi L, Meloni SM, Kim Y‑J, Gargari M, et al. Wirkung der gleichzeitigen sofortigen Implantation und geführten Knochenrekonstruktion mit ultrafeinen Titanmesh-Membranen auf radiographische und klinische Parameter nach 18 Monaten Belastung. Materials. 2019;12(10):1710.
- Jovanovic SA, Nevins M. Knochenbildung unter Verwendung von titanverstärkten Barrieremembranen. Int J Periodontics Restorative Dent. 1995;15(1):56–69.
- Malchiodi L, Scarano A, Quaranta M, Piattelli A. Starre Fixierung mittels Titanmesh bei der Erweiterung des zahnlosen Knochens zur horizontalen Knochenausweitung im Oberkiefer. Int J Oral Maxillofac Implants. 1998;13(5):701–5.
- Barboza E, Caúla A, Machado F. Potenzial von rekombinantem menschlichem Knochen-morphogenetischem Protein-2 in der Knochenregeneration. Implant Dent. 1999;8(4):360–7.
- dal Polo MR, Poli PP, Rancitelli D, Beretta M, Maiorana C. Rekonstruktion des Alveolarkamms mit Titanmesh: eine systematische Übersicht der Literatur. Med Oral Patol Oral Cir Bucal. 2014;19(6): e639.
- Hartmann A, Seiler M. Minimierung des Risikos von Expositionen benutzerdefinierter Titanmesh - eine retrospektive Analyse. BMC Oral Health. 2020;20(1):1–9.
- Wang EA, Rosen V, D’Alessandro JS, Bauduy M, Cordes P, Harada T, et al. Rekombinantes menschliches Knochen-morphogenetisches Protein induziert Knochenbildung. Proc Natl Acad Sci. 1990;87(6):2220–4.
- Toriumi DM, Kotler HS, Luxenberg DP, Holtrop ME, Wang EA. Mandibuläre Rekonstruktion mit einem rekombinanten knocheninduzierenden Faktor: funktionelle, histologische und biomechanische Bewertung. Arch Otolaryngol‑Head Neck Surg. 1991;117(10):1101–12.
- de Faria ABC, Chiantia FB, Teixeira ML, Aloise AC, Pelegrine AA. Vergleichsstudie zwischen mesenchymalen Stammzellen aus Knochenmark und aus Fettgewebe, in Verbindung mit Xenotransplantaten, bei appositionalen Rekonstruktionen: histomorphometrische Studie an Kaninchenkalvarien. Int J Oral Maxillofac Implants. 2016;31(6):e155–61.
- Proussaefs P. Klinische und histologische Bewertung der Verwendung von mandibulären Tori als Entnahmestelle für mandibuläre Blockautotransplantate: Bericht über drei Fälle. Int J Periodontics Restorative Dent. 2006;26(1):43–51.
- Her S, Kang T, Fien MJ. Titanmesh als Alternative zu einer Membran für die Knochenausweitung. J Oral Maxillofac Surg. 2012;70(4):803–10.
- Lim J, Jun SH, Tallarico M, Park JB, Park DH, Hwang KG, Park CJ. Eine randomisierte kontrollierte Studie zur geführten Knochenregeneration bei peri-implantären Dehiszenzdefekten mit zwei anorganischen bovinen Knochenmaterialien, die mit Titanmesh abgedeckt sind. Materials. 2022;15(15):5294.
