Behandlungsresultate von Zahnimplantaten bei Patienten unter aktiver Therapie mit Alendronat: 3-Jahres-Nachbeobachtungsresultate einer multizentrischen prospektiven Beobachtungsstudie
Maschinenübersetzung
Der Originalartikel ist in EN Sprache (Link zum Lesen) geschrieben.
Zusammenfassung
Ziel: Bewertung der 3-jährigen klinischen und radiografischen Daten von festen implantatgetragenen Zahnprothesen, die an Patienten geliefert wurden, die mindestens 3 Jahre lang wöchentlich 35–70 mg Alendronat eingenommen hatten, bevor die Implantation erfolgte.
Materialien und Methoden: Vierzig aufeinanderfolgende Patienten, die mit oralen Bisphosphonaten behandelt wurden und eine implantatgestützte Restauration benötigten, wurden zwischen Januar 2008 und Dezember 2011 in zwei privaten Zentren rekrutiert. Die Implantate wurden minimalinvasiv unter antibakterieller und antibiotischer Behandlung 6 Monate nach dem Absetzen der Alendronat-Gabe eingesetzt. Nach 4 Monaten der submukösen Heilung wurden die Implantate prothetisch belastet. Die Hygieneerhaltung und klinischen Bewertungen wurden alle 4 Monate über 3 Jahre geplant. Die Ergebnisparameter waren folgende: Implantat- und Prothesenerfolg, Überlebensraten, beobachtete klinische Komplikationen, marginale Knochenremodellierung, Sondierungstiefen und Blutung bei der Sondierung.
Ergebnisse: Am Ende der Studie brachen acht Patienten ab. Die endgültige Stichprobengröße bestand aus 32 aufeinanderfolgenden teilweise oder vollständig zahnlosen Patienten (32 Frauen; Durchschnittsalter 64,6 Jahre) mit 98 submergierten Implantaten. Bei nur einem Patienten fiel das maxilläre Implantat während der Heilungsphase aus. Während der gesamten Nachbeobachtungszeit fiel keine Prothese aus, und es wurden keine schwerwiegenden Komplikationen aufgezeichnet. Der Erfolg von Implantaten und Prothesen führte zu einer Gesamtüberlebensrate von 98, 98 % bzw. 100 %. Der durchschnittliche marginale Knochenverlust nach drei Jahren betrug 1,35 ± 0,21 (CI 95 % 1,24–1,38). Erfolgreiche Weichgewebsparameter wurden um alle Implantate herum festgestellt.
Schlussfolgerungen: Die orale Bisphosphonattherapie schien den Implantatüberleben und -erfolg bei genauer Auswahl der Behandlungszeit, minimalinvasivem chirurgischen Ansatz und konstantem Follow-up nicht signifikant zu beeinflussen. Weitere prospektive Studien mit größeren Stichprobengrößen und längeren Nachbeobachtungszeiträumen sind erforderlich, um diese Ergebnisse zu bestätigen.
Einführung
Osteoporose ist eine fortschreitende systemische Knochenerkrankung, die durch eine niedrige Knochendichte und eine mikroarchitektonische Verschlechterung des Knochengewebes gekennzeichnet ist, was zu einer erhöhten Knochenschwäche und Anfälligkeit für Frakturen führt (Kanis et al. 2008). Die häufigste medizinische Behandlung für Osteoporose umfasst die Verwendung von Bisphosphonaten (BPs) (Bernabei et al. 2014). Im Jahr 2009 hat die Food and Drug Administration die jährliche Injektion von Zoledronsäure zur Prävention von Osteoporose bei menopausalen Populationen genehmigt (Khosla 2009). Bisphosphonate sind stabile Analoga von natürlich vorkommenden anorganischen Pyrophosphaten und werden als antiresorptive Medikamente klassifiziert (Fleisch et al. 1966), die verwendet werden, um die Osteoklastenaktivität zu verringern, die Resorption von Knochen zu verhindern und dessen Umsatz zu reduzieren (Reszka & Rodan 2004). Sie werden häufig zur Behandlung von Erkrankungen eingesetzt, die den Knochenstoffwechsel betreffen, einschließlich multiples Myelom, sekundäre Hyperkalzämie verursacht durch bösartige Tumoren, Knochenmetastasen bei metastasierendem Prostata- oder Brustkrebs, Morbus Paget sowie Osteoporose (Sarzi Amadè et al. 2008).
Die Wirkung eines BPs hängt von der chemischen Struktur des Medikaments ab. Traditionell werden BPs in stickstoffhaltige (N-BPs) und stickstofffreie (nicht-N-BPs) Medikamente unterteilt. Die stickstofffreien Bisphosphonate werden in der Zelle in Verbindungen metabolisiert, die die terminale Pyrophosphatgruppe von ATP ersetzen, wodurch ein nicht-funktionelles Molekül entsteht, das mit Adenosintriphosphat (ATP) im zellulären Energiestoffwechsel konkurriert. Der Osteoklast initiiert die Apoptose und stirbt, was zu einer insgesamt verringerten Zersetzung von Knochen führt. Die Hinzufügung einer Aminogruppe an das Ende einer Seitenkette erhöht die Wirksamkeit des Medikaments; jedoch ist der Mechanismus der stickstoffhaltigen BPs weniger gut bekannt. Laut Reszka & Rodan (2004) hemmen N-BPs das Enzym Farnesyl-Diphosphat-Synthase des Cholesterinbiosynthesewegs und stören den Isoprenylierungszweig, was Proteine und andere Faktoren hemmt, die eine geschwindigkeitsbestimmende Rolle bei der Osteoklastenresorption von Knochen spielen. N-BPs reichern sich in maximaler Konzentration in der knöchernen Matrix und in Osteoklasten an, hauptsächlich während der ersten 24–48 Stunden der Medikation. Das Endergebnis ist eine zelluläre Dysfunktion und der Tod der Osteoklasten (Jones et al. 2001). Die resultierende Hemmung der normalen Knochenresorption führt zu einer verringerten Knochenumsatzrate, erhöhten Knochendichte, verbesserter Mineralisierung und reduziertem Frakturrisiko (Jones et al. 2001).
Alendronat ist ein stickstoffhaltiges Bisphosphonat, das umfangreich zur Behandlung von Osteoporose eingesetzt wird (Tsetsenekou et al. 2012). Die Auswirkungen von lokal und/oder systemisch verabreichtem Alendronat auf die Osseointegration wurden umfassend evaluiert, wobei Experimente an Tieren durchgeführt wurden (Abtahi et al. 2013). Laut einer von der American Society for Bone and Mineral Research eingerichteten Arbeitsgruppe gibt es jedoch nur wenige Informationen über die Nebenwirkungen der oralen N-BPs (Kos et al. 2010).
Zwei aktuelle systematische Übersichten der Literatur deuten darauf hin, dass die Einnahme von oralen BPs die kurzzeitigen (1–4 Jahre) Überlebensraten von Implantaten nicht beeinflusste, selbst wenn Komplikationen auftraten (Madrid & Sanz 2009; Ata-Ali et al. 2014). Dennoch fehlen weiterhin prospektive Studien, die Überlebens- und Erfolgsraten von Implantaten berichten. Da universell akzeptierte Richtlinien noch nicht veröffentlicht wurden, bleibt das klinische Management der bisphosphonatbedingten ONJ umstritten (Rupel et al. 2014). Seit 2003 wurden Berichte über Nekrosen der Kieferknochen veröffentlicht, die möglicherweise mit der Verabreichung von Bisphosphonaten in Verbindung stehen (Hasegawa et al. 2012). Es gab Diskussionen über die Risiken, die mit der Durchführung oraler chirurgischer Eingriffe, insbesondere Knochenaugmentation und Implantatplatzierung, bei Patienten, die orale BPs einnehmen, verbunden sind (Sarzi Amadè et al. 2008; Memon et al. 2012; Kwon et al. 2014). Dieselben Autoren kamen zu dem Schluss, dass die Prävention von BP-bedingter ONJ nicht vollständig möglich ist, aber nicht-invasive präventive Verfahren helfen könnten, ihre Inzidenz zu verringern (Sarzi Amadè et al. 2008; Memon et al. 2012; Kwon et al. 2014). Die American Association of Oral and Maxillofacial Surgeons empfiehlt, dass Patienten BPs 3 Monate vor und 3 Monate nach der oralen Chirurgie, wenn möglich, aussetzen, insbesondere wenn ein Patient BPs länger als 3 Jahre eingenommen hat (Ruggiero et al. 2009; Allen & Ruggiero 2014). Für Patienten mit einer Vorgeschichte der oralen Bisphosphonatbehandlung von mehr als 3 Jahren und solchen mit gleichzeitiger Behandlung mit Prednison sollten zusätzliche Tests und alternative Behandlungsoptionen in Betracht gezogen werden (Grant et al. 2008).
Ziel dieser multizentrischen prospektiven Beobachtungsstudie war es, die 3-Jahres-Daten zu Implantaten und prothetischen Überlebens- und Erfolgsraten sowie den peri-implantären Knochenverlust nach der Platzierung einer festen implantatgetragenen Zahnprothese bei Patienten, die seit mindestens 3 Jahren orale Bisphosphonate (Alendronat 70 mg Tablette einmal pro Woche oder 5–10 mg einmal täglich) einnehmen, zu präsentieren. Diese Studie folgte den STROBE (Strengthening the Reporting of Observational studies in Epidemiology) Richtlinien.
Material und Methoden
Studienaufbau
Diese multizentrische prospektive Beobachtungsstudie wurde entworfen, um das klinische und radiologische Ergebnis von festen implantatgetragenen Zahnprothesen zu bewerten, die Patienten, die Alendronat 70 mg Tablette einmal wöchentlich oder 5–10 mg einmal täglich einnehmen, mindestens 3 Jahre vor der Implantatplatzierung, geliefert wurden. Vierzig Patienten wurden ausgewählt und in zwei privaten Zentren behandelt (20 in Rom, 20 in Sassari, Italien), zwischen Januar 2008 und Dezember 2011. Zwei erfahrene Kliniker führten alle Implantate und prothetischen Verfahren durch. Die Untersuchung wurde gemäß den Prinzipien durchgeführt, die in der Helsinki-Deklaration von 1964 für biomedizinische Forschung mit menschlichen Probanden, wie 2008 geändert, verankert sind. Die Patienten wurden über klinische Verfahren, verwendete Materialien, Vorteile, potenzielle Risiken und Komplikationen sowie die für die klinische Studie erforderlichen Nachuntersuchungen informiert und gaben ihr schriftliches Einverständnis zur Teilnahme an dieser Studie.
Jeder gesunde Patient <90 Jahre alt, über 18 Jahre alt zum Zeitpunkt der Implantation, der eine implantatgestützte Prothese benötigt, wurde in aufeinanderfolgender Reihenfolge gebeten, an der Untersuchung teilzunehmen. Patienten wurden in die Studie aufgenommen, nachdem sie die Einschlusskriterien erfüllt und keine der Ausschlusskriterien erfüllt hatten.
Die Ausschlusskriterien waren wie folgt:
- Allgemeine medizinische (American Society of Anesthesiologist, ASA, Klasse III oder IV) und/oder psychiatrische Kontraindikationen;
- Schwangerschaft oder Stillzeit;
- Alkohol- oder Drogenmissbrauch;
- Starkes Rauchen (>10 Zigaretten/Tag);
- Strahlentherapie im Kopf- oder Halsbereich innerhalb der letzten 5 Jahre;
- Hohe und moderate parafunktionale Aktivität;
- Fehlen von Zähnen/Prothesen im gegenüberliegenden Kiefer;
- Unbehandelte Parodontitis;
- Post-extraktive Implantate;
- Vollständige Mundblutung und vollständiger Mundplaque-Index höher oder gleich 25 %;
- <10 mm Höhe und 5 mm Breite des Knochens zur Ermöglichung von Implantaten;
- Nichtverfügbarkeit für regelmäßige Nachuntersuchungen.
Alle Patienten wurden gemäß einem zweistufigen diagnostischen und therapeutischen Protokoll behandelt (Abb. 1). Die diagnostischen Schritte sind wie folgt:
- Anamnese;
- Klinische Untersuchung und Fotografien;
- Radiologische Untersuchung einschließlich peri-apikaler und panoramischer Röntgenaufnahmen, Computertomographie (CT) oder Cone Beam CT (CBCT);
- Parodontaluntersuchung (Sondierung und Messung der Indizes der Mundgesundheit);
- Fotografische Dokumentation;
- Patienteninformation (Medikamente und mögliche Konsequenzen).
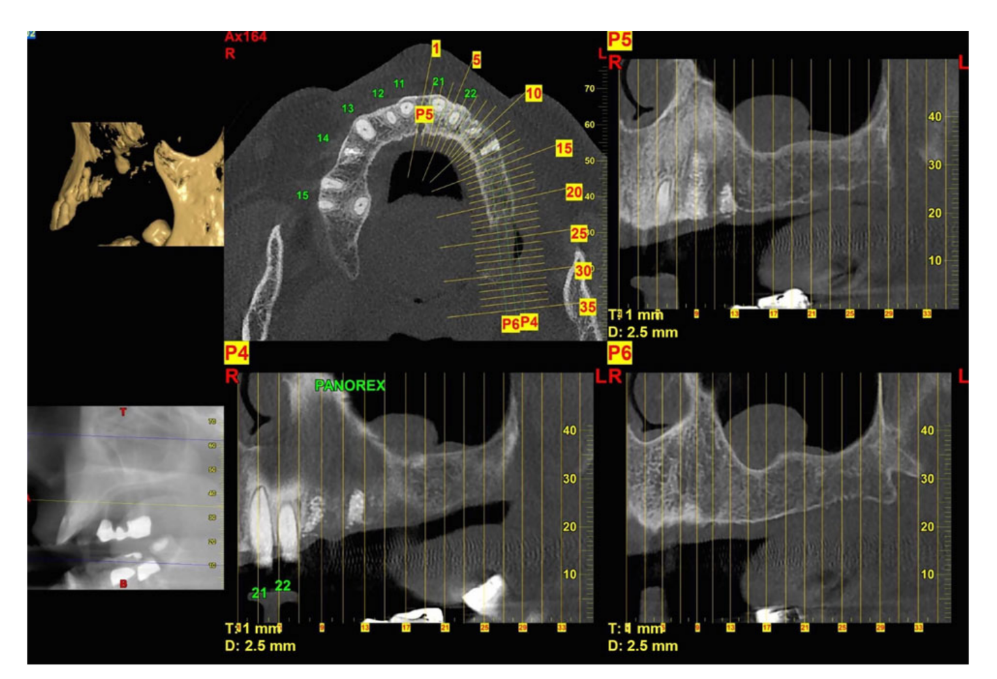
Klinische Verfahren
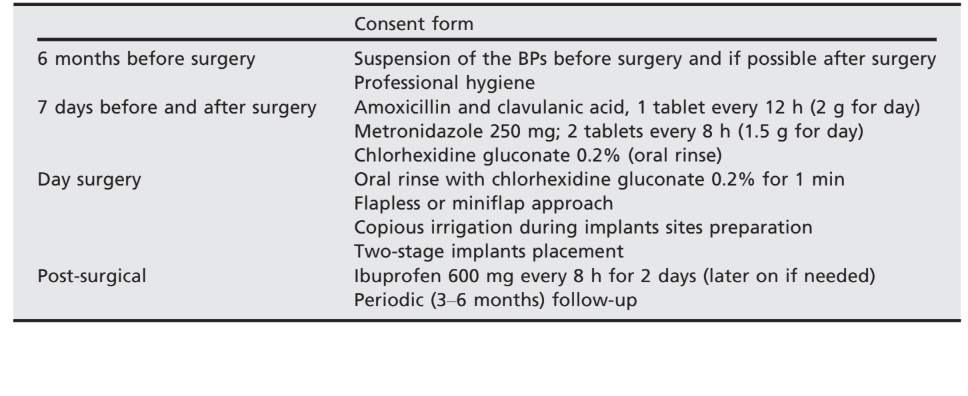
Therapeutisches Protokoll (Tabelle 1):
- Professionelle Hygiene;
- Beseitigung aller Infektionsherde (restliche Wurzeln, Karies, parodontaltherapie):
- nicht-restaurative-chirurgische Behandlung aller kompromittierten Zähne oder mit schlechter Prognose;
- restaurative Behandlung von Zähnen, die von Karies betroffen sind;
- parodontaler Behandlung und unterstützender Therapie;
- Bewertung der Angemessenheit von herausnehmbaren und festen Prothesen. Insbesondere wurde der Sitz der prothetischen Strukturen und die Stabilität der herausnehmbaren Prothese bewertet, die atraumatisch sein müssen.
Am Ende der Präventionsphase wurden die Patienten motiviert, ein sorgfältiges häusliches Mundhygieneprotokoll einzuhalten und professionelle Nachsorgetermine wahrzunehmen.
Zwei erfahrene Chirurgen (MT & SMM) führten alle Eingriffe durch. Wenn geplant, wurde die atraumatische Zahnextraktion mindestens 8 Wochen vor der Implantation durchgeführt. Die Kronen mehrwurzeliger Zähne wurden in Segmente geschnitten. Die Wurzeln wurden dann einzeln entfernt und, falls nötig, mit Hilfe eines Periotoms. Die verbleibenden Extraktionssocket wurden gründlich von Granulationsgewebe und verbleibenden parodontalen Fasern mit Küretten gereinigt.
Das präoperative Protokoll erforderte die Aussetzung der BPs 6 Monate vor der Operation und bis zur vollständigen Heilung 4–6 Monate nach der Implantation. Antibiotika wurden prophylaktisch 7 Tage vor der Operation verabreicht und für 7 Tage fortgesetzt (Sarzi Amadè et al. 2008):
- Amoxicillin und Clavulansäure, eine Tablette alle 12 h (2 g pro Tag);
- Metronidazol 250 mg; zwei Tabletten alle 8 h (1,5 g pro Tag).
Vor Beginn der Operation spülten die Patienten 1 Minute lang mit einer 0,2%igen Chlorhexidin-Mundspülung. Die lokale Anästhesie wurde mit einer 4%igen Articainlösung mit Epinephrin 1 : 100.000 (Ubistein; 3M Italy SpA, Mailand, Italien) induziert. Die Implantate wurden an den geplanten anatomischen Stellen mit einer flapless oder einer Miniflap-Technik eingesetzt, (Abb. 2). Die Knochendichte wurde während der Bohrphase anhand der Erfahrung und Empfindung des Klinikers beurteilt und basierte auf der Klassifikation von Lekholm und Zarb (Brånemark et al. 1985). Jeder Bohrer wurde unter reichlicher Spülung gemäß dem vom Hersteller empfohlenen Protokoll verwendet. Die Implantatplattform wurde auf Höhe des alveolären Kamms oder leicht darunter im ästhetischen Bereich positioniert.
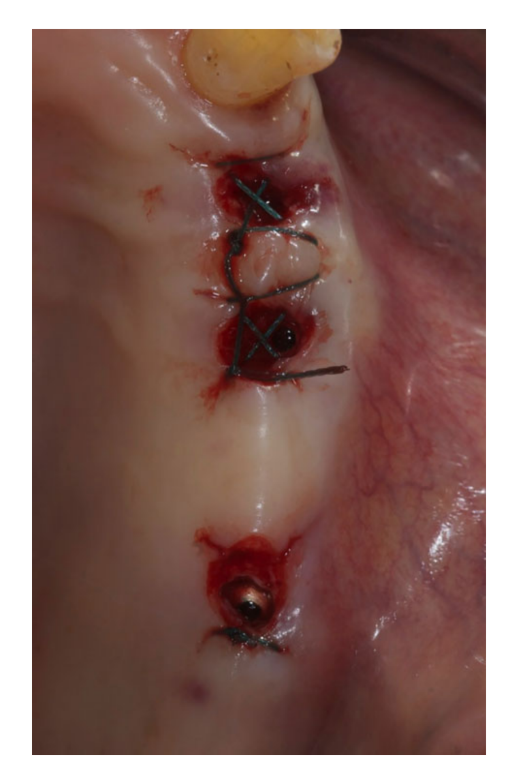
Nach der Implantation erhielten alle Patienten mündliche und schriftliche Empfehlungen bezüglich Medikation, Mundhygiene und Ernährung. Die postoperative Schmerzbehandlung wurde mit Ibuprofen 100 mg durchgeführt, das alle 8 Stunden für 2 Tage nach der Operation verabreicht wurde und später bei Bedarf. Die Patienten wurden angewiesen, zweimal täglich mit einer Chlorhexidin 0,2% Mundspülung zu spülen, ohne den Implantatbereich bis zur Fadenentfernung (10–14 Tage danach) zu putzen.
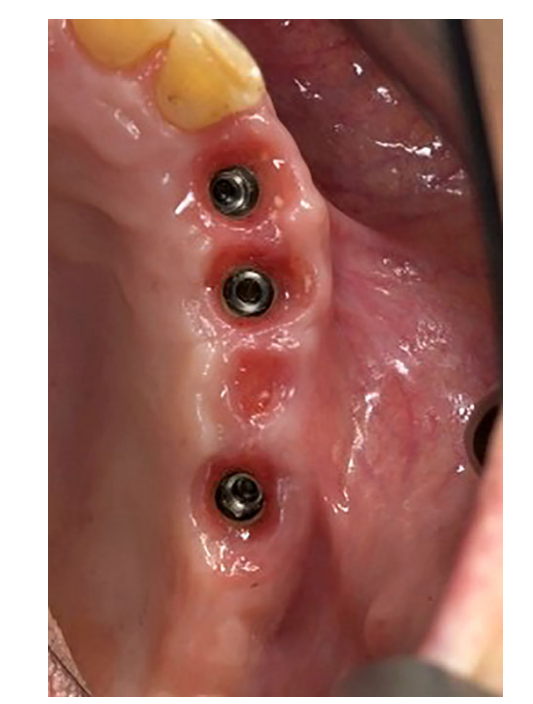
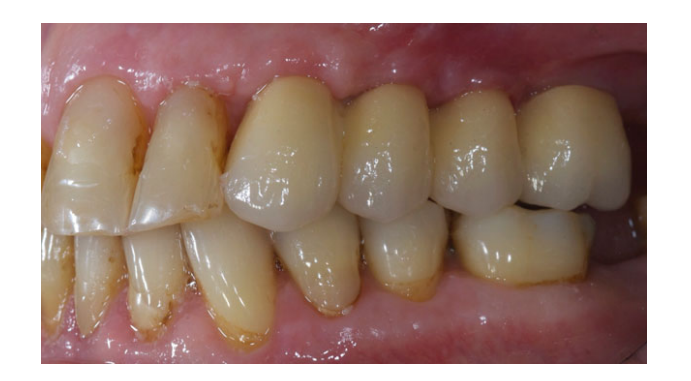
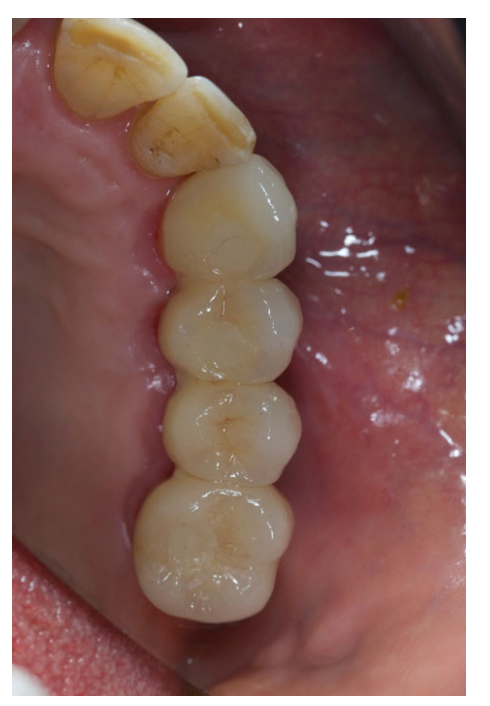
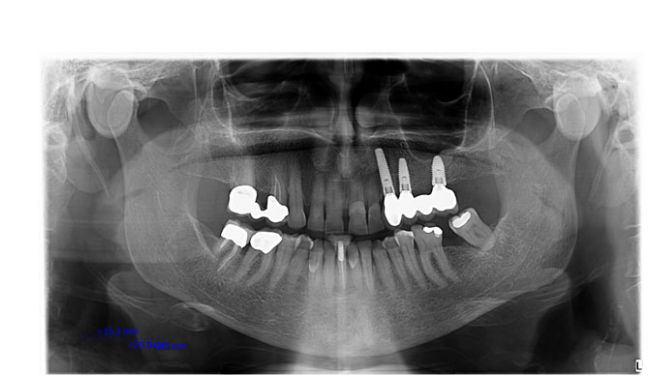
Alle Implantate wurden submers platziert. Die Implantate wurden 3 Monate nach der Implantation freigelegt (Abb. 3 und 4). Offene Tray-Abdrücke wurden mit einem Polyether-Material (ImpregumTM, 3M ESPE, Seefeld, Deutschland) unter Verwendung eines maßgefertigten offenen Tray (Diatray Top, Dental Kontor, Stockelsdorf, Deutschland) genommen. Zum Zeitpunkt der Prothesenabgabe (Abb. 5 und 6) wurde der Biss angepasst und die Restaurationen wurden entweder geschraubt oder mit zementfreiem Eugenol-Zinkoxid-Zement (Temp Bond NE, Kerr Corporation, Orange, CA, USA) 12 Wochen nach der ersten Operation gemäß einem konventionellen Belastungsprotokoll (Gallucci et al. 2013) zementiert. Nachsorgeuntersuchungen wurden 1–6 Monate und dann jährlich bis zu 3 Jahre nach der Funktion (Abb. 7) geplant. Bei jeder Nachsorgeuntersuchung wurde der okklusale Anpassung der Zahnprothese bei Bedarf durchgeführt. Die Patienten unterzogen sich alle 4–6 Monate einer professionellen Reinigung durch eine zahnmedizinische Fachkraft. Periapikale Röntgenaufnahmen wurden jährlich nach der definitiven Prothesenabgabe mit demselben maßgeschneiderten Rinn-Halter (Rinn, Elgin, IL, USA) angefertigt.
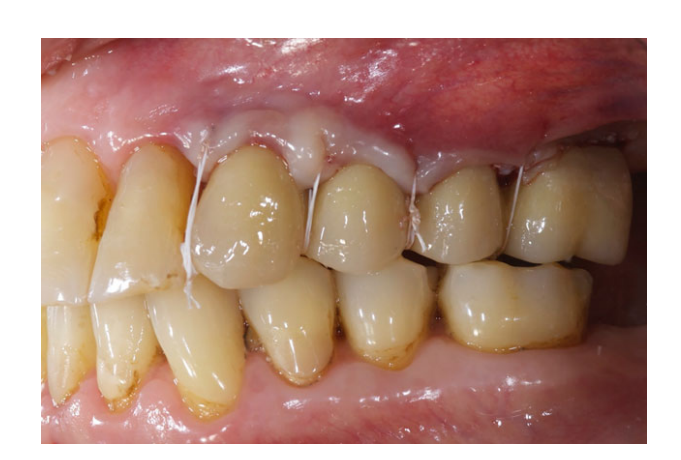
Ergebnismaße
Die primären Ergebnismaße waren die Erfolgs- und Überlebensraten der Implantate. Bei jeder Nachuntersuchung wurden die Implantate auf Gewebeintegration gemäß den strengen Parametern untersucht, die von Buser et al. (1990) definiert wurden. Insbesondere wurde die Integration als erfolgreich angesehen, wenn die folgenden Parameter erfüllt waren: (1) Abwesenheit einer wiederkehrenden peri-implantären Infektion mit Eiterbildung; (2) Abwesenheit anhaltender subjektiver Beschwerden wie Schmerzen, Fremdkörpergefühl und/oder Dysästhesie; (3) Abwesenheit einer kontinuierlichen Radioluzens um das Implantat und (4) Abwesenheit jeglicher nachweisbarer Implantatmobilität. Diese Kriterien haben sich als effektiv erwiesen, um den Erfolg eines Implantatsystems zu definieren und langfristige Ergebnisse in klinischen Studien zu bewerten. Der Erfolg der Prothese wurde nach einer Modifikation der Bewertungskriterien, die von der California Dental Association (CDA (Vereinigung CD 1976)) vorgeschlagen wurden, bewertet.
Die sekundären Ergebnisse waren die folgenden: alle chirurgischen und prothetischen Komplikationen, die während der gesamten Nachbeobachtungszeit auftraten, marginaler Knochenverlust, Sondierungstiefen (PPD) und Blutung bei der Sondierung (BOP).
- Komplikationen: Alle technischen (Bruch des Gerüsts und/oder des Verblendmaterials, Schraubenlockerung usw.) und/oder biologischen (Schmerzen, Schwellungen, Eiterbildung usw.) Komplikationen wurden berücksichtigt.
- Marginaler Knochenverlust: Der Abstand vom höchsten Rand des Implantathals und dem höchsten Punkt des Knochen-zu-Implantat-Kontakts wurde als marginaler Knochenstand (MBL) betrachtet. Der MBL um die Implantate wurde anhand von intraoralen digitalen Röntgenaufnahmen, die mit der Parallelschichttechnik unter Verwendung eines Filmhalters (Rinn XCP, Dentsply, Elgin, IL, USA) bei der Implantation (Basislinie) und nach 12, 24 und 36 Monaten gemacht wurden, bewertet. Die Röntgenaufnahmen wurden zur Bewertung akzeptiert oder abgelehnt, basierend auf der Klarheit der Implantatgewinde. Alle lesbaren Röntgenaufnahmen wurden in einem Bildanalyseprogramm (DFW2.8 für Windows, Soredex, Tuusula, Finnland) auf einem 24-Zoll-LCD-Bildschirm (iMac, Apple, Cupertino, CA, USA) angezeigt und unter standardisierten Bedingungen (SO 12646:2004) bewertet. Die Software wurde für jedes einzelne Bild unter Verwendung des bekannten Abstands des Implantatdurchmessers oder der Länge kalibriert. Messungen des mesialen und distalen Knochenkammniveaus neben jedem Implantat wurden auf die nächstgelegene 0,1 mm genau durchgeführt und auf Patientenebene gemittelt.
- PPD und BoP wurden von einem blinden Operator mit einer Parodontalsonde (PCP-UNC 15; Hu-Friedy Manufacturing, Chicago, IL, USA) bei 6, 12, 24 und 36 Monaten gemessen. Drei vestibuläre und drei linguale Werte wurden für jedes Implantat erfasst und auf Patientenebene gemittelt.
Zwei unabhängige und vollständig verblindete Zahnärzte (LC und EX) für jedes Zentrum bewerteten die Überlebens- und Erfolgsraten von Implantaten und Prothesen. Komplikationen wurden von den behandelnden Klinikern (MT und SMM), die nicht verblindet waren, bewertet und behandelt. Der marginale Knochenverlust (DMBL) wurde von einem unabhängigen Radiologen bewertet. Ein unabhängiger Hygieniker führte alle parodontalen Messungen durch.
Statistische Analyse
Die statistische Analyse wurde für numerische Parameter wie marginale Knochenhöhe und Weichgewebsparameter mit SPSS für Mac OS X Version 22.0 (SPSS, Chicago, IL, USA) durchgeführt. Eine deskriptive Analyse wurde unter Verwendung des Mittelwerts, der Standardabweichung (SD) und des Medians mit einem 95% Konfidenzintervall (CI) durchgeführt. Kumulative Überlebens- und Erfolgsraten wurden berechnet, wobei die Implantate und Prothesen als statistische Einheit der Analysen verwendet wurden. Unterschiede der durchschnittlichen marginalen Knochenhöhen zwischen den Nachuntersuchungen, gemittelt auf Patientenebene, wurden mit dem Wilcoxon-Vorzeichen-Rang-Test für gepaarte Stichproben verglichen. Das Niveau der statistischen Signifikanz wurde auf 0,05 festgelegt. Vergleiche zwischen den Zentren wurden durch eine einfaktorielle Varianzanalyse (ANOVA) durchgeführt.
Ergebnisse
Am Ende der Studie brachen acht Patienten (20%) mit 18 Implantaten (15,5%) ab. Ein Patient im Rom-Zentrum starb an Leberkrebs. Fünf Patienten (zwei im Rom-Zentrum und drei im Sassari-Zentrum) hatten ernsthafte Gesundheitsprobleme, die nicht mit der Zahnimplantattherapie in Zusammenhang standen, sodass sie nicht zu den geplanten Nachuntersuchungen kommen konnten. Zwei Patienten zogen ins Ausland. Basierend auf einem Telefoninterview hatten jedoch alle diese Patienten ihre Implantate ohne patientenbezogene Komplikationen (Schmerzen, Schwellungen) in Funktion. Die endgültige Stichprobengröße ergab insgesamt 98 Implantate mit rauer oxidierter Oberfläche und konischem Implantatdesign (NobelReplace, Nobel Biocare AB), die bei 32 aufeinanderfolgenden zahnlosen Patienten (32 Frauen) mit einem Durchschnittsalter von 64,6 Jahren (Bereich 46–80) eingesetzt wurden. Jedes Zentrum behandelte die gleiche Anzahl von 16 Patienten. Jeder Patient wurde über einen Zeitraum von ≥3 Jahren in Funktion verfolgt (Bereich 36–72 Monate; Durchschnitt 47,6 Monate). Es gab keine offensichtlichen Ausgangsungleichgewichte zwischen den beiden Gruppen, abgesehen von einer höheren Anzahl längerer Implantate, die vom Zentrum in Rom verwendet wurden, und der Anwesenheit von mehr Fällen, die mit computerassistierter, schablonenbasierter Chirurgie im Zentrum Sardinien behandelt wurden. Es gab keine Abweichung vom ursprünglichen Protokoll. Alle gesammelten Daten wurden in die statistische Analyse einbezogen.
- Eines von 98 Implantaten (1,02%) versagte während der Heilungsphase, vor der Lieferung der endgültigen Prothesen, was zu einer kumulierten Überlebensrate der Implantate von 98,98% bei der 3-Jahres-Nachuntersuchung führte. Der einzige Implantatfehler trat bei einem Patienten im Sardinien-Zentrum auf (schmaler Plattform-Implantat, 10 mm lang). Das Implantat wurde nicht ersetzt.
- Bei der 3-Jahres-Nachuntersuchung hatte keine der endgültigen Prothesen versagt, was zu einer kumulierten Überlebensrate der Prothesen von 100% führte.
- Es wurden keine prothetischen Komplikationen beobachtet. Es wurden keine größeren biologischen Komplikationen aufgezeichnet. Drei Patienten hatten nach 6 Monaten eine peri-implantäre Mukosainflammation mit BoP. Verbesserte Mundhygiene reduzierte die peri-implantäre Entzündung ohne chirurgische Eingriffe.
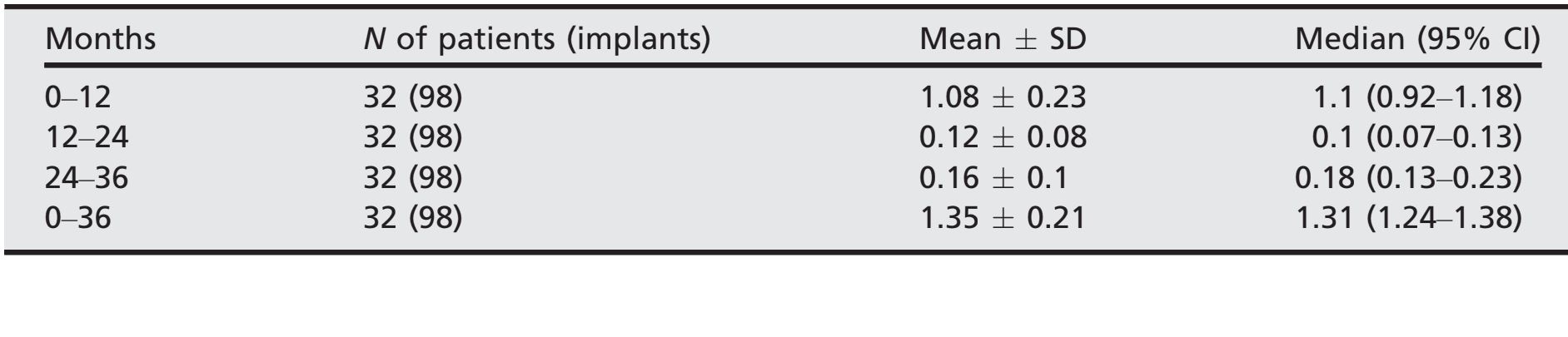
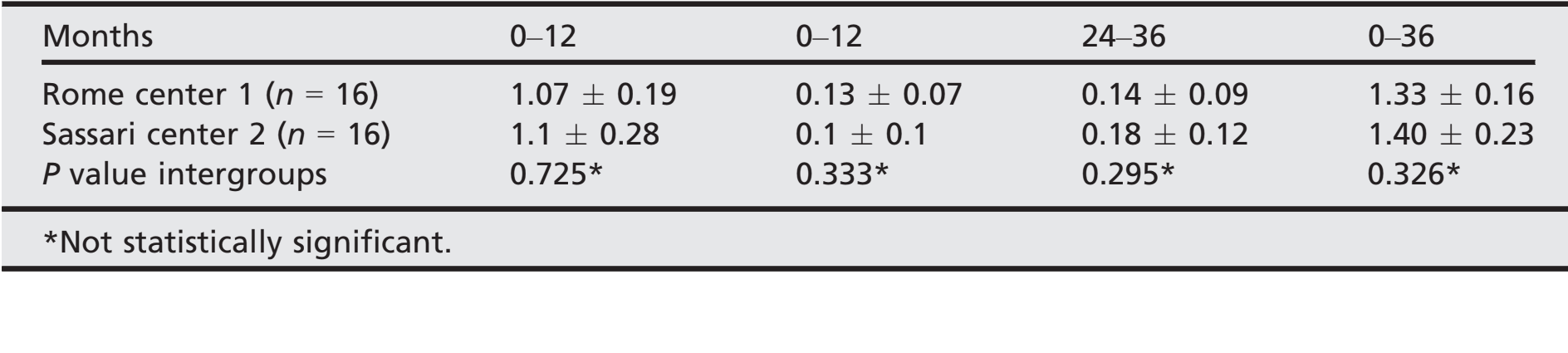
- Nach einem anfänglichen mittleren marginalen Knochenverlust von 1,08 ± 0,23 (Median 1,1; CI 95% 0,92–1,18) verloren alle Implantate zwischen der 1- und 2-Jahres-Nachuntersuchung im Durchschnitt 0,12 ± 0,08 (Median 0,1; CI 95% 0,07–0,13) und zwischen der 2- und 3-Jahres-Nachuntersuchung 0,16 ± 0,1 (Median 0,18; CI 95% 0,13–0,23), ohne statistisch signifikanten Unterschied (P = 0,059). Bei der 3-Jahres-Nachuntersuchung betrug der durchschnittliche marginale Knochenverlust 1,35 ± 0,21 (Median 1,31; CI 95% 1,24–1,38). Alle Daten sind in Tabelle 2 aufgeführt. Bei jeder Nachuntersuchung waren die Veränderungen des Knochenlevels in beiden Zentren ähnlich (P ≥ 0,05). Alle Daten sind in Tabelle 3 aufgeführt.
- Bei der 3-Jahres-Nachuntersuchung betrugen die durchschnittlichen PPD-Werte 2,71 ± 0,38 mm (95% CI = 2,54–2,86). Die durchschnittlichen BoP-Werte lagen bei 1,29 ± 0,76 (95% CI = 0,93–1,63).
Diskussion
Die vorliegende prospektive Beobachtungsstudie wurde entworfen, um die 3-jährigen klinischen und radiografischen Ergebnisse einer festen implantatgetragenen Zahnprothese zu bewerten, die an Patienten abgegeben wurde, die einmal wöchentlich eine Alendronat-Tablette von 70 mg oder 5–10 mg einmal täglich für mindestens 3 Jahre vor der Implantation einnahmen.
Bei der 3-jährigen Nachuntersuchung zeigten die Ergebnisse der vorliegenden Studie eine Überlebensrate von Implantaten und Prothesen von 99% bzw. 100%. Marginale Knochenveränderungen sowie BOP- und PPD-Werte scheinen nach 3 Jahren stabil zu sein, was bestätigt, dass die Implantattherapie bei Patienten, die orale BPs einnehmen, eine tragfähige Behandlung gemäß dem vorgeschlagenen therapeutischen Protokoll ist. Diese Ergebnisse stimmen mit anderen Studien überein, die dasselbe Thema untersuchen. In einer retrospektiven Studie kamen Memon et al. (2012) zu dem Schluss, dass Bisphosphonate den frühen Implantationserfolg oder Veränderungen des crestal Knochen nicht beeinflussten. Jeffcoat (2006) und Russo Dello et al. (2007) berichteten in zwei prospektiven Studien, dass orale BPs anscheinend die Inzidenz von ONJ nicht erhöhten. Grant et al. (2008) berichteten in einer retrospektiven Studie über 115 Patienten (468 Implantate), dass die orale Bisphosphonattherapie keinen signifikanten Einfluss auf den Implantationserfolg zu haben schien.
Die Hauptbeschränkungen dieser Studie sind die begrenzte Anzahl an Teilnehmern, die über einen kurzen Zeitraum nachverfolgt wurden. Dennoch, obwohl acht Patienten ausfielen, wurden 98 Implantate bei 32 Patienten eingesetzt, die mit demselben Protokoll behandelt wurden und mindestens 3 Jahre lang nachverfolgt wurden, was es ermöglicht, die Ergebnisse der vorliegenden Studie auf eine größere Population mit ähnlichen Merkmalen zu verallgemeinern.
Tierstudien haben gezeigt, dass die Verabreichung von BPs das normale Knochenremodellierung nach einer Zahnextraktion beeinträchtigt und die langfristige Heilung um Implantate gefährdet (Kim et al. 2013). Eine der schwerwiegendsten, wenn auch seltenen Komplikationen ist die bisphosphonatbedingte Osteonekrose der Kiefer (BRONJ) (Kwon et al. 2014). Die Häufigkeit von BRONJ kann je nach Verabreichungsweg und der Stärke der verwendeten Medikamente variieren. Die American Association of Oral and Maxillofacial Surgeons berichtete, dass die Prävalenz von BRONJ etwa 0,8 % bis 12 % betrug, wenn BPs intravenös verabreicht werden (Ruggiero et al. 2009; Allen & Ruggiero 2014). Die Prävalenz ist Berichten zufolge niedriger, wenn BPs oral verabreicht werden. Es wurde jedoch vorgeschlagen, dass besondere Aufmerksamkeit geschenkt werden sollte, wenn Patienten mehr als 3 Jahre lang mit BPs behandelt werden, da die Prävalenz von BRONJ im Verlauf der BPs-Behandlung zunimmt (Sarzi Amade` et al. 2008). Nach einer schlechten enthusiastischen vorläufigen Ergebnissen basierend auf unkontrollierten retrospektiven Studien, schlugen einige systematische Übersichten optimistischere Ergebnisse vor. Madrid & Sanz (2009) kamen zu dem Schluss, dass ein Patient, der orale Bisphosphonate über einen Zeitraum von <5 Jahren einnimmt, „sicher“ ist, zahnärztliche Eingriffe, insbesondere Zahnimplantate, durchzuführen (Madrid & Sanz 2009). Darüber hinaus gibt es einen allgemeinen Konsens über die Nicht-Kontraindikation der Implantation bei nicht-krebskranken Patienten, die orale BPs einnehmen, die hauptsächlich zur Behandlung von Osteoporose verschrieben werden (Madrid & Sanz 2009). Kürzlich haben Kumar & Honne (2012) die Überlebensrate von Zahnimplantaten bei Bisphosphonat-Nutzern im Vergleich zu Nicht-Nutzern bewertet und kamen zu dem Schluss, dass eine kurzfristige BPs-Therapie die Überlebensrate von Zahnimplantaten im Vergleich zu Nicht-Nutzern nicht erhöht oder verringert.
Obwohl die submerse Technik keine Voraussetzung für die Osseointegration ist (Tallarico et al. 2011), wurden in der vorliegenden Studie alle Implantate submers platziert, ohne chirurgische Komplikationen. Dies könnte einen der Schlüsselfaktoren darstellen, zusammen mit einer signifikanten Antibiotikabehandlung und dem vorübergehenden Abbruch der Alendronat-Verabreichung, um eine bakterielle Kontamination des Implantatstandorts zu verhindern.
In der vorliegenden Studie, obwohl die Anzahl der Patienten begrenzt war, führte die Implantatchirurgie nach 3 Jahren nach der Implantation nicht zu einer bisphosphonatbedingten Osteonekrose des Kiefers. Dennoch gibt es ausreichende Hinweise darauf, dass alle Patienten, die sich einer Implantation unterziehen, zu ihrer Bisphosphonattherapie befragt werden sollten, einschließlich des eingenommenen Medikaments, der Dosierung und der Dauer der Behandlung vor der Operation. Potenzielle Risiken von BRONJ müssen den Patienten vor der Implantation erklärt werden. Für Patienten mit einer Vorgeschichte der oralen Bisphosphonatbehandlung von mehr als 3 Jahren und solchen, die gleichzeitig mit Prednison behandelt werden, sollten zusätzliche Tests und alternative Behandlungsoptionen in Betracht gezogen werden, und Prävention ist nach wie vor das effektivste Mittel, um mögliche Komplikationen zu vermeiden. Darüber hinaus waren der anatomische Standort des Implantats und die Dauer der Medikamententherapie zum Zeitpunkt der Platzierung keine signifikanten Faktoren für die Erfolgsquote oder knöcherne Veränderungen.
Fazit
Innerhalb der Grenzen dieser Studie zeigte die vorgeschlagene therapeutische Protokoll und die Durchführung einer minimal-invasiven, submersen Chirurgie, dass die orale Bisphosphonattherapie keinen signifikanten Einfluss auf das Überleben und den Erfolg von Implantaten im mittelfristigen Follow-up hatte. Diese Schlussfolgerungen sollten durch weitere prospektive Studien mit größeren Stichprobengrößen und längeren Nachbeobachtungszeiträumen bestätigt werden.
Marco Tallarico, Luigi Canullo
Literaturverzeichnis
- Abtahi, J., Agholme, F., Sandberg, O. & Aspenberg, P. (2013) Einfluss der lokalen vs. systemischen Bisphosphonatgabe auf die Fixierung von Zahnimplantaten in einem Modell der Osteonekrose des Kiefers. Journal of Dental Research 92: 279–283.
- Allen, M.R. & Ruggiero, S.L. (2014) Eine Übersicht über pharmazeutische Mittel und die orale Knochengesundheit: wie die Osteonekrose des Kiefers das Feld beeinflusst hat. International Journal of Oral and Maxillofacial Implants 29: e45–e57.
- Ata-Ali, J., Ata-Ali, F., Penarrocha-Oltra, D. & Galindo-Moreno, P. (2014) Welchen Einfluss hat die Bisphosphonattherapie auf das Überleben von Zahnimplantaten? Eine systematische Übersicht und Metaanalyse. Clinical Oral Implants Research doi: 10.1111/clr.12526. [Epub ahead of print].
- Bernabei, R., Martone, A.M., Ortolani, E., Landi, F. & Marzetti, E. (2014) Screening, Diagnose und Behandlung von Osteoporose: eine kurze Übersicht. Clinical Cases in Mineral and Bone Metabolism 11: 201–207.
- Brånemark, P.I., Zarb, G.A. & Albrektsson, T. (1985) Gewebeintegrierte Prothesen: Osseointegration in der klinischen Zahnheilkunde. Chicago: Quintessence ed.
- Buser, D., Weber, H.P. & Lang, N.P. (1990) Gewebeintegration von nicht-submersen Implantaten. 1-Jahres-Ergebnisse einer prospektiven Studie mit 100 ITI-Hohlzylinder- und Hohl-Schrauben-Implantaten. Clinical Oral Implants Research 1: 33–40.
- California Dental Association, Task Force on Quality Evaluation. (1976) Qualitätsbewertung für zahnärztliche Versorgung: Richtlinien zur Bewertung der klinischen Qualität und der beruflichen Leistung sowie die Standards für das Programmdesign zur Sicherstellung der Versorgungsqualität. Los Angeles: California Dental Association ed. Chicago.
- Fleisch, H., Russell, R. & Straumann, F. (1966) Einfluss von Pyrophosphat auf Hydroxylapatit und seine Auswirkungen auf die Calcium-Homöostase. Nature 212: 901–903.
- Grant, B.T., Amenedo, C., Freeman, K. & Kraut, R.A. (2008) Ergebnisse der Platzierung von Zahnimplantaten bei Patienten, die orale Bisphosphonate einnehmen: eine Übersicht über 115 Fälle. Journal of Oral and Maxillofacial Surgery 66: 223–230.
- Hasegawa, Y., Kawabe, M., Kimura, H., Kurita, K., Fukuta, J. & Urade, M. (2012) Einfluss von Prothesen am ursprünglichen Auftretensort auf die Prognose der bisphosphonatbedingten Osteonekrose der Kiefer: eine retrospektive Studie. Oral Surgery, Oral Medicine, Oral Pathology and Oral Radiology 114: 318–824.
- Jeffcoat, M.K. (2006) Sicherheit von oralen Bisphosphonaten: kontrollierte Studien über alveoläres Knochen. International Journal of Oral and Maxillofacial Implants 21: 349–353.
- Jones, D.H., Nakashima, T., Sanchez, O.H., Kozieradzki, I., Komarova, S.V., Sarosi, I., Morony, S., Rubin, E., Sarao, R., Hojilla, C.V., Komnenovic, V., Kong, Y.Y., Schreiber, M., Dixon, S.J., Sims, S.M., Khokha, R., Wada, T. & Penninger, J.M. (2006) Regulation der Migration von Krebszellen und Knochenmetastasen durch RANKL. Nature 440: 692–696.
- Kanis, J.A., McCloskey, E.V., Johansson, H., Oden, A., Melton, L.J. & Khaltaev, N. (2008) Ein Referenzstandard für die Beschreibung von Osteoporose. Bone 42: 467–475.
- Khosla, S. (2009) Zunehmende Optionen für die Behandlung von Osteoporose. New England Journal of Medicine 361: 818–820.
- Kim, I., Ki, H., Lee, W., Kim, H. & Park, J.B. (2013) Der Einfluss von systemisch verabreichten Bisphosphonaten auf die knöcherne Heilung nach Zahnextraktion und Osseointegration von Zahnimplantaten im Oberkiefer von Kaninchen. International Journal of Oral and Maxillofacial Implants 28: 1194–1200.
- Kos, M., Brusco, D., Kuebler, J. & Engelke, W. (2010b) Klinischer Vergleich von Patienten mit Osteonekrose der Kiefer, mit und ohne Vorgeschichte der Bisphosphonatgabe. International Journal of Oral and Maxillofacial Surgery 39: 1097–1102.
- Kos, M., Kuebler, J.F., Luczak, K. & Engelke, W. (2010a) Bisphosphonat-assoziierte Osteonekrose der Kiefer: eine Übersicht über 34 Fälle und Bewertung des Risikos. Journal of Cranio-Maxillofacial Surgery 38: 255–259.
- Kumar, M.N. & Honne, T. (2012) Überleben von Zahnimplantaten bei Bisphosphonat-Nutzern im Vergleich zu Nicht-Nutzern: eine systematische Übersicht. The European Journal of Prosthodontics and Restorative Dentistry 20: 159–162.
- Kwon, T.G., Lee, C.O., Park, J.W., Choi, S.Y., Rijal, G. & Shin, H.I. (2014) Osteonekrose im Zusammenhang mit Zahnimplantaten bei Patienten, die eine Bisphosphonatbehandlung erhalten. Clinical Oral Implants Research 25: 632–640.
- Madrid, C. & Sanz, M. (2009) Welchen Einfluss haben systemisch verabreichte Bisphosphonate auf die orale Implantattherapie? Eine systematische Übersicht. Clinical Oral Implants Research 20: 87–95.
- Memon, S., Weltman, R.L. & Katancik, J.A. (2012) Orale Bisphosphonate: frühe endossose Zahnimplantat-Erfolge und Veränderungen des Knochens. Eine retrospektive Studie. International Journal of Oral and Maxillofacial Implants 27: 1216–1222.
- Reszka, A.A. & Rodan, G.A. (2004) Mechanismus der Wirkung von stickstoffhaltigen Bisphosphonaten. Mini Reviews in Medicinal Chemistry 4: 711–719.
- Ruggiero, S.L., Dodson, T.B., Assael, L.A., Landesberg, R., Marx, R.E. & Mehrotra, B. (2009) Positionspapier der American Association of Oral and Maxillofacial Surgeons zur bisphosphonatbedingten Osteonekrose des Kiefers – Update 2009. Australian Endodontic Journal 35: 119–130.
- Rupel, K., Ottaviani, G., Gobbo, M., Contardo, L., Tirelli, G., Vescovi, P., Di Lenarda, R. & Biasotto, M. (2014) Eine systematische Übersicht über therapeutische Ansätze bei bisphosphonatbedingter Osteonekrose des Kiefers (BRONJ). Oral Oncology 50: 1049–1057. Russo Dello, N.M., Jeffcoat, M.K., Marx, R.E. & Fugazzotto, P. (2007) Osteonekrose in den Kiefern von Patienten, die orale Bisphosphonate zur Behandlung von Osteoporose verwenden. International Journal of Oral and Maxillofacial Implants 22: 146–153.
- Sarzi Amadè, D., Tallarico, M., Loreti, M.C., Montecchi, P.P. & Niccoli, A. (2008) Klinische Richtlinien zur Prävention von Osteonekrose der Kiefer bei Patienten in Behandlung mit Bisphosphonaten: Literaturübersicht und Bericht über drei Fälle. Minerva Stomatologica 57: 429–446.
- Tallarico, M., Vaccarella, A. & Marzi, G.C. (2011) Klinische und radiologische Ergebnisse der 1- versus 2-stufigen Implantation: 1-Jahres-Ergebnisse einer randomisierten klinischen Studie. European Journal of Oral Implantology 4: 13–20.
- Tsetsenekou, E., Papadopoulos, T., Kalyvas, D., Papaioannou, N., Tangl, S. & Watzek, G. (2012) Der Einfluss von Alendronat auf die Osseointegration von nanobehandelten Zahnimplantaten bei Neuseeländischen Kaninchen. Clinical Oral Implants Research 23: 659–666.