Subperiostale peri-implant augmentierte Schichttechnik zur horizontalen Knochenaugmentation bei Implantatplatzierung
Maschinenübersetzung
Der Originalartikel ist in EN Sprache (Link zum Lesen) geschrieben.
Die prothetisch gesteuerte Implantatplatzierung in einer reduzierten horizontalen Knochendimension führt häufig zu einer peri-implantären Knochendehiszenz oder Fenestration. Selbst bei Vorhandensein einer intakten, aber dünnen buccalen kortikalen Knochenplatte (BCBP) kann Trauma und die daraus resultierende Knochenremodellierung nach dem chirurgischen Eingriff zur Implantatplatzierung zu einem vertikalen Knochenverlust mit der Exposition des koronalen Teils des Implantats bei der Freilegung führen,1 was zu einer buccalen Knochendehiszenz führen kann, die langfristig eine Mukosarezession verursachen kann.
In der Literatur wurden verschiedene Techniken zum Grafting von buccalen Platten ohne Barrieremembranen zur horizontalen Augmentation beschrieben. Kürzlich wurde ein neuartiges Verfahren zur Knochenaugmentation, das auf der Nutzung des Periosts als Barrieremembran und Raum schaffendem „Gerät“ basiert, erfolgreich eingesetzt, um die horizontale Knochendimension vor der Implantatplatzierung zu verbessern. Konsistent führte der Einsatz eines laparoskopischen Ansatzes zur Bereitstellung einer Wachstumsfaktor/Xenotransplantat-Kombination in eine subperiostale Tasche zu vorhersehbarer und konsistenter Knochenregeneration. Die biologische Begründung für die Verwendung der „Periostschicht“ wurde kürzlich durch eine experimentelle Studie bestätigt, in der das peri-implantäre osteogene Potenzial des Periosts bei der Bestimmung der vertikalen Knochenaugmentation um Implantate histologisch berichtet wurde. Insgesamt deuten diese Ergebnisse darauf hin, dass die prä- und peri-implantäre Gewebeaugmentation durch chirurgische Verfahren verbessert werden kann, bei denen das Periost intakt gelassen wird, obwohl es vom darunter liegenden Knochen abgetrennt ist, und ein abgeschotteter Raum zwischen dem Periost und dem Knochen oder Implantat erforderlich ist.
Ziel des vorliegenden Fallberichts ist es, eine vereinfachte Technik zur Behandlung von Weichgewebe zu veranschaulichen, nämlich die subperiostale peri-implantäre augmentierte Schicht (SPAL). Die SPAL-Technik wird vorgeschlagen, um die Dimensionen von Hart- und Weichgewebe im koronalsten Bereich eines Implantats zu erhöhen.
Anwendung der SPAL-Technik
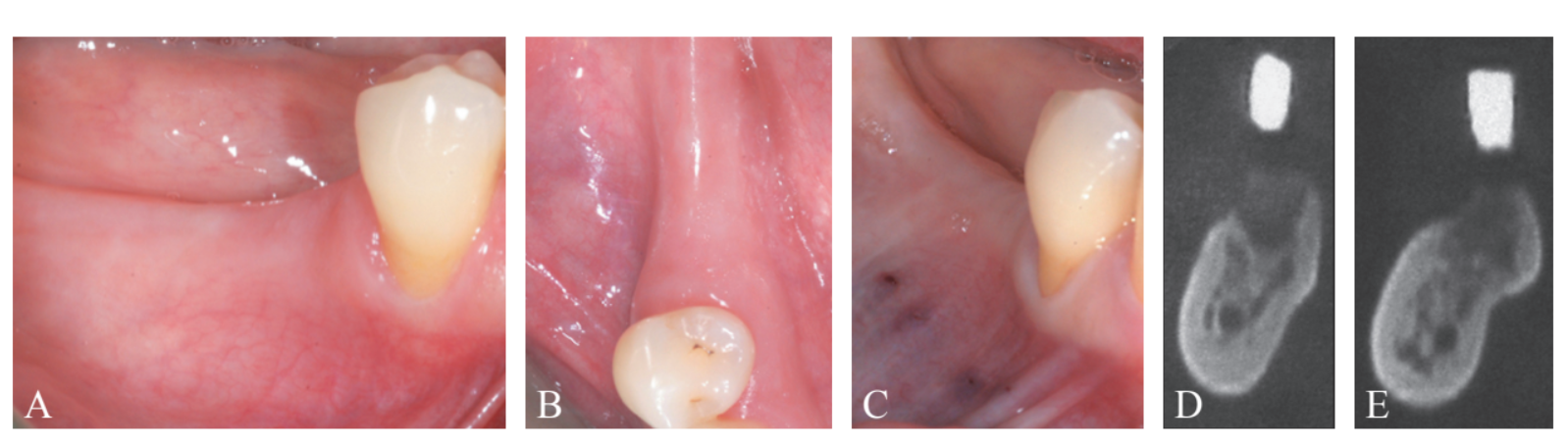
Eine systemisch gesunde, nichtrauchende 61-jährige Frau wurde zur implantatgestützten Rehabilitation am Forschungszentrum für die Studie von Parodontal- und Peri-Implantat-Erkrankungen der Universität Ferrara überwiesen. Vor der Implantation hatte die Patientin eine aktive parodontaltherapeutische Behandlung aufgrund einer schweren Parodontitis durchlaufen und war in ein professionelles sekundäres Präventionsprogramm eingeschrieben. Der Behandlungsplan basierte auf einer 3D-radiografischen Bewertung, und eine chirurgische Schablone wurde auf einem diagnostischen Wachsmodell angefertigt. Die klinische und radiografische Bewertung ergab eine unzureichende horizontale Knochendimension im Bereich der Zähne #4.5 und 4.6, wo die Implantate positioniert werden sollten (Abbildung 1A-E). Der Behandlungsplan wurde der Patientin sorgfältig erklärt, die ihr informierte Zustimmung zu dem vorgeschlagenen chirurgischen Verfahren gab.
Bei der Implantation erhielt der Patient eine Dosis von 2 g Amoxicillin + Clavulansäure (Augmentin, GlaxoSmithKline, Verona, Italien) eine Stunde vor der Operation. Die lokale Anästhesie wurde mit Articain und 1:100.000 Epinephrin durch lokale Infiltration erreicht. Es wurde darauf geachtet, den Bereich, in dem der Spalthautlappen durchgeführt werden muss, nicht zu infiltrieren.
Die chirurgischen Schritte der SPAL-Technik sind in Tabelle I dargestellt.

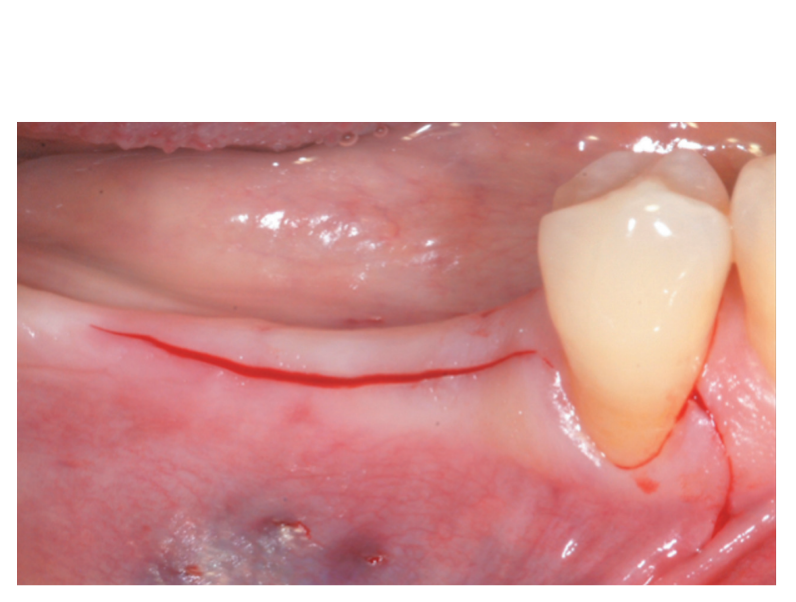
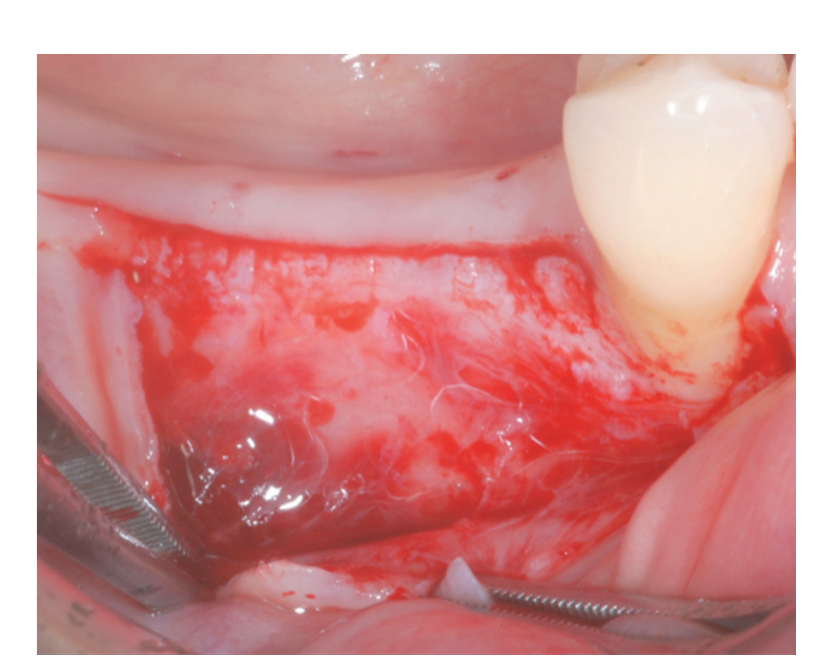
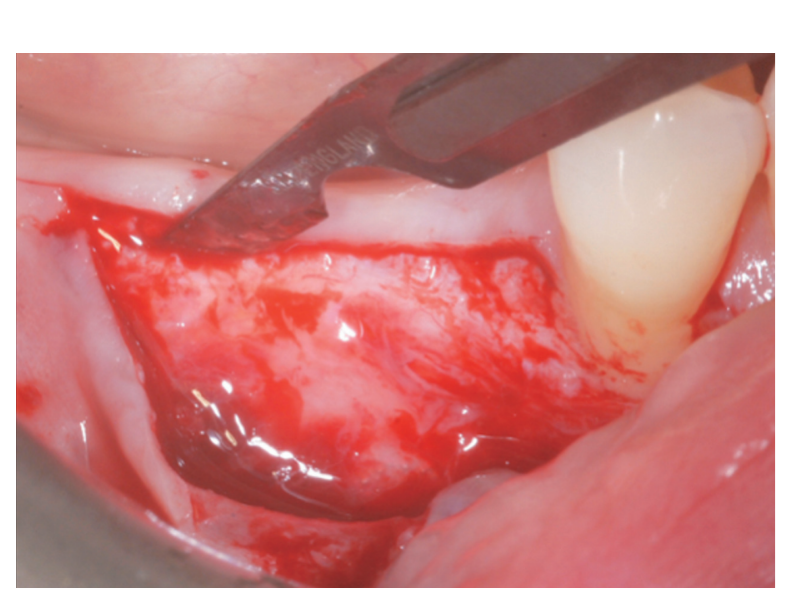
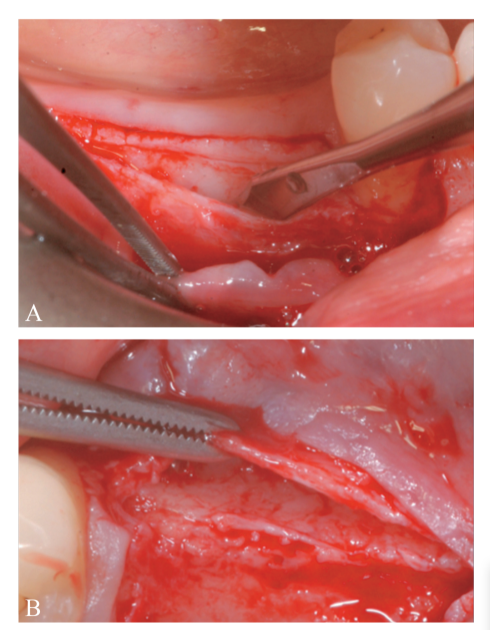
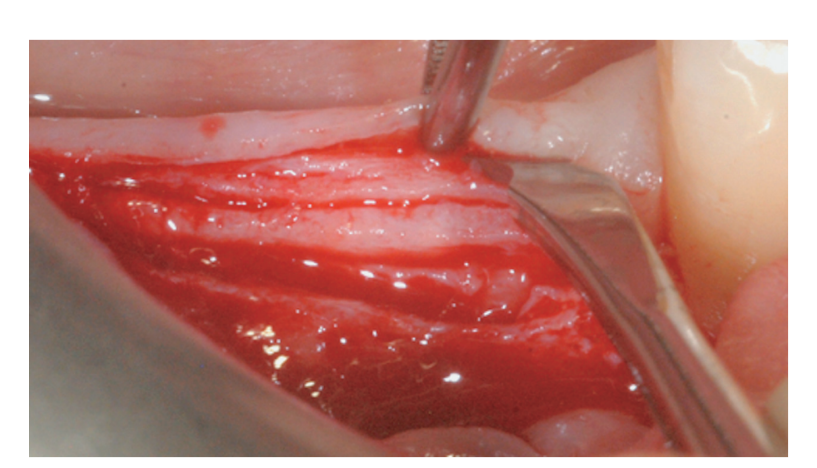
Ein partieller, dünner krester Schnitt wurde mit einer 15C-Klinge durchgeführt. Der Schnitt wurde intra-sulcular an Zahn #4.4 erweitert und ein mesialer, partieller Freischnitt wurde gemacht, um eine bessere Sicht zu erhalten und Spannung auf dem Lappen zu vermeiden (Abbildung 2). Ein split-thickness Lappen wurde an der buccalen Seite durch scharfe Dissektion (nämlich die mukosale Schicht) angehoben und die periostale Schicht auf dem zahnlosen Kamm intakt gelassen (Abbildung 3). Nach der Trennung zwischen der mukosalen und periostalen Schicht, um eine spannungsfreie, koronale Vorverlagerung der mukosalen Schicht zu ermöglichen, wurde ein zweiter krester Schnitt, der die Knochenkante erreichte, durchgeführt (Abbildung 4). Die periostale Schicht wurde von der Knochenkante angehoben, um eine abgeschottete Tasche zu schaffen, die eine angemessene Erweiterung und Volumen des Knochenmaterialtransplantats aufnehmen konnte (Abbildung 5A, B). Ein vollschichtiger Lappen wurde an der oralen (lingualen/palatalen) Seite angehoben (Abbildung 6).
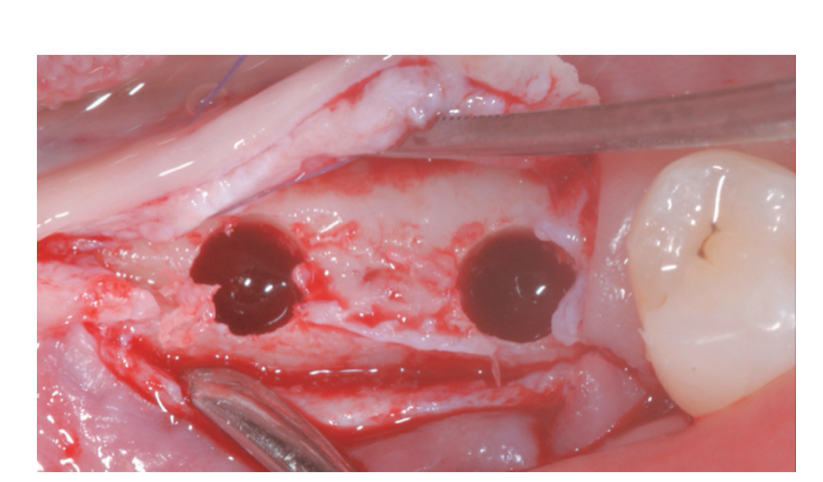
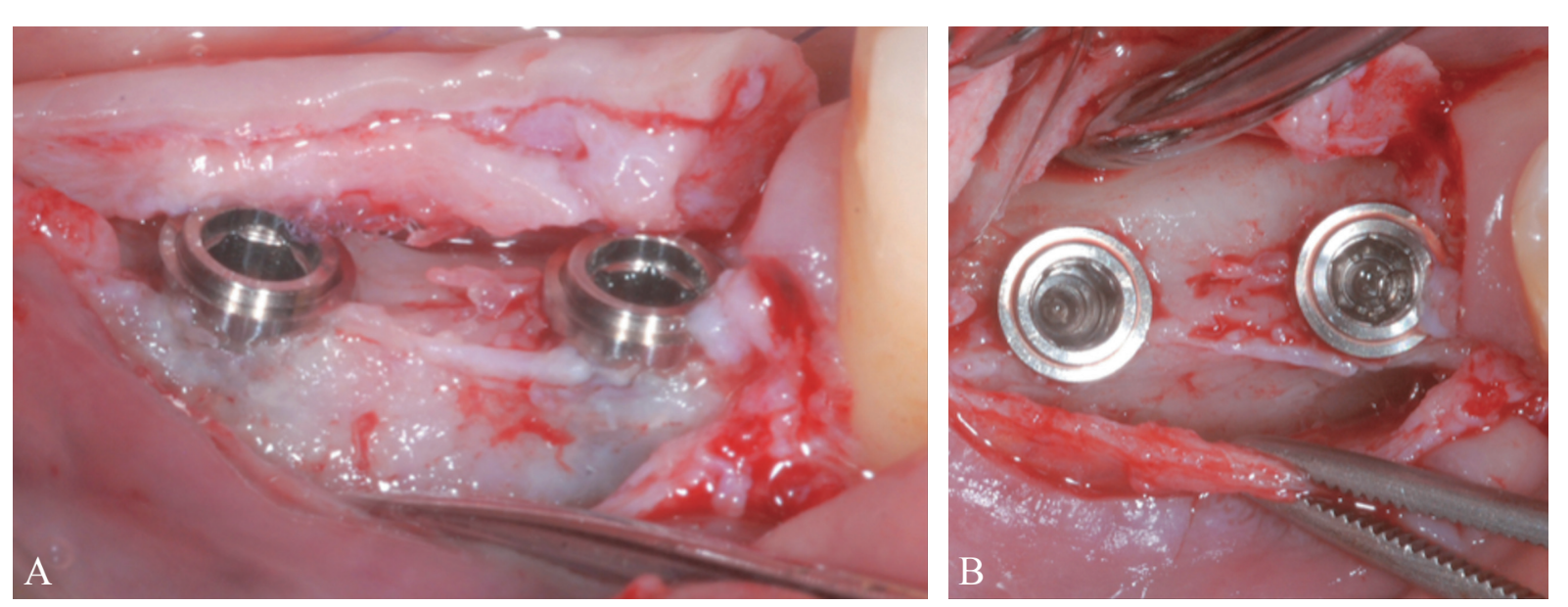
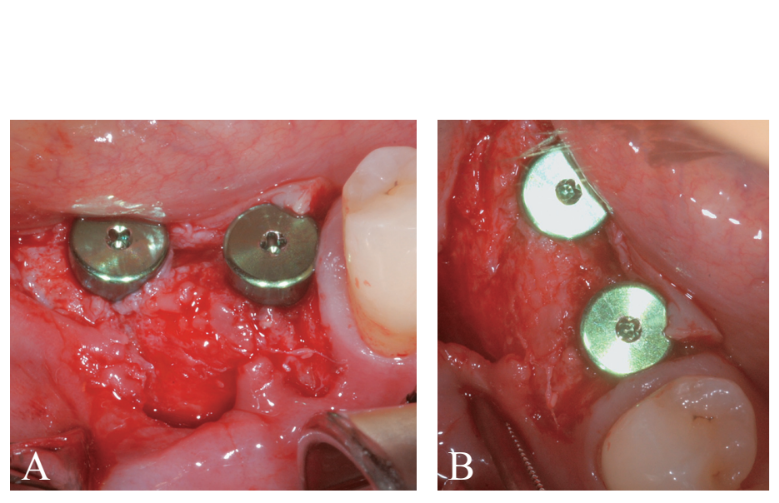
Prothetisch gesteuerte Implantatstandortvorbereitung führte zu einer dünnen BCBP (Abbildung 7). Gewebeebenen-Implantate (Thommen Medical, Grenchen, Schweiz) wurden mit einem 1-mm polierten Kragen über dem Knochenrand platziert (Abbildung 8A, B). Heilungskappen wurden auf beiden Implantaten verwendet. Bio-Oss® Xenograft Spongiosa-Granulate (Partikelgröße 0,25-1,0 mm; Geistlich Pharma, AG, Wolhusen, Schweiz) wurden als Platzhalter verwendet, um den chirurgisch geschaffenen Raum zwischen der periostalen Schicht und der BCBP bis zum polierten Kragen des Implantats zu füllen (Abbildung 9A-C).
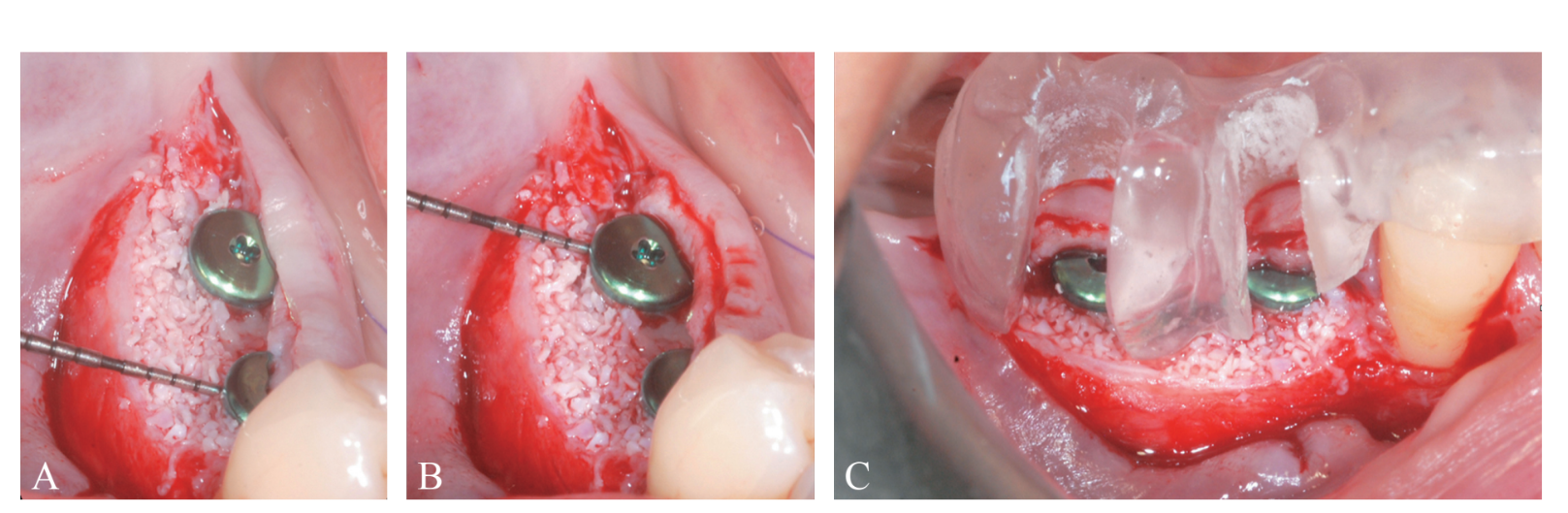
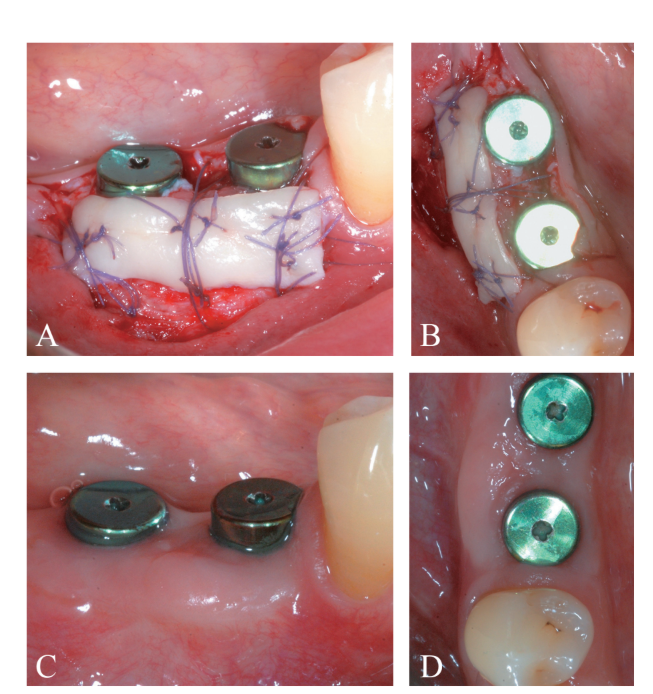
Die periostale Schicht wurde mit Hilfe von internen Matratzennähten an den oralen Mukoperiostlappen genäht (Abbildung 10A, B). Die Mukosaschicht wurde kranial vorgeschoben und spannungsfrei mit horizontalen internen Matratzen- und unterbrochenen Nähten genäht, um sowohl das Transplantat als auch die Implantate zu verbergen (Abbildung 11). Für sowohl die mukosale als auch die periostale Schicht wurde ein resorbierbarer 6/0 Faden (Vicryl 6/0, Ethicon, Somerville, NJ, USA) verwendet.
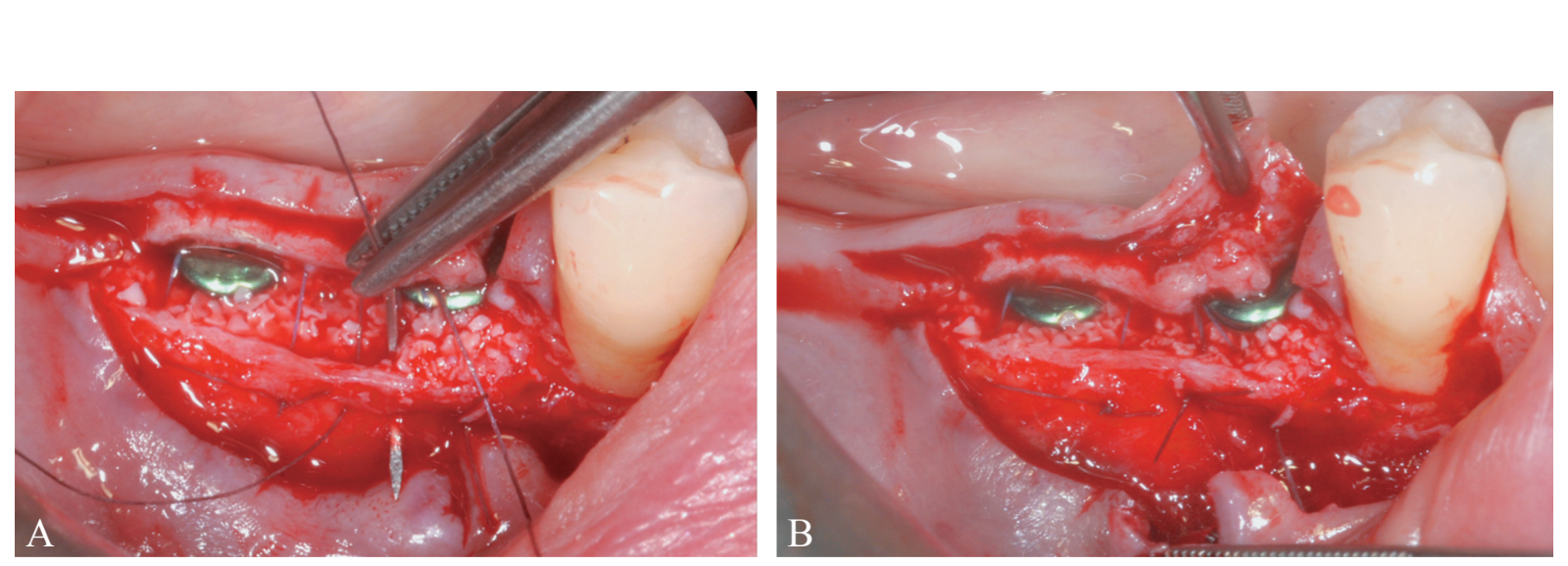
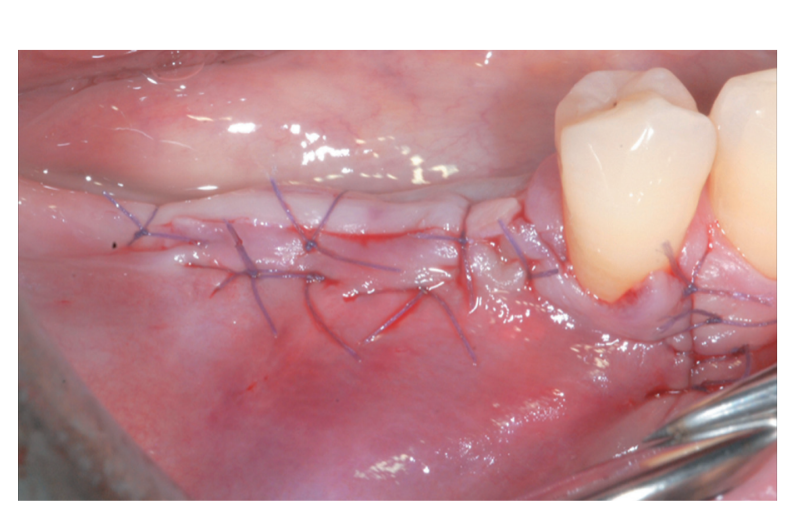
Der Patient trug keine herausnehmbaren Prothesen, um Druck auf die Operationsstelle zu vermeiden, und wurde gebeten, etwa 2 Wochen lang im behandelten Bereich nicht zu kauen oder zu putzen. Die häusliche Anwendung einer 0,12%igen Chlorhexidinlösung (Curasept ADS Trattamento Rigenerante®, Curaden Healthcare, Saronno, Italien) wurde zur chemischen Plaque-Kontrolle verschrieben (1-minütiges Spülen b.i.d. für 3 Wochen). Die Nähte wurden 2 Wochen nach der Operation entfernt.
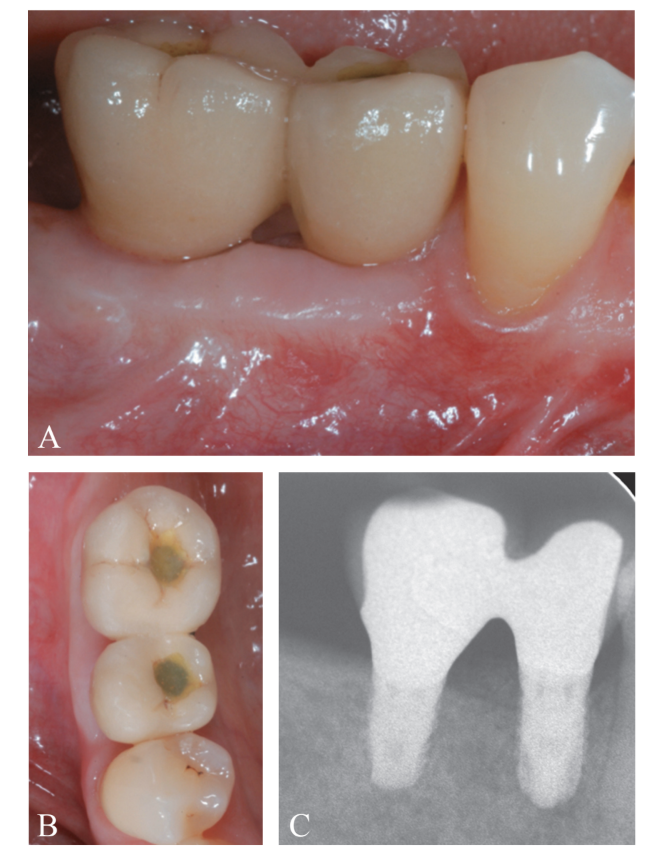
Vier Monate nach der Implantation wurde ein Re-Entry-Verfahren zur Freilegung des Implantats durchgeführt (Abbildung 12A-C). Ein bukkaler Spalthautlappen wurde angelegt, um das Heilungsabutment zu positionieren, wobei darauf geachtet wurde, eine erhebliche Gewebedicke zu belassen, um den koronalen Teil des Implantats zu schützen (Abbildung 13A, B). Es wurde eine Zunahme der Dicke (>2 mm) des bukkalen peri-implantären Gewebes beobachtet. In diesem speziellen Fall, da die koronale Verschiebung des Lappens während des ersten chirurgischen Eingriffs zu einem Mangel an ausreichendem bukkalen peri-implantären Mukosa führte, wurde ein freies epithelialisiertes Zahnfleischtransplantat im koronalen Bereich der Implantate positioniert (Abbildung 14A-D). Die endgültige prothetische Rehabilitation ist in Abbildung 15A-C dargestellt.
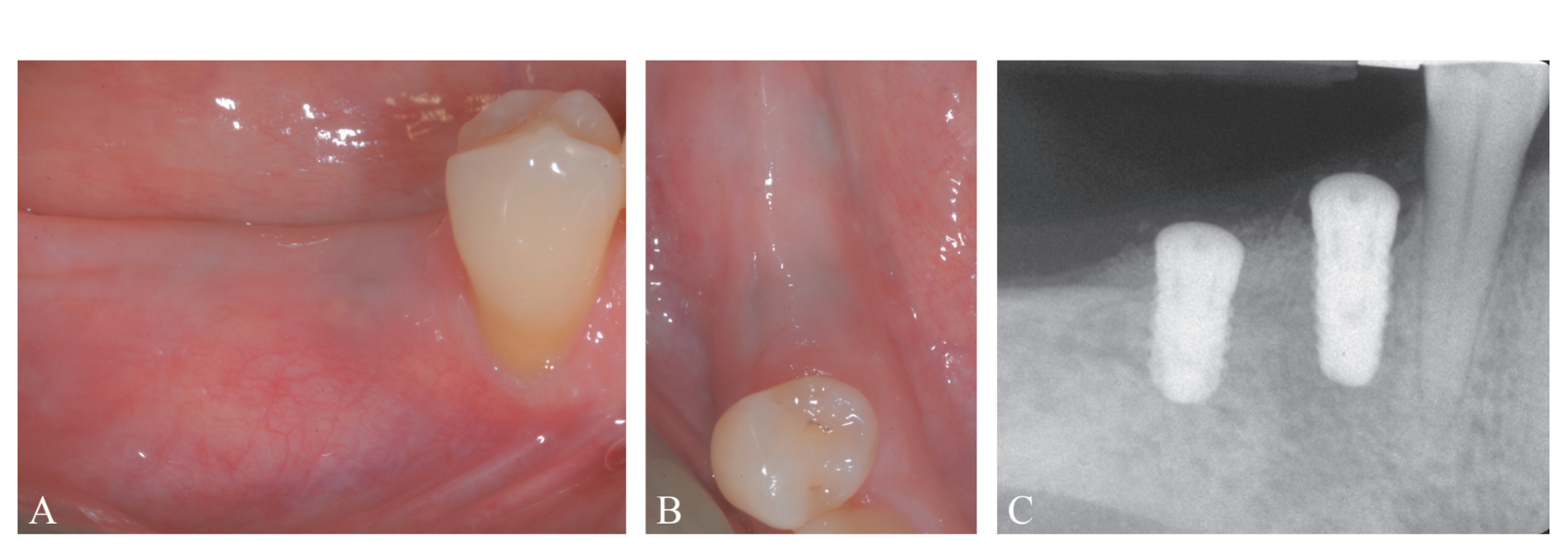
Diskussion
Die SPAL-Technik stammt von der Double Flap-Inzision, wie ursprünglich von Hur et al. vorgeschlagen und von Steigmann et al. modifiziert. Dieses Design umfasst eine Teil-Thickness-Flap-Erhebung, die die periostale Schicht auf dem zahnlosen Kamm belässt, und die Trennung der mukosalen Schicht des Lappens. Die periostale Schicht wird dann verwendet, um den regenerativen Bereich mit periostalen Nähten zu stabilisieren. Verschiedene regenerative Geräte, wie nicht resorbierbare/resorbierbare Membranen und Titan-Gitter in unterschiedlichen Größen und Positionen, wurden sowohl für die horizontale als auch für die vertikale Implantatstandortentwicklung verwendet. Kürzlich wurde ein ähnliches Lappendesign berichtet, das GBR für die horizontale Knochenaugmentation vor der Implantation durchführt. Eine periostale Tasche wurde durch das Spalten einer Mukosa von einer periostalen Schicht geschaffen, und der geschaffene subperiostale Raum wurde dann mit Knochenersatzmaterialien gefüllt und mit einer resorbierbaren Membran abgedeckt. Nach 6 Monaten wurde ein erheblicher Anstieg der horizontalen Knochenkamm-Dimensionen verzeichnet. Die SPAL-Technik profitiert von den Vorteilen der beiden vorherigen Techniken in Bezug auf das Lappendesign und die Schaffung eines subperiostalen Raums, der darauf abzielt, ein osteokonduktives Gerüst zu erhalten.8 Unser Vorschlag ist jedoch durch zwei wesentliche technische Unterschiede gekennzeichnet, die das Verfahren vereinfachen und gleichzeitig zu vorhersehbaren Ergebnissen führen: 1) die Erhöhung des BCBP erfolgt zum Zeitpunkt der Implantation; 2) die verbesserte horizontale Dimension beruht lediglich auf dem osteogenetischen Potenzial, das dem Periost innewohnt, ohne den Einsatz von Membranen.
Die SPAL-Technik basiert auf dem sogenannten PASS-Prinzip, das die primäre Wundabdeckung, Angiogenese, Schaffung von Raum und Wundstabilität umfasst.
Raum ist notwendig, damit die osteogenen Zellen in die Wundstelle eindringen, sich zu Osteoblasten differenzieren und geflechtartiges Knochengewebe bilden können. Die Stabilität des abgeschotteten Raums, der das Transplantat-Biomaterial enthält, das als Gerüst für die Bildung und Reifung des Blutgerinnsels dient, wurde wiederholt für die Knochenregeneration betont. In unserer Technik wurde die Schaffung von Raum gewährleistet durch: 1) die Schaffung einer subperiostalen Tasche, die nur in ihrem koronalen Bereich geöffnet ist, während sie an den mesialen, apikalen und distalen Aspekten nicht vom darunterliegenden Knochen abgetrennt ist; und 2) die Verwendung von langsam resorbierbarem Xenograft, das mit begrenzter Dispersion und minimalen Mikrobewegungen eingesetzt und stabilisiert wurde.
Deproteinierte bovine Knochenpartikel könnten ein geeignetes osteokonduktives Gerüst für die Bildung neuen Knochengewebes geschaffen haben, während sie mechanisch die periostale Schicht vom darüber liegenden Implantat und der Knochenoberfläche abgehoben halten. Frühere Studien haben gezeigt, dass die Elevation des Periosts durch verschiedene Geräte zur Induktion der suprakortikalen peri-implantären Knochenbildung führte. Die Periostschicht könnte nicht nur eine Quelle für osteogenetische Zellen darstellen, sondern auch effektiv zur Angiogenese beitragen, die eine Voraussetzung für die Bildung neuen Knochengewebes ist. Obwohl der präsentierte Fall keine Informationen über die Beschaffenheit der augmentierten Gewebe zuließ, zeigte die menschliche Histologie, die aus einem ähnlichen Verfahren stammt, bei dem eine subperiostale Tasche chirurgisch geschaffen wurde, dass Xenograft-Partikel von neu gebildetem Knochen umgeben waren.
Unser Klappendesign ermöglicht die Mobilisierung von Weichgewebe, was zu einer spannungsfreien primären Verschlussführung führt, einem Zustand, der als wesentlich angesehen wird, um eine ungestörte Knochenregeneration zu erreichen. Der primäre Verschluss wurde durch zwei Faktoren erleichtert: 1) Die Menge an horizontaler Knochenresorption korreliert positiv mit der Dicke des Weichgewebes; 2) Das Einbringen von Transplantaten war auf den koronalsten Teil des Implantats beschränkt.
Fazit
Zusammenfassend könnte die SPAL-Technik eine wertvolle chirurgische Option bei der horizontalen Augmentation der Dicke des peri-implantären Gewebes darstellen. Weitere longitudinale Studien sind erforderlich, um zu bewerten, ob und in welchem Umfang dieses Verfahren zur Behandlung von peri-implantären Knochendehiszenzen eingesetzt werden kann und ob es in der Lage ist, langfristige Stabilität des buccalen Mukosaprofiles und gesunde Bedingungen des peri-implantären Gewebes zu fördern.
Leonardo Trombelli, Mattia Severi, Mattia Pramstraller, Roberto Farina
Referenzen
- Spray JR, Black CG, Morris HF, Ochi S. Der Einfluss der Knochendicke auf die Reaktion des Gesichtsrandknochens: Platzierung in Phase 1 bis Freilegung in Phase 2. Ann Periodontol 2000;5:119–28.
- Le B, Burstein J. Ästhetisches Transplantat für kleine Volumen von harten und weichen Gewebe-Konturdefekten zur Entwicklung von Implantatstandorten. Implant Dent 2008;17:136–41.
- Block MS, Degen M. Horizontale Knochenerweiterung mit humanem mineralisiertem Partikelknochen: vorläufige Ergebnisse. J Oral Maxillofac Surg 2004;62(Suppl 2):67–72.
- Block MS. Horizontale Knochenerweiterung mit Partikelknochen. Atlas Oral Maxillofac Surg Clin North Am 2006;14:27–38.
- Le B, Burstein J, Sedghizadeh PP. Kortikale Zelttransplantationstechnik im stark atrophen Alveolarkamm zur Vorbereitung des Implantatstandorts. Implant Dent 2008;17:40–50.
- Park SH, Lee KW, Oh TJ, Misch CE, Shotwell J, Wang HL. Einfluss von resorbierbaren Membranen auf die Sandwich-Knochenerweiterung. Clin Oral Implants Res 2008;19:32–41.
- Cortes AR, Cortes DN, Arita ES. Korrektur der buccalen Dehiszenz zum Zeitpunkt der Implantatplatzierung ohne Barrieremembranen: eine retrospektive Studie mit Cone-Beam-Computertomographie. Int J Oral Maxillofac Implants 2013;28:1564–9.
- Steigmann M, Salama M, Wang HL. Periostale Taschenklappen für die horizontale Knochenregeneration: eine Fallserie. Int J Periodontics Restorative Dent 2012;32:311–20.
- Lee EA. Subperiostale minimalinvasive ästhetische Knochenerweiterungstechnik (SMART): Ein neuer Standard für die Knochenrekonstruktion der Kiefer. Int J Periodontics Restorative Dent 2017;37:165–73.
- Lutz R, Sendlbeck C, Wahabzada H, Tudor C, Prechtl C, Schlegel KA. Periostale Elevation induziert suprakortikale peri-implantäre Knochenbildung. J Craniomaxillofac Surg 2017;45:1170–8.
- Hur Y, Tsukiyama T, Yoon TH, Griffin T. Doppelte Klappeninzision für die geführte Knochenregeneration: eine neuartige Technik und klinische Überlegungen. J Periodontol 2010;81:945–52.
- Wang HL, Boyapati L. „PASS“-Prinzipien für vorhersehbare Knochenregeneration. Implant Dent 2006;15:8–17.
- Tudor C, Bumiller L, Birkholz T, Stockmann P, Wiltfang J, Kessler P. Statische und dynamische periostale Elevation: eine Pilotstudie in einem Schweinemodell. Int J Oral Maxillofac Surg 2010;39:897–903.
- Dziewiecki D, van de Loo S, Gremse F, Kloss-Brandstätter A, Kloss F, Offermanns V, et al. Osteoneogenese durch periostale Elevation mit abbaubaren und nicht abbaubaren Geräten in Göttinger Minischweinen. J Craniomaxillofac Surg 2016;44:318–24.