Peri-Implantäre Knochenaugmentation durch die subperiostale peri-implantäre augmentierte Schichttechnik und einen bovinen Knochenblock: Ein Fallbericht
Maschinenübersetzung
Der Originalartikel ist in EN Sprache (Link zum Lesen) geschrieben.
Hintergrund: Bei der Verwendung von deproteinisiertem bovinem Knochenmineral (DBBM), das als Partikel geliefert wird, war die subperiostale peri-implantäre augmentierte Schicht (SPAL)-Technik effektiv, um bis zu 92 % der peri-implantären buccalen Knochendefekte vollständig zu korrigieren. Die Verwendung eines DBBM-Blocks (bDBBM) kann jedoch zu einer Verbesserung des peri-implantären Knochendefekts sowie zu einer relevanten lateralen Knochenaugmentation führen, da seine mechanischen Eigenschaften eine bessere dimensionsstabilität bei der Klappenmanipulation als partikuläres DBBM gewährleisten können. Ziel des vorliegenden Proof-of-Principle-Fallberichts ist es zu untersuchen, ob SPAL erfolgreich zur Knochenaugmentation an peri-implantären Defektstellen eingesetzt werden kann, wenn es mit bDBBM verwendet wird.
Fallpräsentation: Eine laterale Knochenaugmentation wurde mit der SPAL-Technik an zwei Implantaten durchgeführt, die unmittelbar nach ihrer Platzierung einen buccalen peri-implantären Knochendefekt aufwiesen. Eine Teilklappe wurde angehoben, wobei die periostale Schicht auf der buccalen kortikalen Knochenplatte belassen wurde. Die periostale Schicht wurde wiederum angehoben, um eine Tasche zu schaffen, die verwendet wurde, um ein bDBBM-Transplantat an den peri-implantären buccalen Knochendefekten zu stabilisieren. Bei der Wiederöffnung waren die exponierten Implantatoberflächen vollständig mit neuem dickem Hartgewebe bis zu ihrem kranialsten Teil bedeckt. Ein freies epithelial-bindegewebiges Transplantat wurde verwendet, um den peri-implantären Weichgewebsphänotyp zu augmentieren.
Fazit: Wenn SPAL verwendet wird, um bDBBM über den koronalsten Teil eines exponierten Implantats zu platzieren, kann dies erfolgreich zu einer Zunahme der peri-implantären buccalen Gewebedicke führen. Clin Adv Periodontics 2022;12:39–43.
Hintergrund
Eine vereinfachte Technik zur Augmentierung der knöchernen Komponente des peri-implantären Phänotyps bei der Implantation, nämlich die sub-periostale peri-implantäre augmentierte Schicht (SPAL), wurde kürzlich vorgeschlagen. SPAL basiert auf der Trennung des buccalen Lappens in zwei Schichten: einer periostalen Schicht, die einen „osteogenen“ geschützten Raum schafft, um ein Transplantat bei einer dünnen oder defizienten peri-implantären buccalen Knochenplatte zu stabilisieren, und einer mukosalen Schicht, die mobilisiert wird, um eine primäre Wundheilung zu ermöglichen. Frühere Studien haben gezeigt, dass SPAL zu einer erheblichen Korrektur von Dehiszenzen führen kann, wodurch Bedingungen für die peri-implantäre Gesundheit an den behandelten Implantaten geschaffen werden. Außerdem hat sich gezeigt, dass SPAL bei der Behandlung von Dehiszenz-typischen peri-implantären Defekten, die mit einem interproximalen oder zirkumferentialen Bestandteil verbunden sind, wirksam ist.
In allen Fällen, die mit SPAL behandelt wurden, wurde ein deproteinisiertes bovines Knochenmineral (DBBM) – geliefert als Partikel – zwischen der periostalen Schicht und der freiliegenden Implantatoberfläche untergebracht. Obwohl es sich als effektiv erwiesen hat, als raumschaffendes osteokonduktives Gerüst eine vollständige Abdeckung von peri-implantären Knochendefekten zu erreichen, könnte das partikuläre DBBM mit einer begrenzten Zunahme der Dicke der buccalen Knochenplatte verbunden sein.
Präklinische und klinische Studien scheinen darauf hinzudeuten, dass die geführte Knochenregeneration (GBR) zu einer Verbesserung des peri-implantären Knochendefekts sowie zu einer relevanten lateralen Knochenaugmentation führen kann, wenn sie mit einem DBBM-Block (bDBBM) verwendet wird. Die vorliegende Studie besteht aus einem Proof-of-Principle-Fallbericht, der darauf abzielt zu untersuchen, ob SPAL erfolgreich zur Knochenaugmentation an peri-implantären Defektstellen eingesetzt werden kann, wenn es mit bDBBM verwendet wird.
Ethik Aspekte
Der vorliegende Bericht wurde vom Ethikkomitee des Bereichs Vasta Emilia Centro, Italien (Protokoll Nr. 637/2018/Oss/UniFe, Datum der Genehmigung 12.12.2018) genehmigt. Der Patient hat vor der chirurgischen Behandlung eine schriftliche informierte Einwilligung gegeben. Alle klinischen Verfahren wurden in Übereinstimmung mit der Deklaration von Helsinki und den Richtlinien für gute klinische Praxis durchgeführt.
Klinische Präsentation, Fallmanagement und klinische Ergebnisse
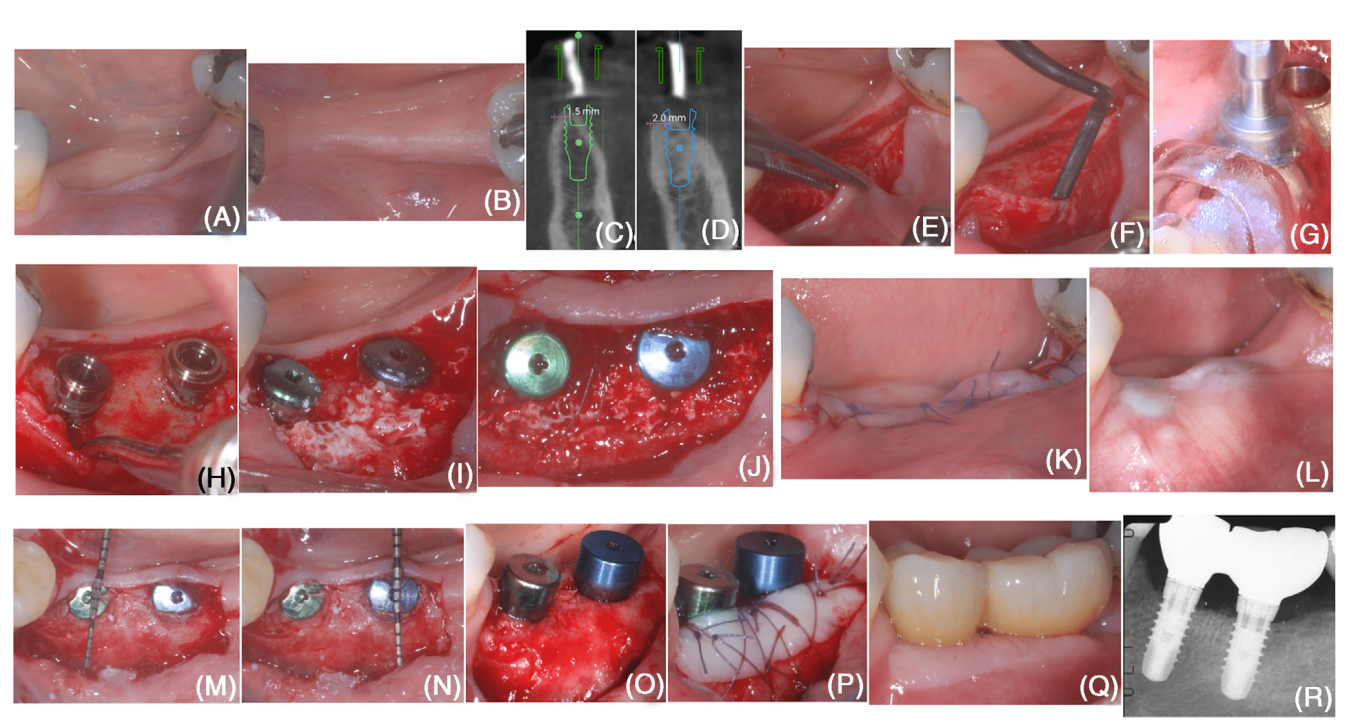
Im Oktober 2020 stellte sich eine 50-jährige, nichtrauchende, systemisch gesunde Patientin zur Rehabilitation eines zahnlosen Bereichs (#18 und #19; Abbildungen 1A,B). Nach Behandlung der Parodontitis im Stadium III wies die Patientin einen Blutungs-auf-Sondierung-Wert <10% und keine Stellen mit einer Sondierungstiefe ≥ 5 mm auf und wurde in ein unterstützendes
Parodontalpflegeprogramm. Eine implantatgestützte Rehabilitation wurde im Bereich #18 und #19 geplant.
Die Implantatposition wurde digital anhand einer Cone-Beam-Computertomographie-Untersuchung geplant, und eine chirurgische Schablone wurde angefertigt (Abbildung). Die digitale Planung zeigte die Bildung einer bukkalen Dehiszenz bei der Platzierung beider Implantate, was auf die Notwendigkeit eines horizontalen Knochenaufbauverfahrens hinweist (Abbildungen 1C,D).
Dem Patienten wurden 2 g Amoxicillin + Clavulansäure 1 Stunde vor der Operation verabreicht. Die lokale Anästhesie wurde mit Articain und 1:100.000 Epinephrin durch lokale Infiltration erreicht.
Im bukkalen Bereich wurde ein Spalthautlappen (der die „mukosale Schicht“ bildet) angehoben, wobei die periostale Schicht auf dem zahnlosen Kamm intakt blieb (Abbildung 1E). Dann wurde die periostale Schicht mit einem mikrosurgischen Periostheber und tunnelförmigen Messern mit unterschiedlich gewinkelten scharfen Kanten vom Knochenrand abgehoben (Abbildung 1F). Im lingualen Bereich wurde ein Vollhautlappen angehoben. Die Anhebung wurde in apikale Richtung verlängert, um die oberflächlichen Fasern des Mylohyoid-Muskels zu lösen und einen spannungsfreien lingualen Lappen zu erhalten.
Implantatstellen wurden mit dem computerassistierten chirurgischen Führer vorbereitet (Abbildung 1G), und zwei Gewebe-Implantate wurden positioniert (Abbildung 1H). Die Implantate wiesen eine buccale Dehiszenz (gemessen als der Abstand zwischen dem apikalen Rand des polierten Kragens des Implantats und dem Knochenrand an der buccalen Seite des Implantats) von 3 mm bei #19 und 2 mm bei #18 auf. Kortexperforationen wurden mit einem Hartmetallbohrer durchgeführt.
bDBBM wurde mit einem Hochgeschwindigkeits-Diamantbohrer zugeschnitten, um eine homogene Dicke von 3–4 mm zu erhalten, und wurde unter der periostalen Schicht angepasst, um die freiliegende Implantatoberfläche vollständig zu bedecken (Abbildung 1I). Mit einem resorbierbaren 6/0-Faden wurde die periostale Schicht durch interne Matratzenstiche am lingualen Lappen stabilisiert (Abbildung 1J). Die mukosale Schicht wurde coronar vorverlagert, um eine primäre Wundverschluss zu erreichen (Abbildung 1K).
Der Patient wurde angewiesen, jegliche Kompression des chirurgischen Bereichs zu vermeiden und in dem behandelten Bereich für 2 Wochen nicht zu kauen oder zu putzen. Eine 0,12% Chlorhexidin-Mundspülung wurde verschrieben (1-min Spülung b.i.d. für 3 Wochen). Die Nähte wurden 2 Wochen nach der Operation entfernt.
Sechs Monate nach der Implantation (Abbildung 1L) wurde ein Wiederherstellungsverfahren zur Implantatexposition unter Verwendung eines bukkalen Spalthautlappens durchgeführt. Die zuvor exponierten Implantatoberflächen waren vollständig mit neuem Gewebe bedeckt, das an der krönsten Stelle beider Implantate mindestens 3 mm dick war (Abbildungen 1M–O). Das rekonstruierte Gewebe bot einen klaren Widerstand gegen das Eindringen mit einer parodontalen Sonde, als diese mit einer Prüfkraft von etwa 50 N durch den geschulten Bediener verwendet wurde. Ein freies epithelial-bindegewebiges Transplantat wurde verwendet, um den peri-implantären Weichgewebsphänotyp zu augmentieren (Abbildung 1P).
Ein digitaler Abdruck wurde 4 Wochen nach der Implantatexposition genommen. Die Form und das Notfallprofil der endgültigen Restauration wurden digital geplant. Zwei verbundene Kronen wurden aus einem Zirkonia-Monoblock gefräst und gemäß den Anweisungen des Herstellers auf die Titan-Einsätze zementiert. Die endgültige Restauration wurde 4 Wochen nach dem Abdruck verschraubt.
Die peri-implantären Gewebebedingungen erschienen sowohl bei der klinischen als auch bei der radiografischen Untersuchung als angemessen (Abbildungen 1Q–R).
Diskussion
Der vorliegende Fallbericht legt nahe, dass bDBBM eine geeignete Alternative zu partikulärem DBBM darstellen könnte, wenn die SPAL-Technik zur Knochenaugmentation an peri-implantären Dehiszenzstellen angewendet wird.
Bei der SPAL-Technik wird die Stabilisierung des Transplantats im subperiostalen Raum durch das Nähen des koronalsten Teils sichergestellt (was die schädliche Wirkung mechanischer Störkräfte auf die Mischung aus Gerinnsel/Transplantat begrenzt und den engen Kontakt letzterer mit der hoch vaskularisierten Struktur des Periosts begünstigt) und anschließend durch die mukosale Schicht abgedeckt. Ein potenzieller Nachteil bei der Verwendung von partikulärem DBBM ist die mögliche Verschiebung und/oder Kompression der Transplantatpartikel rund um den koronalen Teil des Implantats beim Nähen. Diese Überlegung ist in der Literatur gut belegt für die Assoziation von partikulärem DBBM und GBR. Im Gegensatz dazu könnte bDBBM als wirksames osteokonduktives Gerüst wirken, während seine mechanischen Eigenschaften eine bessere dimensionsstabilität bei der Klappenmanipulation gewährleisten würden. Frühere präklinische und klinische Studien scheinen unsere Ergebnisse zu bestätigen. Andererseits erfordert die Steifheit des Blocktransplantats eine ideale passive Anpassung der mukosalen Schicht, um das Risiko einer Klappenperforation und Transplantatexposition zu minimieren.
Die Freilegung des Implantats wurde durch einen Spalthautlappen durchgeführt, wodurch eine direkte Inspektion der rekonstruierten Gewebe unter dem Periost verhindert wurde. Zusammen mit dem Fehlen einer histologischen Analyse und/oder einer postoperativen dreidimensionalen radiografischen Bewertung des peri-implantären Raums verhindert dies die Möglichkeit, irgendwelche Schlussfolgerungen über die Beschaffenheit der rekonstruierten Gewebe an der zuvor freigelegten bukkalen Seite der Implantate zu ziehen. Obwohl die Gewebedicke (≥ 3 mm) und ihre hohe Widerstandsfähigkeit gegen Sondierungsdurchdringung bei der Wiederaufnahme auf das Vorhandensein einer mineralisierten Komponente in einem fortgeschrittenen Reifungsstadium hindeuten könnten, bleibt jede Überlegung zur Qualität der subperiostalen Gewebe spekulativ und basiert ausschließlich auf der mechanischen Wahrnehmung des Operateurs während der Sondierungsinspektion. Verfügbare Daten aus experimentellen Studien und 6-monatigen menschlichen histologischen Proben, bei denen bDBBM für die laterale Knochenaugmentation verwendet wurde, zeigten eine begrenztere Neubildung von Knochen, die hauptsächlich an der Schnittstelle zwischen dem nativen Knochen und bDBBM lokalisiert war, im Vergleich zu partikulärem DBBM. Diese Beobachtungen scheinen die Notwendigkeit zu verstärken, die osteogenen Bedingungen der Wunde zu verbessern (z. B. kortikale Perforationen, Verwendung zusätzlicher Wachstumsfaktoren) und/oder eine längere Reifungszeit vor der Freilegung des Implantats abzuwarten, wenn bDBBM verwendet wird. Klinische Beobachtungen aus dem vorliegenden Fallbericht kumulieren mit früheren Beweisen aus Fallberichten und retrospektiven Fallserien zur SPAL-Technik. Insgesamt zeigen die Daten, dass SPAL erfolgreich für die peri-implantäre Knochenaugmentation mit einem bovinen Xenograft in einer Vielzahl klinischer Szenarien in Bezug auf die Implantat-Topographie (d. h. anterior/posterior Sextant und maxilläre/mandibuläre Bogen) sowie die Bedingungen der bukkalen Knochenplatte zum Zeitpunkt der Implantation eingesetzt werden kann. Insbesondere wurde eine klinisch relevante Augmentation für Implantate mit entweder einer bukkalen Knochendefizienz oder einer intakten, aber dünnen bukkalen Knochenplatte bei der Platzierung berichtet. Bei Implantaten mit Knochendefizienz wurden Defekttiefen von bis zu 6 mm erfolgreich mit SPAL korrigiert. Leider ist, obwohl ermutigend, die verfügbare Datenbasis nicht ausreichend, um entweder die lokalen Indikationen/Kontraindikationen der SPAL-Technik klar zu umreißen oder zu klären, welche Faktoren die klinischen Ergebnisse des Verfahrens beeinflussen können.
Fazit
Der vorliegende Proof-of-Principle Fallbericht zeigt, dass die SPAL-Technik erfolgreich eingesetzt werden kann, um bDBBM über den koronalsten Teil eines exponierten Implantats zu platzieren und eine Zunahme der peri-implantären buccalen Gewebedicke zu erreichen.
Leonardo Trombelli, Mattia Severi, Luca Ortensi und Roberto Farina
Literaturverzeichnis
- Avila-Ortiz G, Gonzalez-Martin O, Couso-Queiruga E, Wang HL. Der peri-implantäre Phänotyp. J Periodontol. 2020;91:283-288.
- Trombelli L, Severi M, Pramstraller M, Farina R. Subperiostale peri-implantäre augmentierte Schichttechnik zur horizontalen Knochenaugmentation bei der Implantation. Minerva Stomatol. 2018;67:217-224.
- Trombelli L, Severi M, Pramstraller M, Farina R. Ein vereinfachtes Management von Weichgewebe für die peri-implantäre Knochenaugmentation. Int J Oral Maxillofac Implants. 2019;34:197-204.
- Trombelli L, Pramstraller M, Severi M, Simonelli A, Farina R. Peri-implantäre Gewebebedingungen bei Implantaten, die mit der Subperiostalen Peri-implantären Augmentierten Schichttechnik behandelt wurden: eine retrospektive Fallserie. Clin Oral Impl Res. 2020;31:992-1001.
- Trombelli L, Severi M, Farina R, Simonelli A. Subperiostale peri-implantäre augmentierte Schichttechnik zur Behandlung von peri-implantären Läsionen. Clin Adv Periodontics. 2020;10:169-174.
- Benic GI, Thoma DS, Munoz F, Martin IS, Jung RE, Hämmerle CHF. Geführte Knochenregeneration von peri-implantären Defekten mit partikulierter und blockartiger xenogenen Knochenersatzmaterialien. Clin Oral Impl Res. 2016;27:567-576.
- Benic GI, Thoma DS, Sanz-Martin I, et al. Geführte Knochenregeneration an Zirkonium- und Titan-Zahnimplantaten: eine pilot-histologische Untersuchung. Clin Oral Impl Res. 2017;00:1-9.
- Benic GI, Eisner BM, Jung RE, Basler T, Schneider D, Hämmerle CHF. Veränderungen des Hartgewebes nach geführter Knochenregeneration von peri-implantären Defekten im Vergleich von Block- zu Partikeln-Knochenersatzmaterialien: 6-Monats-Ergebnisse einer randomisierten kontrollierten klinischen Studie. Clin Oral Impl Res. 2019;30:1016-1026.
- Ainamo J, Bay I. Probleme und Vorschläge zur Aufzeichnung von Gingivitis und Plaque. Int Dent J. 1975;25:229-235.
- Mir-Mari J, Wui H, Jung RE, Hämmerle CHF, Benic GI. Einfluss der blinden Wundverschluss auf die Volumenstabilität verschiedener GBR-Materialien: eine in vitro Cone-Beam-Computertomographie-Untersuchung. Clin Oral Impl Res. 2015;27:258-265.
- Naenni N, Berner T, Waller T, Huesler J, Hammerle CHF, Thoma DS. Einfluss des Wundverschlusses auf die Volumenstabilität bei Anwendung verschiedener GBR-Materialien: eine in vitro Cone-Beam-Computertomographie-Studie. J Periodontal Implant Sci. 2019;49:14-24.
- Laass A, Hämmerle CHF, Jung RE, Thoma DS, Benic GI. Histologische Ergebnisse nach geführter Knochenregeneration von peri-implantären Defekten im Vergleich von individuell geformten Block- zu Partikeln-Knochenersatzmaterialien. Int J Periodontics Restorative Dent. 2020;40:519-527.
- Araujo MG, Sonohara M, Hayacibara R, Cardaropoli G, Lindhe J. Laterale Kammaugmentation durch den Einsatz von Transplantaten aus autologem Knochen oder einem Biomaterial. Ein Experiment am Hund. J Clin Periodontol. 2002;29:1122-1131.
- Oda A, Kinoshita K, Ueda M. Auswirkungen der Perforation des kortikalen Knochens auf die periostale Ablenkung: eine experimentelle Studie am Kaninchenunterkiefer. J Oral Maxillofac Surg. 2009;67:1478-1485.
- Schwarz F, Rothamel D, Herten M, Ferrari D, Sager M, Becker J. Laterale Kammaugmentation unter Verwendung von partikulierter oder blockartiger Knochenersatzmaterialien, die mit rhGDF-5 und rhBMP-2 biobeschichtet sind: eine immunhistochemische Studie an Hunden. Clin Oral Impl Res. 2008;19:642-652.